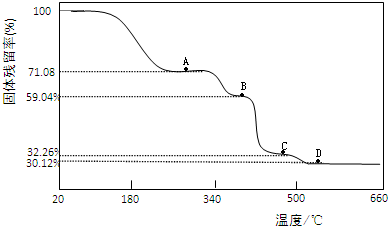
题目内容
下列说法中正确的是( )
| A、乙炔分子中,每个碳原子都有两个未杂化的2p轨道形成π键 |
| B、sp3杂化轨道是由能量相近1个s轨道和3个p轨道混合形成的四个sp3杂化轨道 |
| C、凡中心原子采取sp2杂化的分子,其分子构型都是平面三角形 |
| D、氨气分子中有一对未参与杂化的孤对电子 |
考点:共价键的形成及共价键的主要类型,原子轨道杂化方式及杂化类型判断
专题:化学键与晶体结构
分析:A.乙炔分子为CH≡CH,C原子为sp杂化,为直线结构,未参加杂化的2p轨道形成π键;
B.sp3杂化轨道由1个s和3个p轨道杂化成相同的四个轨道;
C.中心原子采取sp2杂化的分子,不存在孤对电子时为平面结构;
D.N原子最外层5个电子,只形成3个N-H键.
B.sp3杂化轨道由1个s和3个p轨道杂化成相同的四个轨道;
C.中心原子采取sp2杂化的分子,不存在孤对电子时为平面结构;
D.N原子最外层5个电子,只形成3个N-H键.
解答:
解:A.乙炔分子的结构式H-C≡C-H,中心原子碳原子价层电子对个数=σ键个数+孤电子对个数=2+
×(4-2×2)=2,采取sp杂化,每个碳原子都有两个未杂化的2p轨道形成π键,故A正确;
B.sp3杂化轨道是指同一电子层内,1个s轨道和3个p轨道杂化,形成能量相等的四个sp3杂化轨道,故B错误;
C.中心原子采取sp2杂化的分子,n=3,sp2杂化,不含孤电子对其分子构型都是平面三角形,否则不是,如二氧化硫分子中,价层电子对数=2+
(6-2×2)=3,所以采取sp2杂化,含有一对孤电子对,所以立体构型为V型,故C错误;
D.氨气分子中,N原子最外层5个电子,只形成3个N-H键,存在1对孤对电子,N原子为sp3杂化,且孤对电子参与杂化,故D错误;
故选AB.
| 1 |
| 2 |
B.sp3杂化轨道是指同一电子层内,1个s轨道和3个p轨道杂化,形成能量相等的四个sp3杂化轨道,故B错误;
C.中心原子采取sp2杂化的分子,n=3,sp2杂化,不含孤电子对其分子构型都是平面三角形,否则不是,如二氧化硫分子中,价层电子对数=2+
| 1 |
| 2 |
D.氨气分子中,N原子最外层5个电子,只形成3个N-H键,存在1对孤对电子,N原子为sp3杂化,且孤对电子参与杂化,故D错误;
故选AB.
点评:本题考查了杂化轨道、分子空间结构等,题目难度中等,注意把握杂化轨道理论的应用,注意判断中心原子的价层电子对以及孤对电子数的判断.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
已知丁基共有4种,不必试写,立即可推断分子C5H10O2的羧酸(R-COOH)的同分异构体的数目是( )
| A、3种 | B、4种 | C、5种 | D、6种 |
下列关于化学反应进行的方向说法正确的是( )
| A、放热反应都能自发进行,吸热反应都不能自发进行 |
| B、自发反应的熵一定增大,非自发反应的熵一定减小 |
| C、能自发进行的反应一定能实际发生 |
| D、常温下,反应C(s)+CO2(g)═2CO(g)不能自发进行,则该反应的△H>0 |
25℃将相同物质的量浓度的CH3COOH和NaOH溶液混合,欲使混合液的pH=7,则CH3COOH溶液的体积V1和NaOH溶液的体积V2的关系是( )
| A、V1=V2 |
| B、V1>V2 |
| C、V1<V2 |
| D、V1≥V2 |
可逆反应2SO2(g)+O2(g)?2SO3(g),在不同条件下测得化学反应速率最快的为( )
| A、v(O2)=3 mol?L-1?min-1 |
| B、v (SO2)=4 mol?L-1?min-1 |
| C、v (SO3)=0.1 mol?L-1?s-1 |
| D、v (O2)=0.1 mol?L-1?s-1 |
下列有关化学用语表达正确的是( )
A、次氯酸的电子式: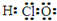 |
B、CCl4分子的球棍模型: |
| C、乙醛结构简式:CH3CHO |
D、H2O2的电子式: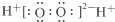 |
设NA为阿伏加德罗常数,下列说法不正确的是( )
| A、标准状况下,22.4 L O2含有的分子数为NA |
| B、常温常压下,3.4 g H2O2含有极性键的数目为0.2 NA |
| C、将含Na+数目为NA的NaCl固体溶于1 L水中,所得溶液的浓度为1 mol?L-1 |
| D、标准状况下,2.24 L Cl2与足量NaOH溶液反应,转移电子的数目为0.1 NA |
元素周期表中铋元素的数据见图,下列说法正确的是( )


| A、Bi元素的质量数是209.0 |
| B、Bi元素中子数为83 |
| C、Bi原子6p亚层有有一个未成对电子 |
| D、Bi位于第六周期VA族,属于p区 |