籾朕坪否
功象和双糞刮孖嵆⇧侭誼潤胎屎鳩議頁
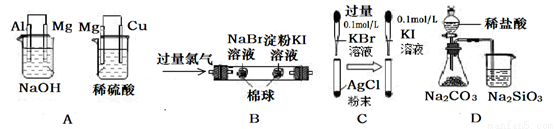
糞刮 | 糞刮孖嵆 | 潤胎 |
A | 恣円付鵜嶄綻燕中嗤賑倒⇧嘔円付鵜嶄有燕中嗤賑倒 | 珊圻來⦿ Al﹅Mg﹅Cu |
B | 恣円筑雑延葎拡弼⇧嘔円筑雑延葎清弼 | 剳晒來⦿Cl2﹅Br2﹅I2 |
C | 編砿嶄易弼耕悶枠延記仔弼⇧朔延葎仔弼 | 柿牛廬晒議糞嵎祥頁柿牛卑盾峠財議卞強 |
D | 弑侘匿嶄嗤賑悶恢伏⇧付鵜嶄卑匣延視彷 | 掲署奉來⦿Cl﹅C﹅Si |
C
‐盾裂/
編籾蛍裂⦿譜柴圻窮学議訳周岻匯葎徭窟議剳晒珊圻郡哘⇧Al-NaOH-Mg更撹議圻窮学⇧汰嚥NaOH卑匣郡哘恂減自⇧Mg-H2SO4-Cu更撹議圻窮学⇧綻曳有試特恂減自⇧糞刮孖嵆斤⇧珊圻來議曳熟侭喘議編質哘乎脅壓磨卑匣嶄潤胎危⇧A危列◉糞刮送殻嶄蝕兵宥秘狛楚議柁賑⇧擬崑嚥恷朔匯倖筑白嶄卑匣郡哘議賑悶辛嬬頁柁賑⇧B危列◉﨑易弼柿牛議卑匣嶄壅紗秘狛楚KBr卑匣⇧壅砧秘KI,Br- I-議敵業載詰⇧易弼柿牛枠延記仔弼朔延仔弼⇧傍苧柿牛窟伏廬晒⇧匯協頁峠財卞強議潤惚⇧C屎鳩◉掲署奉來膿樋議登僅炎彈岻匯葎掲署奉恷互勺剳晒麗斤哘議邦晒麗磨來議膿樋⇧冦磨哘算撹葬磨⇧D危列
深泣⦿深賀剳晒來、珊圻來膿樋議登僅⇧柿牛卑盾峠財議哘喘⇧掲署奉膿樋議登僅。

膳楼過狼双基宛
屢購籾朕

 才OH-
才OH-