题目内容
根据下列流程回答:
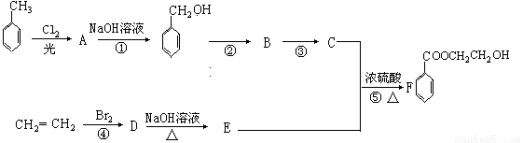
(1)写出C、E中含氧官能团的名称分别为: 、 。
(2)写出结构简式 A E
(3)在①~⑤反应中,属于取代反应的是 (填编号)。
(4)写出有关⑤的化学方程式:
(1)羧基,羟基;(2)C6H5CH2Cl HOCH2CH2OH;(3)① ⑤
(4)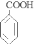 + HOCH2CH2OH
+ HOCH2CH2OH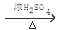
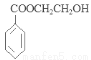 +H2O
+H2O
【解析】
试题分析: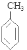 与Cl2在光照时发生取代反应得到A:
与Cl2在光照时发生取代反应得到A: 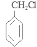 ;A在NaOH的水溶液中发生取代反应得到
;A在NaOH的水溶液中发生取代反应得到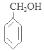 苯甲醇催化氧化得到B苯甲醛
苯甲醇催化氧化得到B苯甲醛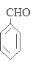 ;苯甲醛再催化氧化得到C苯甲酸
;苯甲醛再催化氧化得到C苯甲酸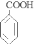 ;CH2=CH2与Br2发生加成反应得到D:1,2-二溴乙烷CH2BrCH2Br;1,2-二溴乙烷CH2BrCH2Br 与NaOH的水溶液混合加热发生取代反应得到E:乙二醇
;CH2=CH2与Br2发生加成反应得到D:1,2-二溴乙烷CH2BrCH2Br;1,2-二溴乙烷CH2BrCH2Br 与NaOH的水溶液混合加热发生取代反应得到E:乙二醇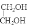 ;乙二醇与本甲酸发生酯化反应
;乙二醇与本甲酸发生酯化反应 (1)C苯甲酸
(1)C苯甲酸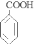 含氧官能团的名称为羧基;E乙二醇
含氧官能团的名称为羧基;E乙二醇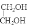 含氧官能团的名称为羟基。(2)A结构简式为
含氧官能团的名称为羟基。(2)A结构简式为 或C6H5CH2Cl;E结构简式为
或C6H5CH2Cl;E结构简式为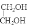 或HOCH2CH2OH。(3)在①~⑤反应中,①是取代反应。②是氧化反应;③是氧化反应;④是加成反应;⑤属于取代反应。因此属于取代反应的是①⑤。(4)有关⑤的化学方程式为
或HOCH2CH2OH。(3)在①~⑤反应中,①是取代反应。②是氧化反应;③是氧化反应;④是加成反应;⑤属于取代反应。因此属于取代反应的是①⑤。(4)有关⑤的化学方程式为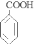 + HOCH2CH2OH
+ HOCH2CH2OH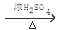
 +H2O。
+H2O。
考点:考查有机合成与推断、物质的结构简式、化学方程式的书写、反应类型的判断的知识。

(15分)
(1)人们常用催化剂来选择反应进行的方向。下图所示为一定条件下1mol CH3OH与O2发生反应时,生成CO、CO2或HCHO的能量变化图[反应物O2(g)和生成物H2O(g)略去]。
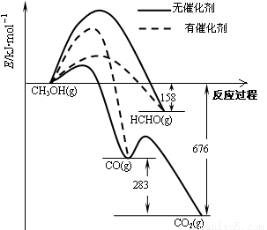
①在有催化剂作用下,CH3OH与O2反应主要生成 (填“CO、CO2” 或“HCHO”)。2HCHO(g)+O2(g)=2CO(g)+2H2O(g) △H= 。
②甲醇制取甲醛可用Ag作催化剂,含有AgCl会 影响Ag催化剂的活性。用氨水可以溶解除去其中的AgCl,写出该反应的离子方程式: 。
(2)已知:CO(g)+ 2H2(g)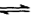 CH3OH(g)△H = -a kJ?mol-1。
CH3OH(g)△H = -a kJ?mol-1。
①经测定不同温度下该反应的平衡常数如下:
温度(℃) | 250 | 300 | 350 |
K | 2.041 | 0.270 | 0.012 |
若某时刻、250℃测得该反应的反应物与生成物的浓度为c(CO)=0.4 mol·L-1、c(H2)=0.4 mol·L-1、c(CH3OH)=0.8 mol·L-1, 则此时v正 v逆(填“>”、“<”或“=”)。
②某温度下,在体积固定的2L的密闭容器中将1 mol CO和2 mol H2混合,测得不同时刻的反应前后压强关系如下:
时间(min) | 5 | 10 | 15 | 20 | 25 | 30 |
压强比(P后/P前) | 0.98 | 0.90 | 0.80 | 0.70 | 0.70 | 0.70 |
则0~15 min,用H2表示的平均反应速率为 ,达到平衡时CO的转化率为 。
(3)利用钠碱循环法可除去SO2,消除SO2对环境的污染。吸收液吸收SO2的过程中,pH随n(SO3?-)∶n(HSO3-)变化关系如下表:
n(SO3?-) ∶n(HSO3-) | 91∶9 | 1∶1 | 1∶91 |
pH | 8.2 | 7.2 | 6.2 |
根据上表判断NaHSO3溶液显 性。
② 在NaHSO3溶液中离子浓度关系正确的是 (填字母)。
a. c(Na+)> c(HSO3-)> c(H+)> c(SO32-)> c(OH-)
b. c(Na+)= 2c(SO32-)+ c(HSO3-)
c. c(H2SO3)+ c(H+)= c(SO32-)+ (OH-)
d. c( Na+)+ c(H+)= c(SO32-)+ c(HSO3-)+ c(OH-)
根据下列实验现象,所得结论正确的是
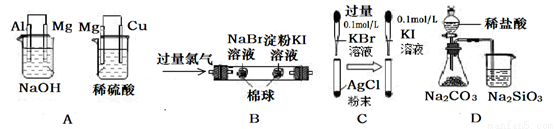
实验 | 实验现象 | 结论 |
A | 左边烧杯中镁表面有气泡,右边烧杯中铜表面有气泡 | 还原性: Al>Mg>Cu |
B | 左边棉花变为橙色,右边棉花变为蓝色 | 氧化性:Cl2>Br2>I2 |
C | 试管中白色固体先变淡黄色,后变为黄色 | 沉淀转化的实质就是沉淀溶解平衡的移动 |
D | 锥形瓶中有气体产生,烧杯中溶液变浑浊 | 非金属性:Cl>C>Si |
 H++CH3COO-,下列叙述不正确的是( )
H++CH3COO-,下列叙述不正确的是( )