题目内容
(16分)FeBr2是一种黄绿色鳞片状的固体,某研究性学习小组为了探究它的还原性,进行了如下实验:
I.实验需要90mL 0.1mol/LFeBr2溶液
(1) 配制FeBr2溶液除烧杯、量筒、胶头滴管外还需的玻璃仪器是________
(2)下列有关配制过程中说法错误的是________(填序号)。
a.用托盘天平称量质量为1.944g的FeBr2
b.将称量的FeBr2放入容量瓶中,加90mL蒸馏水溶解
c.洗涤溶解FeBr2的烧杯,并将洗涤液转移至容量瓶中
d.容量瓶贴签存放配好的FeBr2溶液
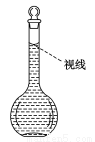
e.定容时,仰视容量瓶刻度线会使配制的FeBr2溶液浓度偏高
II. 探究FeBr2的还原性
取10mL上述FeBr2溶液,向其中滴加少量新制的氯水,振荡后溶液呈黄色。某同学对产生黄色的原因提出了假设:
假设1:Br-被Cl2氧化成Br2溶解在溶液中;
假设2:Fe2+被Cl2氧化成Fe3+。

Ⅰ⑴玻璃棒、100mL容量瓶 ⑵abde
Ⅱ⑴
|
|
①振荡、静置,CCl4层呈橙红色 | 假设1正确 |
②KSCN溶液,溶液变为红色 | 假设2正确 |
萃取和分液
⑵2Fe2++Br2 = 2Fe3++2Br- ⑶2Fe2++2Br-+2Cl2=2Fe3++ Br2+4Cl-
【解析】
试题分析:Ⅰ⑴用FeBr2固体配制FeBr2溶液需要烧杯、量筒、胶头滴管、玻璃棒、100mL容量瓶;
⑵a项用托盘天平不能称量质量为1.944g的FeBr2,错误;
b项将称量的FeBr2放入容量瓶中,加90mL蒸馏水溶解不能刚好达到刻度线,错误;
c项洗涤溶解FeBr2的烧杯,并将洗涤液转移至容量瓶中,减少溶质的损失,正确;
d 项容量瓶不能贴签存放配好的FeBr2溶液 ,错误;
e项定容时,仰视容量瓶刻度线会多加蒸馏水,使配制的FeBr2溶液浓度偏低,错误。
Ⅱ⑴为了证明假设1(Br-被Cl2氧化成Br2溶解在溶液中)正确,可向所得黄色溶液中加入CCl4萃取,CCl4层呈橙红色;为了证明假设2(Fe2+被Cl2氧化成Fe3+)正确,可向所得黄色溶液中加入KSCN溶液,溶液变为红色。若假设1正确,从实验①中分离出Br2的实验操作为萃取和分液。
⑵可通过离子反应“2Fe2++Br2 = 2Fe3++2Br-”证明还原性Fe2+>Br-;
⑶根据还原性Fe2+>Br-,通过计算说明Fe2+全部被氧化,而Br-只有一半被氧化,其发生的离子反应可表示为2Fe2++2Br-+2Cl2=2Fe3++ Br2+4Cl-。
考点:考查化学探究实验。

 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案根据下列实验现象,所得结论正确的是
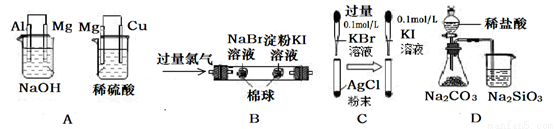
实验 | 实验现象 | 结论 |
A | 左边烧杯中镁表面有气泡,右边烧杯中铜表面有气泡 | 还原性: Al>Mg>Cu |
B | 左边棉花变为橙色,右边棉花变为蓝色 | 氧化性:Cl2>Br2>I2 |
C | 试管中白色固体先变淡黄色,后变为黄色 | 沉淀转化的实质就是沉淀溶解平衡的移动 |
D | 锥形瓶中有气体产生,烧杯中溶液变浑浊 | 非金属性:Cl>C>Si |
 NH4++OH-
NH4++OH- Cu2++2Cl-
Cu2++2Cl-