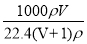题目内容
(14分)固态化合物A由两种短周期元素组成,可与水发生复分解反应,甲组同学用如图装置(夹持装置略)对其进行探究实验。
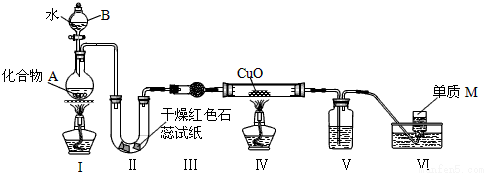
(1)仪器B的名称是____________。
(2)试验中,Ⅱ中的试纸变蓝,Ⅳ中黑色粉末逐渐变为红色并有M生成,则Ⅲ中的试剂为__________________;Ⅳ发生反应的化学方程式为____________;Ⅴ中的试剂为____________________。
(3)乙组同学进行同样实验,但装置连接顺序为Ⅰ——Ⅲ——Ⅳ——Ⅱ——Ⅴ——Ⅵ,此时Ⅱ中现象为________,原因是__________________。
(4)经上述反应,2.5g 化合物A理论上可得0.56L(标准状况)M;则A的化学式为________________。
26、(14分)
(1)分液漏斗(1分)
(2)碱石灰(2分) CuO+2NH3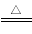 3Cu+3H2O+N2↑(2分) 浓硫酸(1分)
3Cu+3H2O+N2↑(2分) 浓硫酸(1分)
(3)试纸变蓝(2分) CuO与氨气反应生成的水和未反应的氨气形成氨水,使试纸变蓝(3分)
(4)Mg3N2(3分)
【解析】
试题分析:(1)注意观察仪器特征(分液漏斗和长颈漏斗的区别)仪器B的名称是分液漏斗;(2)中学阶段,能使红色石蕊试纸变蓝的只有氨气一种气体,所以整个实验流程Ⅰ是制备氨气,Ⅱ是检验氨气,Ⅳ是氨气与CuO反应,那么Ⅲ必须干燥氨气,Ⅴ是除去未反应的氨气,Ⅵ是收集氮气,所以Ⅲ中的试剂为碱石灰;Ⅳ发生反应的化学方程式为CuO+2NH3 3Cu+3H2O+N2↑;Ⅴ中的试剂为浓硫酸(3)装置连接顺序为Ⅰ生成氨气—Ⅲ干燥氨气—Ⅳ是氨气与CuO反应生成水—Ⅱ湿润的氨气与干燥红色石蕊试纸反应,所以此时Ⅱ中现象为试纸变蓝,原因是CuO与氨气反应生成的水和未反应的氨气形成氨水,使试纸变蓝。(4)氨气与氧化铜反应生成氮气,所以A中含有N;另一个只能是短周期的金属与N组成的化合物,这样的化合物可以与水反应产生NH3,并且生成金属的氢氧化物,满足短周期的金属有Li、Na、Mg、Al。那么与N组合有:Li3N、Na3N、Mg3N2和AlN。写出方程式计算,满足题意的只有Mg2N3,即A为Mg2N3
3Cu+3H2O+N2↑;Ⅴ中的试剂为浓硫酸(3)装置连接顺序为Ⅰ生成氨气—Ⅲ干燥氨气—Ⅳ是氨气与CuO反应生成水—Ⅱ湿润的氨气与干燥红色石蕊试纸反应,所以此时Ⅱ中现象为试纸变蓝,原因是CuO与氨气反应生成的水和未反应的氨气形成氨水,使试纸变蓝。(4)氨气与氧化铜反应生成氮气,所以A中含有N;另一个只能是短周期的金属与N组成的化合物,这样的化合物可以与水反应产生NH3,并且生成金属的氢氧化物,满足短周期的金属有Li、Na、Mg、Al。那么与N组合有:Li3N、Na3N、Mg3N2和AlN。写出方程式计算,满足题意的只有Mg2N3,即A为Mg2N3
考点:考察常见仪器、常用试剂,氨气的化学性质等知识。

Ⅰ (本题4分)赤铜矿的成分是Cu2O,辉铜矿的成分是Cu2S,将赤铜矿与辉铜矿混合物加热有以下反应发生:2Cu2O+Cu2S 6Cu+SO2↑; 填写下列空白:
6Cu+SO2↑; 填写下列空白:
①在该反应中,氧化剂是 。还原剂是 。
②氧化产物与还原产物的质量比是 。
Ⅱ(本题7分)A、B、C、D、E为易溶化合物,其离子组成为
阳离子 | Fe3+、Ba2+、Al3+、Na+、Ag+ |
阴离子 | NO3—、OH—、SO42—、Cl—、CO32— |
在各化合物中离子不重复,分别取其溶液进行实验,结果如下:
①在A溶液中逐滴加入氨水,有白色沉淀生成,继续加氨水至过量,沉淀消失;
②用pH试纸测得B和C溶液显碱性,0.1mol/L的C溶液pH小于13;
③在D溶液中加入铁粉,溶液质量增加且无气体产生;
④在E溶液中加入过量B,没有沉淀产生。
完成下列填空:
(1)A的化学式为 ; (2)③反应的离子方程式为 ;
(3)检验D溶液中阴离子的的方法是 ;
(4)E的的化学式为 ,将E蒸干、灼热至质量不再改变,最后所得物质是(填化学式) 。
根据下列实验现象,所得结论正确的是
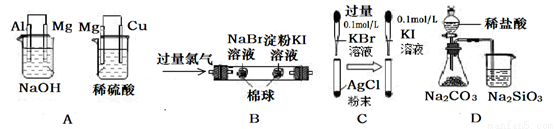
实验 | 实验现象 | 结论 |
A | 左边烧杯中镁表面有气泡,右边烧杯中铜表面有气泡 | 还原性: Al>Mg>Cu |
B | 左边棉花变为橙色,右边棉花变为蓝色 | 氧化性:Cl2>Br2>I2 |
C | 试管中白色固体先变淡黄色,后变为黄色 | 沉淀转化的实质就是沉淀溶解平衡的移动 |
D | 锥形瓶中有气体产生,烧杯中溶液变浑浊 | 非金属性:Cl>C>Si |
 B.
B.
 D.
D.
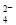 +4H+
+4H+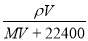 B.
B. 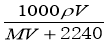 C.
C.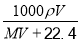 D.
D.