题目内容
 影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究.他们利用他们利用Cu、Fe、Mg和不同浓度的硫酸(0.5mol/L、2mol/L、18.4mol/L),设计实验方案来研究影响反应速率的因素.
影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究.他们利用他们利用Cu、Fe、Mg和不同浓度的硫酸(0.5mol/L、2mol/L、18.4mol/L),设计实验方案来研究影响反应速率的因素.甲同学研究的实验报告如表:
| 实 验 步 骤 | 现 象 | 结 论 |
| ①分别取等体积的2mol/L硫酸于试管中; ②分别投入大小、形状相同的Cu、Fe、Mg. | 反应快慢: Mg>Fe>Cu | 反应物的性质越活泼,反应速率越快. |
(2)乙同学为了更精确地研究浓度对反应速率的影响,利用如图装置进行定量实验.完成该实验应选用的实验药品是
(3)在使用铁与稀硫酸反应制氢气时,实验室里选择粗铁比纯铁效果更好,原因是:
考点:探究影响化学反应速率的因素
专题:实验设计题
分析:(1)根据表中数据可知,硫酸的浓度相同,不同金属的规格相同,说明实验目的是探究反应物本身对反应速率的影响;影响反应速率的还有温度,所以应该使反应温度相同;
(2)金属和酸反应生成氢气,根据v=
确定测定量;
(3)根据粗铁含有碳,与稀硫酸反应时构成原电池加快反应速率来解释.
(2)金属和酸反应生成氢气,根据v=
| △V |
| △t |
(3)根据粗铁含有碳,与稀硫酸反应时构成原电池加快反应速率来解释.
解答:
解:(1)根据表中的信息得出该同学的实验目的是研究反应物本身的性质对反应速率的关系对反应速率的影响;温度对化学反应速率的影响较大,故根据控制变量法,要得出正确的实验结论,还需控制的实验条件是保持温度相同,
故答案为:探究反应物本身的性质对反应速率的影响;温度相同;
(2)乙同学为了更精确地研究浓度对反应速率的影响,利用如图1装置进行定量实验,图1中药品是金属和酸,浓硫酸和铁发生钝化现象而影响判断,所以完成该实验应选用的实验药品是Mg(或Fe)和 0.5mol/L、2mol/L的硫酸,根据v=
知应该测定的实验数据是测定一定时间产生气体的体积或测定产生一定体积的气体所需时间,
故答案为:Mg(或Fe)和 0.5mol/L、2mol/L的硫酸;测定一定时间产生气体的体积或测定产生一定体积的气体所需时间;
(3)因为粗铁含有碳,与稀硫酸反应时构成原电池加快反应速率,比纯铁反应速率快,故答案:粗铁含有碳,与稀硫酸反应时构成原电池加快反应速率.
故答案为:探究反应物本身的性质对反应速率的影响;温度相同;
(2)乙同学为了更精确地研究浓度对反应速率的影响,利用如图1装置进行定量实验,图1中药品是金属和酸,浓硫酸和铁发生钝化现象而影响判断,所以完成该实验应选用的实验药品是Mg(或Fe)和 0.5mol/L、2mol/L的硫酸,根据v=
| △V |
| △t |
故答案为:Mg(或Fe)和 0.5mol/L、2mol/L的硫酸;测定一定时间产生气体的体积或测定产生一定体积的气体所需时间;
(3)因为粗铁含有碳,与稀硫酸反应时构成原电池加快反应速率,比纯铁反应速率快,故答案:粗铁含有碳,与稀硫酸反应时构成原电池加快反应速率.
点评:本题考查了探究影响化学反应速率的因素,注意做对比实验时只能改变一个条件,其它条件必须相同,否则无法得出正确结论.

练习册系列答案
相关题目
对于某些离子的检验及结论一定正确的是( )
| A、焰色反应为黄色,则该物质一定为钠的化合物 |
| B、加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+ |
| C、加入稀盐酸酸化的氯化钡溶液有白色沉淀产生,则一定含有SO42- |
| D、加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+ |
将一定质量的铁、氧化铁、氧化铜的混合物粉末放入100mL4.40mol/L盐酸中,充分反应后产生896mLH2(标准状况),残留固体1.28g.过滤,滤液中无Cu2+,将滤液加水稀释到200mL,测得其中c(H+)为0.40mol/L.则原混合物中氧化铁的质量是( )
| A、2.4g | B、3.6g |
| C、5.6g | D、6.4g |
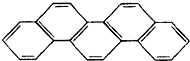 有一种有机物,因其酷似奥林匹克旗中的五环(如图),科学家称其为奥林匹克烃,下列有关奥林匹克烃的说法正确的是( )
有一种有机物,因其酷似奥林匹克旗中的五环(如图),科学家称其为奥林匹克烃,下列有关奥林匹克烃的说法正确的是( )| A、该烃属于烯烃 |
| B、该烃分子中只含非极性键 |
| C、该烃的二氯代物只有一种 |
| D、该烃完全燃烧生成H2O的物质的量小于CO2的物质的量 |
 某学生利用以下装置探究氯气与氨气之间的反应.其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置.请回答下列问题:
某学生利用以下装置探究氯气与氨气之间的反应.其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置.请回答下列问题:
 某学习小组制作如图所示简易量热计测定中和反应的反应热,烧杯中,并用温度计测量盐酸的温度;用另一个量筒量取50mL筒中的NaOH溶液一次倒入小烧杯,盖好插有温度计和环形搅拌棒的盖板,匀速搅拌,记录溶液到达的最高温度.
某学习小组制作如图所示简易量热计测定中和反应的反应热,烧杯中,并用温度计测量盐酸的温度;用另一个量筒量取50mL筒中的NaOH溶液一次倒入小烧杯,盖好插有温度计和环形搅拌棒的盖板,匀速搅拌,记录溶液到达的最高温度.