题目内容
20.用下面的方案进行某些离子的检验,其中方案设计严密的是( )| A. | 检验试液中的SO42-:试液$\stackrel{足量稀硝酸}{→}$无沉淀$\stackrel{BaCl_{2}溶液}{→}$白色沉淀 | |
| B. | 检验试液中的SO32-:试液$\stackrel{浓盐酸}{→}$气体$\stackrel{品红}{→}$褪色 | |
| C. | 检验试液中的I-:试液$\stackrel{H_{2}O_{2}}{→}$棕黄色溶液$\stackrel{浓粉溶液}{→}$蓝色溶液 | |
| D. | 检验试液中的CO32-:试液$\stackrel{足量BaCl_{2}溶液}{→}$白色沉淀$\stackrel{足量稀盐酸}{→}$沉淀溶解 |
分析 A.硝酸可氧化亚硫酸根离子;
B.亚硫酸氢根离子与盐酸反应也生成二氧化硫;
C.淀粉遇碘变蓝,可知棕黄色溶液中含碘;
D.白色沉淀可能为亚硫酸钡.
解答 解:A.硝酸可氧化亚硫酸根离子,则不能确定一定硫酸根离子,不严密,故A不选;
B.亚硫酸氢根离子与盐酸反应也生成二氧化硫,不一定含亚硫酸根离子,故B不选;
C.淀粉遇碘变蓝,可知棕黄色溶液中含碘,则可知试液中含I-,故C选;
D.白色沉淀可能为亚硫酸钡,不能确定是否含碳酸根离子,可能CO32-、SO32-二者均有,故D不选;
故选C.
点评 本题考查常见离子的检验,为高考常见题型,侧重于学生的分析、实验能力的考查,把握离子检验的试剂、现象为解答的关键,注意检验时排除干扰离子,题目难度不大.

练习册系列答案
相关题目
10.下列说法不正确的是( )
| A. | 近年来禽流感病毒H7N9时有病例报告,卫生部门强调要尽量避免接触活禽,个人也应加强消毒预防,其中消毒剂可以选用含氯消毒剂、酒精、双氧水等适宜的物质 | |
| B. | 将浸泡过高锰酸钾溶液的硅藻土放入新鲜的水果箱内是为了催熟水果 | |
| C. | “埃博拉”病毒在常温下较稳定,对热有中等度抵抗力,56℃不能完全灭活,60℃30min方能破坏其感染性,此过程主要发生了蛋白质的变性 | |
| D. | 用二氧化碳制全降解塑料,可以缓解温室效应 |
11.根据“金刚石?石墨+1.896kJ”,可以得出的正确结论是( )
| A. | 石墨的能量比金刚石低 | B. | 石墨和金刚石都是碳的同位素 | ||
| C. | 金刚石转化为石墨是物理变化 | D. | 金刚石比石墨更稳定 |
8.用如图所示的装置进行实验,反应一段时间后断开K,向烧杯中加入0.1mol CuO后CuSO4溶液恰好恢复到反应前的浓度和pH.下列说法中不正确的是( )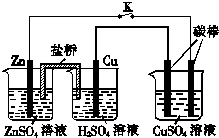

| A. | 铜棒为正极,其电极反应式为2H++2e-=H2↑ | |
| B. | 烧杯右侧碳棒为阴极,其电极表面有红色物质析出 | |
| C. | 反应中消耗锌的质量为6.5 g | |
| D. | 导线中通过电子的物质的量为0.1 mol |
15.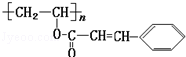 某种“光敏性高分子”材料在荧光屏及大规模集成电路中应用广泛.其结构可表示为:对该“光敏性高分子”叙述正确的是( )【-COO-基团与氢气不反应】
某种“光敏性高分子”材料在荧光屏及大规模集成电路中应用广泛.其结构可表示为:对该“光敏性高分子”叙述正确的是( )【-COO-基团与氢气不反应】
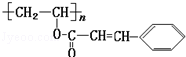 某种“光敏性高分子”材料在荧光屏及大规模集成电路中应用广泛.其结构可表示为:对该“光敏性高分子”叙述正确的是( )【-COO-基团与氢气不反应】
某种“光敏性高分子”材料在荧光屏及大规模集成电路中应用广泛.其结构可表示为:对该“光敏性高分子”叙述正确的是( )【-COO-基团与氢气不反应】| A. | 化学式为(C11H11O2)n | |
| B. | 它能发生还原反应 | |
| C. | 它可以和FeCl3溶液发生显色反应 | |
| D. | 1mol该分子最多能和4molH2发生加成反应 |
5.元素X的原子,其M层与K层电子数相同;元素Y的原子,其M层上有7个电子.X和Y所形成的稳定化合物的相对分子质量为( )
| A. | 100 | B. | 95 | C. | 88 | D. | 80 |
12.优质的锂碘电池可用于心脏起搏器延续患者的生命,它的正极材料是聚2一乙烯吡啶(简写P2VP)和I2 的复合物,电解质是固态薄膜状的碘化锂,电池的总反应为2Li+P2VP•nI2═P2VP•(n-1)I2+2LiI,则下列说法正确的是( )
| A. | 聚2一乙烯吡啶的复合物与有机物性质相似,因此聚2一乙烯吡啶的复合物不会导电 | |
| B. | 正极的反应为P2VP•nI2+2Li++2e-═P2VP•(n-1)I2+2LiI | |
| C. | 电池工作时,碘离子移向P2VP一极 | |
| D. | 该电池所产生的电压低,使用寿命比较短 |
9.下表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式填空回答以下问题:
(1)在这些元素中,金属性最强的元素是K,最活泼的非金属元素是F;化学性质最不活泼的元素是Ar.
(2)元素的最高价氧化物对应的水化物中酸性最强的是HClO4,碱性最强的是KOH,呈两性的氢氧化物是Al(OH)3
(3)在③~⑦元素中,原子半径最大的是Na;
(4)在⑦与⑩的单质中,化学性质较活泼的是Cl2,可用什么化学反应说明(写出反应的化学方程式):2NaBr+Cl2=2NaCl+Br2.与⑩元素同主族下一周期元素的一种化合物是食用盐中必须加入的,此化合物的化学式KIO3.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅤⅡA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
(2)元素的最高价氧化物对应的水化物中酸性最强的是HClO4,碱性最强的是KOH,呈两性的氢氧化物是Al(OH)3
(3)在③~⑦元素中,原子半径最大的是Na;
(4)在⑦与⑩的单质中,化学性质较活泼的是Cl2,可用什么化学反应说明(写出反应的化学方程式):2NaBr+Cl2=2NaCl+Br2.与⑩元素同主族下一周期元素的一种化合物是食用盐中必须加入的,此化合物的化学式KIO3.
10.砹(At)是卤素中核电荷数最大的元素,推测砹或砹的化合物性质的叙述中正确的是( )
| A. | 砹为有色固体 | |
| B. | HAt 很稳定 | |
| C. | AgAt易溶于水 | |
| D. | 砹单质的熔沸点比碘单质的熔沸点低 |