题目内容
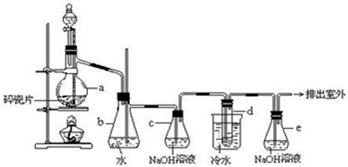
14. 正丁醛是一种重要的化工原料.肥西中学高二某化学兴趣小组在老师的指导下利用如图装置合成正丁醛.发生的反应如下:
正丁醛是一种重要的化工原料.肥西中学高二某化学兴趣小组在老师的指导下利用如图装置合成正丁醛.发生的反应如下:CH3CH2CH2CH2OH$\underset{\stackrel{N{a}_{2}C{r}_{2}{O}_{7}}{→}}{{H}_{2}S{O}_{4}加热}$CH3CH2CH2CHO
反应物和产物的相关数据列表如下:
| 沸点/.c | 密度/(g•cm-3) | 水中溶解性 | |
| 正丁醇 | 117.2 | 0.8109 | 微溶 |
| 正丁醛 | 75.7 | 0.8017 | 微溶 |
将6.0gNa2Cr2O7放入100mL烧杯中,加30mL水溶解,再缓慢加入5mL浓硫酸,将所得溶液小心转移至B中.在A中加入4.0g正丁醇和几粒沸石,加热.当有蒸汽出现时,开始滴加B中溶液.滴加过程中保持反应温度为90-95℃,在E中收集90℃以下的馏分.将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75-77℃馏分,产量2.0g.
回答下列问题:
(1)实验中,能否将Na2Cr2O7溶液加到浓硫酸中,简述理由不能,浓硫酸溶于水放出大量热,容易发生迸溅伤人.
(2)上述装置图中,D仪器的名称是直形冷凝管,E仪器的名称是锥形瓶.
(3)C1、C2温度计水银球位置不同的原因是C1控制反应温度;C2测定蒸馏出来气体的温度
(4)反应温度应保持在90-95℃,其原因是保证正丁醛及时蒸出,促使反应正向进行,又可尽量避免其被进一步氧化.
(5)正丁醇的同分异构体有许多种,请写出符合下列条件的正丁醇的同分异构体:①含有与正丁醇相同的官能团;②一定条件下能被氧化成醛.(CH3)2CHCH2OH
(6)本实验中正丁醛的产率为51%.
分析 (1)不能将Na2Cr2O7溶液加到浓硫酸中,因为浓硫酸的密度大,容易发生迸溅;
(2)根据装置图可知仪器的名称,D为冷凝器,E为接受馏分的锥形瓶;
(3)C1控制反应混合溶液的温度,C2处的温度计是控制馏出成分的沸点;
(4)根据题目所给反应物和产物的沸点数据可知,反应温度保持在90~95℃,既可保证正丁醛及时蒸出,又可尽量避免其被进一步氧化;
(5)根据条件 ①含有与正丁醇相同的官能团,即有醇羟基,②一定条件下能被氧化成醛,说明羟基连在CH2上,据此写出符合条件的正丁醇的同分异构体;
(6)设正丁醛的理论产量为xg,根据关系式C4H10O~C4H8O列计算出理论产量,根据产率=$\frac{实际产量}{理论产量}$×100%计算.
解答 解:(1)因为浓硫酸的密度大,能将Na2Cr2O7溶液加到浓硫酸中,容易发生迸溅伤人,
故答案为:不能,浓硫酸溶于水放出大量热,容易发生迸溅伤人;
(2)D仪器的名称直形冷凝管,E仪器为锥形瓶;
故答案为:分直形冷凝管;锥形瓶;
(3)温度计的作用是,C1控制反应混合溶液的温度,C2处的温度计是控制馏出成分的沸点,测定蒸馏出来气体的温度,
故答案为:C1控制反应温度;C2测定蒸馏出来气体的温度;
(4)根据题目所给反应物和产物的沸点数据可知,反应温度保持在90~95℃,既可保证正丁醛及时蒸出,又可尽量避免其被进一步氧化,
故答案为:保证正丁醛及时蒸出,促使反应正向进行,又可尽量避免其被进一步氧化;
(5)根据条件 ①含有与正丁醇相同的官能团,即有醇羟基,②一定条件下能被氧化成醛,说明羟基连在CH2上,则符合条件的正丁醇的同分异构体为(CH3)2CHCH2OH,
故答案为:(CH3)2CHCH2OH;
(6)设正丁醛的产率为x,则正丁醇的利用率为x,根据关系式,
C4H10O~C4H8O
74 72
4xg 2g
解得:x=$\frac{74×2}{72×4}$×100%=51%,
故答案为:51%.
点评 本题考查有机化学实验、反应原理、基本操作、化学计算等,难度中等,注意计算中正丁醇的转化率等于正丁醛的产率,注意对基础知识的理解掌握.

 实验室制取溴乙烷的主反应如下:
实验室制取溴乙烷的主反应如下:NaBr+H2SO4→HBr+NaHSO4
C2H5OH+HBr?C2H5Br+H2O
副反应:在该实验中经常会有乙醚、溴等副产物生成,装置如图所示.
| 相对分子质量 | 密度/(g•cm-3) | 沸点/℃ | 溶解度 | |
| 乙 醇 | 46 | 0.789 | 78.3 | 易溶 |
| 溴乙烷 | 109 | 1.46 | 38.2 | 难溶 |
| 浓硫酸 | 98 | 1.84 | 338.0 | 易溶 |
①向A中先加入5mL 95%的无水乙醇(0.085mol)和4.5mL的水,加入溴化钠7.725g,再加入沸石,摇匀.在接受器F中加冷水及3ml饱和亚硫酸氢钠溶液,并将其放入冰水浴中.
②在B中加入9.5mL浓硫酸(0.17mol),向A中缓缓滴入浓硫酸,加热体系,控制反应温度,保持反应平稳地发生,直至无油状物馏出为止;
③分出馏出液中的有机层,加入1-2mL浓硫酸以除去乙醚、乙醇、水等杂质,溶液明显分层后,分离得到粗产物;
④将粗产物转入蒸馏瓶中,加入沸石,在水浴上加热蒸馏,收集35-40℃的馏分,称量得5.23g.
回答问题:
(1)仪器E的名称为冷凝管;反应装置中有使用C、D两根温度计,其中D温度计的作用是:D温度计用来测反应体系的温度
(2)步骤①在接受器F中加冷水以及将F放入冰水浴中的目的是溴乙烷沸点低、极易挥发,冰水主要可以防止溴乙烷的挥发.饱和亚硫酸氢钠溶液的作用是除去反应中的副产物溴;
(3)步骤②中浓硫酸要缓缓滴加而不一次加入,其作用有abd(填标号).
a.可以防止乙醇发生碳化 b.避免生成HBr的速度过快,减少其挥发
c.避免溶液发生暴沸 d.减少因浓硫酸氧化HBr而生成副产物溴;
(4)步骤③中分出馏出液中有机层的操作名称为分液.加入浓硫酸除杂后的溶液明显分层,粗产物在上层(填“上”或“下”);
(5)本实验的产率为64%.
有关物质的性质:
| 名称 | 相对分子质量 | 沸点/(℃) | 密度/(g/mL) |
| 苯 | 78 | 78 | 0.88 |
| 氯苯 | 112.5 | 132.2 | 1.1 |
| 邻二氯苯 | 147 | 180.4 | 1.3 |
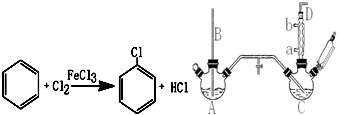
(1)A反应器是利用实验室法制取氯气,反应原理为(写化学反应方程式):MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,装置中中空导管B的作用是平衡气压
(2)把干燥的氯气通入装有干燥苯的反应器C中制备氯苯,C的反应温度不宜过高,原因为①温度过高,反应得到二氯苯;②温度过高,苯挥发,原料利用率不高,D出口的主要尾气成分有Cl2、苯蒸气、HCl.
(3)提纯粗产品过程如下:

①净化过程中加入NaCl晶体的目的是吸水干燥,系列操作为过滤、蒸馏
②为了确定所得产品为氯苯,而非二氯苯,可对产品进行分析,下列方法可行的是AB
A、质谱法 B、红外光谱法 C、滴定法
(4)实验中最终得到产品14.7mL,产率为23.0%,产率不高的原因可能是:温度过高,反应生成二氯苯
(5)苯气相氧氯化氢法制氯苯:空气、氯化氢气混合物温度210℃,进入氯化反应器,在迪肯型催化剂(CuCl2 FeCl3附在三氧化铝上)存在下进行氯化,反应方程式为:2
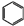 +2HCl+O2$→_{210℃}^{催化剂}$2
+2HCl+O2$→_{210℃}^{催化剂}$2 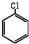 +2 H2O.
+2 H2O. 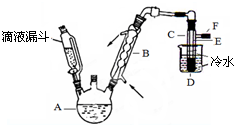 图是实验室用乙醇、硫酸、溴化钠混合反应来制备溴乙烷的装置.反应需要加热,图中省去了加热装置.乙醇、溴乙烷、溴的有关性状参数见表.
图是实验室用乙醇、硫酸、溴化钠混合反应来制备溴乙烷的装置.反应需要加热,图中省去了加热装置.乙醇、溴乙烷、溴的有关性状参数见表.| 乙醇 | 溴乙烷 | 溴 | |
| 状态 | 无色液体 | 无色液体 | 深红棕色液体 |
| 密度/g.cm-3 | 0.79 | 1.44 | 3.1 |
| 沸点/℃ | 78.5 | 38.4 | 59 |
| 水溶性 | 易溶 | 难溶 | 微溶 |
(2)若选用较浓的硫酸作为反应物,得到的产品则会呈棕黄色,这说明反应过程中有Br2生成.为去除颜色,最好选择下列的d溶液来洗涤产品.
a.四氯化碳 b.硫酸钠 c.碘化亚铁 d.亚硫酸钠
产品选择上述溶液洗涤后,还需再用蒸馏水洗涤一次.洗涤液与产品分离的方法是分液(填方法名称).
(3)装置中,B和D两部分的作用分别是:B冷凝回流反应物,冷却产物蒸汽;D冷凝产品.
| A. | 离子的还原性强弱:I->Fe2+>Br- | |
| B. | 当a≥b时,发生的离子反应:2I-+Br2=I2++2Br- | |
| C. | 当3a≤2b时,发生的离子反应:2Fe2++2I-+2Br2=2Fe3++I2+4Br- | |
| D. | 当5a=4b时,反应后的离子浓度之比:c(Fe2+):c(Fe3+):c(Br-)=1:1:5 |
| A. | 摩尔是用来描述微观粒子的物理量 | |
| B. | 1 mol任何物质都含有Na个原子 | |
| C. | 0.5 mol H2O中含有的原子数目为1.5Na | |
| D. | 64g氧相当于2mol氧 |