��Ŀ����
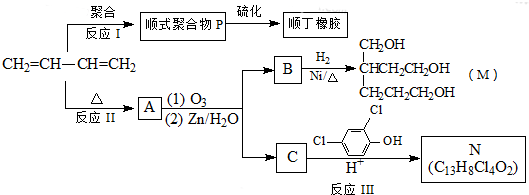
A��һ���л��ϳ��м��壬��ṹΪ��
A�ĺϳ�·����ͼ������B��H�ֱ����һ���л��

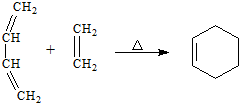
��֪�� R��R�����������
R��R�����������
��ش��������⣺
��1��A��̼ԭ�ӵ��ӻ���������� ��A�����ƣ�ϵͳ�������� ���ڢಽ��Ӧ��������
��
��2���ڢٲ���Ӧ�Ļ�ѧ����ʽ�� ��
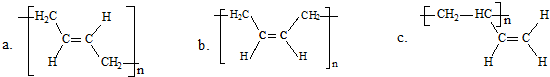
��3��C������CH2=C��CH3��COOH�����ʵ���֮��1��1��Ӧ������ᆳ�Ӿ۵õ����������۾��ľ�Ƭ����I��I�Ľṹ��ʽ�� ��
��4���ڢ���Ӧ�Ļ�ѧ����ʽ�� ��
��5��д��������Ԫ������һ��ȡ����ֻ��2�֣������������칹����A��ͬ���칹��Ľṹ��ʽ�� ��

A�ĺϳ�·����ͼ������B��H�ֱ����һ���л��

��֪��
 R��R�����������
R��R�������������ش��������⣺
��1��A��̼ԭ�ӵ��ӻ����������
��2���ڢٲ���Ӧ�Ļ�ѧ����ʽ��
��3��C������CH2=C��CH3��COOH�����ʵ���֮��1��1��Ӧ������ᆳ�Ӿ۵õ����������۾��ľ�Ƭ����I��I�Ľṹ��ʽ��
��4���ڢ���Ӧ�Ļ�ѧ����ʽ��
��5��д��������Ԫ������һ��ȡ����ֻ��2�֣������������칹����A��ͬ���칹��Ľṹ��ʽ��
���㣺���⼯��,�л�����ƶ�
ר�⣺�л���Ļ�ѧ���ʼ��ƶ�
������BΪC2H5OH��C2H5OH��Ũ�������ᷢ��ȡ����Ӧ����C2H5Br��C2H5Br��þ��Ӧ����C2H5MgBr��C�ܷ���2�δ���������CΪHOCH2CH20H��HOCH2CH20H����2�δ���������D����DΪHOOC-COOH��HOOC-COOH��״�����������Ӧ����E��EΪ ��������֪��Ϣ��֪��
��������֪��Ϣ��֪�� ��C2H5MgBr����ȡ����Ӧ����F��G��FCH3OMgBr��GΪ
��C2H5MgBr����ȡ����Ӧ����F��G��FCH3OMgBr��GΪ ��
�� ����ˮ������H��HΪ
����ˮ������H��HΪ ��
�� ����������/�������������·�����ȥ��Ӧ����A�����˽��з������ó���ȷ���ۣ�
����������/�������������·�����ȥ��Ӧ����A�����˽��з������ó���ȷ���ۣ�
 ��������֪��Ϣ��֪��
��������֪��Ϣ��֪�� ��C2H5MgBr����ȡ����Ӧ����F��G��FCH3OMgBr��GΪ
��C2H5MgBr����ȡ����Ӧ����F��G��FCH3OMgBr��GΪ ��
�� ����ˮ������H��HΪ
����ˮ������H��HΪ ��
�� ����������/�������������·�����ȥ��Ӧ����A�����˽��з������ó���ȷ���ۣ�
����������/�������������·�����ȥ��Ӧ����A�����˽��з������ó���ȷ���ۣ����
�⣺��1��A�м�̼ԭ�Ӻ���4���Ҽ�������Cԭ�ӵ��ӻ��������Ϊsp3��̼̼˫����Cԭ�ӵ��ӻ��������Ϊsp2��A��ϵͳ������Ϊ��3��4-���һ�-2��4-����ϩ���ڢಽ��ӦΪ ����������/�������������·�����ȥ��Ӧ����A��
����������/�������������·�����ȥ��Ӧ����A��
�ʴ�Ϊ��sp2��sp3��3��4-���һ�-2��4-����ϩ����ȥ��Ӧ��
��2���ڢٲ���ӦΪ��C2H5OHŨ�������ᷢ��ȡ����Ӧ����C2H5Br������ʽΪ��C2H5OH+HBr
C2H5Br+H2O��
�ʴ�Ϊ��C2H5OH+HBr
C2H5Br+H2O��
��3��CΪHOCH2CH20H��HOCH2CH20H��CH2=C��CH3��COOH�����ʵ���֮��1��1����������Ӧ����CH2=C��CH3��COOCH2CH20H��CH2=C��CH3��COOCH2CH20H�����Ӿ۷�Ӧ����I��IΪ ��
��
�ʴ�Ϊ�� ��
��
��4���ڢ���ӦΪ�� ��C2H5MgBr����ȡ����Ӧ����F��G��FΪCH3OMgBr��GΪ
��C2H5MgBr����ȡ����Ӧ����F��G��FΪCH3OMgBr��GΪ ������ʽΪ��
������ʽΪ�� ��
��
�ʴ�Ϊ�� ��
��
��5��A��ͬ���칹���к�����Ԫ������һ��ȡ����ֻ��2�ֵĽṹ��ʽΪ ��
��
�ʴ�Ϊ�� ��
��
 ����������/�������������·�����ȥ��Ӧ����A��
����������/�������������·�����ȥ��Ӧ����A���ʴ�Ϊ��sp2��sp3��3��4-���һ�-2��4-����ϩ����ȥ��Ӧ��
��2���ڢٲ���ӦΪ��C2H5OHŨ�������ᷢ��ȡ����Ӧ����C2H5Br������ʽΪ��C2H5OH+HBr
| �� |
�ʴ�Ϊ��C2H5OH+HBr
| �� |
��3��CΪHOCH2CH20H��HOCH2CH20H��CH2=C��CH3��COOH�����ʵ���֮��1��1����������Ӧ����CH2=C��CH3��COOCH2CH20H��CH2=C��CH3��COOCH2CH20H�����Ӿ۷�Ӧ����I��IΪ
 ��
���ʴ�Ϊ��
 ��
����4���ڢ���ӦΪ��
 ��C2H5MgBr����ȡ����Ӧ����F��G��FΪCH3OMgBr��GΪ
��C2H5MgBr����ȡ����Ӧ����F��G��FΪCH3OMgBr��GΪ ������ʽΪ��
������ʽΪ�� ��
���ʴ�Ϊ��
 ��
����5��A��ͬ���칹���к�����Ԫ������һ��ȡ����ֻ��2�ֵĽṹ��ʽΪ
 ��
���ʴ�Ϊ��
 ��
��
���������⿼���л�����ƶϼ���ط���ʽ����д��������Ϣ���ƶ������ǽ��Ĺؼ�����Ŀ�Ѷ��еȣ�

��ϰ��ϵ�д�
�����Ŀ
����˵������ȷ���ǣ�������
| A��C2H4��HCN�����У������Ҽ��ͦм�����Cԭ�ӵ��ӻ���ʽ������ͬ |
| B����Ԫ�����ڱ��У�p��Ԫ�ص����������Ų����ɱ�ʾΪns2np1��6 |
C��ij��̬ԭ�ӵĺ�������Ų�ͼΪ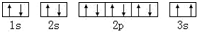 ����Υ��������������ԭ�� ����Υ��������������ԭ�� |
| D���ú�����ɼ����Ҵ��Ͷ����ѣ���X-��������ʵ��ɼ�������ˮ�� |
����˵����ȷ���ǣ�������
| A��CS2ΪV�εļ��Է��� |
| B��������ʾ��ͼ�е�ÿ��С�ڵ㶼��ʾһ������ |
| C���Ǽ��Լ�Ҳ���Դ����ڻ������� |
| D�����顢����ˮ�����ɼ��Լ���϶��ɵļ��Է��� |
 �����ѣ�CH3OCH3���������������ʣ�����Ϊ21���͵����͡������Դ������δ������������ͺ�Һ������Ϊ�ྻҺ��ȼ��ʹ�ã���ҵ����C0��H2Ϊԭ������CH30CH3���¹�����Ҫ����������Ӧ��
�����ѣ�CH3OCH3���������������ʣ�����Ϊ21���͵����͡������Դ������δ������������ͺ�Һ������Ϊ�ྻҺ��ȼ��ʹ�ã���ҵ����C0��H2Ϊԭ������CH30CH3���¹�����Ҫ����������Ӧ�� ʵ��������480mL 0.1mol?L-1NaOH��Һ���ش���������
ʵ��������480mL 0.1mol?L-1NaOH��Һ���ش���������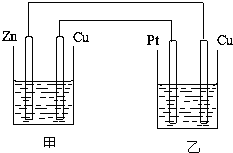 ��ͼ��ʾ��װ�ã���װ���еĵ������ҺΪ����ͭ��Һ������Ϊϡ���ᣬ�밴����Ҫ��ش����⣮
��ͼ��ʾ��װ�ã���װ���еĵ������ҺΪ����ͭ��Һ������Ϊϡ���ᣬ�밴����Ҫ��ش����⣮