题目内容
11.用98%(密度为1.84g/cm3)的浓硫酸稀释成3mol/L的稀硫酸100mL,需要取浓硫酸16.3mL.分析 密度为1.84g/cm3,质量分数为98%的浓硫酸的物质的量浓度为:c(H2SO4)=$\frac{1000ρω}{M}$=$\frac{1000×1.84g/L×98%}{98g/mol}$=18.4mol/L,稀释过程中硫酸的物质的量不变进行计算需要3mol/L硫酸溶液的体积,以此解答该题.
解答 解:c(H2SO4)=$\frac{1000ρω}{M}$=$\frac{1000×1.84g/L×98%}{98g/mol}$=18.4mol/L,溶液稀释前后溶质的物质的量不变,设需要VmL浓硫酸,
则18.4mol/L×V×10-3L/mL=3mol/L×100mL×10-3L/mL,
V=16.3mL.
故答案为:16.3.
点评 本题考查了物质的量浓度计算,题目难度中等,注意物质的量浓度与溶液密度、质量分数的关系,该题是高考中的常见考点和题型,试题基础性强,侧重对学生基础知识的巩固和训练,旨在考查学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
相关题目
1.化学与生产、生活密切相关,下列说法正确的是( )
| A. | 利用粮食酿酒经历了淀粉→葡萄糖→乙醇的化学变化过程 | |
| B. | 淀粉、油脂和蛋白质都是高分子化合物 | |
| C. | 煤经过气化和液化等物理变化可转化为清洁燃料 | |
| D. | 聚氯乙烯塑料薄膜可用作食品保鲜膜、一次性食品袋等 |
2.下列各溶液中能大量共存的离子组是( )
| A. | 澄清透明的溶液中:Fe2+、Mg2+、SO42-、Cl- | |
| B. | 使酚酞试液呈红色的溶液中:Al3+、Cu2+、SO42-、K+ | |
| C. | 使石蕊试液变红的溶液中:Na+、Cl-、K+、HCO3- | |
| D. | 碳酸钠溶液中:Ba2+、NO3-、Cl-、H+ |
19.现有Fe、Al、Si三种单质的混合物,取一半投入足量的NaOH溶液中,将剩余的一半投入足量的稀硫酸中,若经测量两次实验产生的气体质量相等,则原混合物中Fe、Al、Si三种单质的物质的量之比可能为( )
| A. | 6:4:3 | B. | 1:1:1 | C. | 2:3:4 | D. | 3:7:6 |
6.某反应由两步反应A→B→C构成,反应能量曲线如图,下列叙述正确的是( )


| A. | 两步反应均为吸热反应 | B. | 三种化合物中C最稳定 | ||
| C. | A与C的能量差为E4 | D. | A→B反应,反应条件一定要加热 |
16.下列仪器名称为“蒸馏烧瓶”的是( )
| A. | 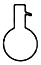 | B. |  | C. |  | D. | 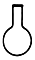 |
4.下列关于气体摩尔体积的叙述中正确的是( )
| A. | 1mol二氧化碳在标准状况时所占的体积约是22.4L | |
| B. | 氧气在标准状况下頕有体积约为22.4L | |
| C. | 1mol任何物质在0℃,1.01×105Pa时体积都约是22.4L | |
| D. | 1mol任何气体的体积都约是22.4L |
5.下列名称与化学式表示同一物质的是( )
| A. | 明矾FeSO4•7H2O | B. | 石膏Na2SO4•10H2O | ||
| C. | 重晶石Na2CO3•10H2O | D. | 胆矾CuSO4•5H2O |