��Ŀ����
�����̿���Ҫ�ɷ�MnO2������������Ҫ�ɷ�FeS2��Ϊԭ����ȡ�ߴ���MnO2������߿����Դ�ĸ���ֵ����������������£�
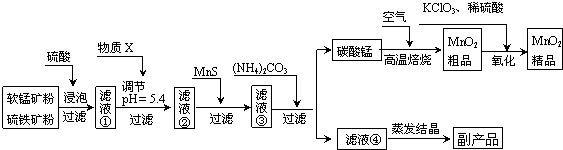
�ش��������⣺
��1��MnO2�����������¾���ǿ�����ԣ������Խ�FeS2����������������ԭ��Mn2+����Ӧ���������ʻ�����
������������������Ӧ�в��������ɵ���
A��Fe3+ B��H2S ����C��SO42- ��D��S
�����д�ʩ������߷�Ӧ���ʵ���
A��ʹ��۸��顡��B����߽����¶� C���ʵ��������Ũ�ȡ���D���ı����̿����������ı���
��2����������X������Һ�ٵ�pH=5.4�Գ�ȥFe3+���ӣ�����X���˲��õ���
A��MnCO3 �� B��Na2CO3 ��C����ˮ
��3����Һ���к�������Zn2+������MnS�ɳ�ȥ����Ӧ����ʽΪ��MnS+Zn2+=ZnS+Mn2+����Ӧ��ȫ����Һ���е�Mn2+��Zn2+���ӵ�Ũ�ȱ��� ������֪Ksp��MnS��=2.0��10-10��Ksp��ZnS��=4.0��10-22��
��4������Ʒ�Ļ�ѧʽ��
��5����֪��2MnO��s��+O2��g��=2MnO2��s����H1=a kJ?mol-1��MnCO3��s��=MnO��s��+CO2��g����H2=b kJ?mol-1��д������̼���̵��Ȼ�ѧ����ʽ��
��6�����±��պ����в���MnCO3����ת��ΪMnO2�����������ϡ�����KClO3��Һ����������������Ӧ���£�MnCO3+ClO3-+H+--MnO2+Cl2��+CO2��+H2O��δ��ƽ�����÷�Ӧ��MnCO3��ClO3-�����ʵ���֮��Ϊ ��

�ش��������⣺
��1��MnO2�����������¾���ǿ�����ԣ������Խ�FeS2����������������ԭ��Mn2+����Ӧ���������ʻ�����
������������������Ӧ�в��������ɵ���
A��Fe3+ B��H2S ����C��SO42- ��D��S
�����д�ʩ������߷�Ӧ���ʵ���
A��ʹ��۸��顡��B����߽����¶� C���ʵ��������Ũ�ȡ���D���ı����̿����������ı���
��2����������X������Һ�ٵ�pH=5.4�Գ�ȥFe3+���ӣ�����X���˲��õ���
A��MnCO3 �� B��Na2CO3 ��C����ˮ
��3����Һ���к�������Zn2+������MnS�ɳ�ȥ����Ӧ����ʽΪ��MnS+Zn2+=ZnS+Mn2+����Ӧ��ȫ����Һ���е�Mn2+��Zn2+���ӵ�Ũ�ȱ���
��4������Ʒ�Ļ�ѧʽ��
��5����֪��2MnO��s��+O2��g��=2MnO2��s����H1=a kJ?mol-1��MnCO3��s��=MnO��s��+CO2��g����H2=b kJ?mol-1��д������̼���̵��Ȼ�ѧ����ʽ��
��6�����±��պ����в���MnCO3����ת��ΪMnO2�����������ϡ�����KClO3��Һ����������������Ӧ���£�MnCO3+ClO3-+H+--MnO2+Cl2��+CO2��+H2O��δ��ƽ�����÷�Ӧ��MnCO3��ClO3-�����ʵ���֮��Ϊ
���㣺���ʷ�����ᴿ�ķ����ͻ��������ۺ�Ӧ��,������ԭ��Ӧ�ļ���,��ѧ��Ӧ���ʵ�Ӱ������,���ܵ���ʵ��ܽ�ƽ�⼰����ת���ı���
ר�⣺ʵ�������,�����������������
��������1����MnO2�����������¾���ǿ�����ԣ�����Һ�еĻ�ԭ�����ʲ��������ɣ�
�������¶ȣ�����Ũ�ȣ�ʹ��۸�������Ӧ�Ӵ���������ܼӿ췴Ӧ���ʣ��ı�������ʵ��������ܸı䷴Ӧ���ʣ�
��2����ȥFe3+����ʱ���������µ��������ӣ�
��3������Һ�������ӵ�Ũ����ͬ������Ksp��MnS��=2.0��10-10�����c��Mn2+��������Ksp��ZnS��=4.0��10-22�����c��Zn2+��=������ɽ⣻
��4������Һ���м��루NH4��2CO3����̼���̳������������Һ���������Һ���������ᾧ�õ���NH4��2SO4���壻
��5�����ݸ�˹����д������̼���̵��Ȼ�ѧ����ʽ��
��6��MnCO3������ϡ�����KClO3��Һ��Ӧ����MnO2��Cl2����ƽ����ʽΪ5MnCO3+2ClO3-+2H+=5MnO2+Cl2��+5CO2��+H2O����֪��Ӧ��MnCO3��ClO3-�����ʵ���֮��Ϊ5��2��
�������¶ȣ�����Ũ�ȣ�ʹ��۸�������Ӧ�Ӵ���������ܼӿ췴Ӧ���ʣ��ı�������ʵ��������ܸı䷴Ӧ���ʣ�
��2����ȥFe3+����ʱ���������µ��������ӣ�
��3������Һ�������ӵ�Ũ����ͬ������Ksp��MnS��=2.0��10-10�����c��Mn2+��������Ksp��ZnS��=4.0��10-22�����c��Zn2+��=������ɽ⣻
��4������Һ���м��루NH4��2CO3����̼���̳������������Һ���������Һ���������ᾧ�õ���NH4��2SO4���壻
��5�����ݸ�˹����д������̼���̵��Ȼ�ѧ����ʽ��
��6��MnCO3������ϡ�����KClO3��Һ��Ӧ����MnO2��Cl2����ƽ����ʽΪ5MnCO3+2ClO3-+2H+=5MnO2+Cl2��+5CO2��+H2O����֪��Ӧ��MnCO3��ClO3-�����ʵ���֮��Ϊ5��2��
���
��1����MnO2�����������¾���ǿ�����ԣ�����Һ�еĻ�ԭ�����ʲ��������ɣ�Fe3+��SO42- �����л�ԭ�ԣ��������ɣ�S������ˮ����һ�ֳ������������ɣ�H2S���л�ԭ�ԣ��ܱ����������������ɣ��ʴ�Ϊ��B��
�������¶ȣ�����Ũ�ȣ�ʹ��۸�������Ӧ�Ӵ���������ܼӿ췴Ӧ���ʣ��ı�������ʵ��������ܸı䷴Ӧ���ʣ��ʸı����̿����������ı������ܼӿ췴Ӧ���ʣ��ʴ�Ϊ��D��
��2����ȥFe3+����ʱ���������µ��������ӣ�����Na2CO3����PHֵ���ں��������в���Na+�ѳ�ȥ���ʴ�Ϊ��B��
��3������Һ�������ӵ�Ũ����ͬ������Ksp��MnS��=2.0��10-10֪c��Mn2+��=
������Ksp��ZnS��=4.0��10-22֪c��Zn2+��=
������Mn2+��Zn2+���ӵ�Ũ�ȱ�Ϊ
=5.0��1011���ʴ�Ϊ��5.0��1011��
��4������Һ���м��루NH4��2CO3����̼���̳������������Һ���������ˣ���ҺΪ�������Һ���������Һ�����ᾧ�õ���NH4��2SO4���壻
�ʴ�Ϊ����NH4��2SO4��
��5����֪2MnO��s��+O2��g��=2MnO2��s����H1=a kJ?mol-1 ��
MnCO3��s��=MnO��s��+CO2��g����H2=b kJ?mol-1�� ��
��+�ڡ�2��2MnCO3��s��+O2��g��=2MnO2��s��+2CO2��g����H=��H1+��H2��2�T��a+2b��kJ?mol-1��
�ʴ�Ϊ��2MnCO3��s��+O2��g��=2MnO2��s��+2CO2��g����H=��a+2b��kJ?mol-1��
��6��MnCO3������ϡ�����KClO3��Һ��Ӧ����MnO2��Cl2��MnԪ����+2�����ߵ�+4�ۣ�ClԪ����+5�۽��͵�0�ۣ����ݻ��ϼ��������֪MnCO3��ClO3-�ļ������ֱ�Ϊ5��2������ԭ���غ�͵���غ���ƽ����ʽΪ5MnCO3+2ClO3-+2H+=5MnO2+Cl2��+5CO2��+H2O���ʸ÷�Ӧ��MnCO3��ClO3-�����ʵ���֮��Ϊ5��2��
�ʴ�Ϊ��5��2��
�������¶ȣ�����Ũ�ȣ�ʹ��۸�������Ӧ�Ӵ���������ܼӿ췴Ӧ���ʣ��ı�������ʵ��������ܸı䷴Ӧ���ʣ��ʸı����̿����������ı������ܼӿ췴Ӧ���ʣ��ʴ�Ϊ��D��
��2����ȥFe3+����ʱ���������µ��������ӣ�����Na2CO3����PHֵ���ں��������в���Na+�ѳ�ȥ���ʴ�Ϊ��B��
��3������Һ�������ӵ�Ũ����ͬ������Ksp��MnS��=2.0��10-10֪c��Mn2+��=
| 2.0��10-10 |
| c(S2-) |
| 4.0��10-22 |
| c(S2-) |
| ||
|
��4������Һ���м��루NH4��2CO3����̼���̳������������Һ���������ˣ���ҺΪ�������Һ���������Һ�����ᾧ�õ���NH4��2SO4���壻
�ʴ�Ϊ����NH4��2SO4��
��5����֪2MnO��s��+O2��g��=2MnO2��s����H1=a kJ?mol-1 ��
MnCO3��s��=MnO��s��+CO2��g����H2=b kJ?mol-1�� ��
��+�ڡ�2��2MnCO3��s��+O2��g��=2MnO2��s��+2CO2��g����H=��H1+��H2��2�T��a+2b��kJ?mol-1��
�ʴ�Ϊ��2MnCO3��s��+O2��g��=2MnO2��s��+2CO2��g����H=��a+2b��kJ?mol-1��
��6��MnCO3������ϡ�����KClO3��Һ��Ӧ����MnO2��Cl2��MnԪ����+2�����ߵ�+4�ۣ�ClԪ����+5�۽��͵�0�ۣ����ݻ��ϼ��������֪MnCO3��ClO3-�ļ������ֱ�Ϊ5��2������ԭ���غ�͵���غ���ƽ����ʽΪ5MnCO3+2ClO3-+2H+=5MnO2+Cl2��+5CO2��+H2O���ʸ÷�Ӧ��MnCO3��ClO3-�����ʵ���֮��Ϊ5��2��
�ʴ�Ϊ��5��2��
����������ѧ����Ԫ�ؼ��仯�������Ҫ���ʵ����ա��Ȼ�ѧ����ʽ����д���Ķ���Ŀ��ȡ����Ϣ�������Թ������̵�����ȣ��Ѷ��еȣ���Ҫѧ���߱���ʵ�Ļ������ۺ�����֪ʶ����Ϣ�����������������

��ϰ��ϵ�д�
�����Ŀ
�ڳ����£����Ȼ�����������������ˮ���γɵ�Ũ�ȵ������������壬����������ȷ���ǣ�������
| A�������Ȼ�����������������δ������ѧ�仯 |
| B��FeCl3��Һ��Fe��OH��3�����з�ɢ�ʿ�����ֱ����ͬ |
| C�������ö����ЧӦʵ����Ч�������Ȼ�����Һ�������������� |
| D�����Ȼ�����������ˮ�� |
��NA��ʾ����٤������������˵����ȷ���ǣ�������
| A��32g O2����������Ϊ2NA |
| B��28g N2����������Ϊ2NA |
| C��NA��CO���Ӻ�0.5mol CH4������֮��Ϊ7��4 |
| D��14g N2���7NA������ |
��NA��ʾ�����ӵ�������ֵ������˵����ȷ���ǣ�������
| A��78g Na2O2��������������Ϊ4NA |
| B�������£�2L��1 mol?L-1��������Һ�У�������������С��2NA |
| C����״���£�5.6L NO��5.6 L O2��ɵĻ������������ԭ����ΪNA |
| D�����ڷ�Ӧ��C2H2��g��+5/2O2��g��=2CO2��g��+H2O��l����H=-1300 kJ/mol����2NA��̼��˫���γ�ʱ���ų�1300 kJ������ |

 X��Y��Z��W����ͼ��ʾ��ת����ϵ����֪��H=��H1+��H2����X��Y������
X��Y��Z��W����ͼ��ʾ��ת����ϵ����֪��H=��H1+��H2����X��Y������