题目内容
下列反应的离子方程式中,正确的是( )
| A、稀硫酸滴在银片上:2Ag+2H+=2Ag++H2↑ |
| B、氧化铁与稀盐酸混合:Fe2O3+6H+=2Fe3++3H2O |
| C、碳酸钙溶于醋酸溶液中:CaCO3+2H+=Ca2++CO2↑+H2O |
| D、饱和石灰水跟稀硝酸反应:Ca(OH)2+2H+=Ca2++2H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.银活泼性较差,金属银无法与稀硫酸反应生成氢气;
B.氧化铁为碱性氧化物,能够与稀盐酸反应生成氯化铁和水;
C.醋酸为弱电解质,离子方程式中不能拆开;
D.氢氧化钙应该写成离子形式,不需要保留化学式.
B.氧化铁为碱性氧化物,能够与稀盐酸反应生成氯化铁和水;
C.醋酸为弱电解质,离子方程式中不能拆开;
D.氢氧化钙应该写成离子形式,不需要保留化学式.
解答:
解:A.银与稀硫酸不发生反应,无法写出反应的离子方程式,故A错误;
B.氧化铁与稀盐酸混合,反应生成铁离子和水,反应的离子方程式为:Fe2O3+6H+=2Fe3++3H2O,故B正确;
C.碳酸钙为难溶物,需要保留化学式,正确的离子方程式为:CaCO3+2CH3COOH=Ca2++H2O+CO2↑+2CH3COO-,故C错误;
D.饱和石灰水跟稀硝酸反应,氢氧化钙应该写成离子形式,正确的离子方程式为:OH-+H+=H2O,故D错误;
故选B.
B.氧化铁与稀盐酸混合,反应生成铁离子和水,反应的离子方程式为:Fe2O3+6H+=2Fe3++3H2O,故B正确;
C.碳酸钙为难溶物,需要保留化学式,正确的离子方程式为:CaCO3+2CH3COOH=Ca2++H2O+CO2↑+2CH3COO-,故C错误;
D.饱和石灰水跟稀硝酸反应,氢氧化钙应该写成离子形式,正确的离子方程式为:OH-+H+=H2O,故D错误;
故选B.
点评:本题考查了离子方程式的正误判断,该题是高考中的高频题,属于中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法,如:检查反应能否发生,检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等).

练习册系列答案
相关题目
下列各实验,不可能成功的是( )
①蒸馏普通酒精制无水乙醇;
②苯与浓硫酸混合加热至60℃制硝基苯;
③用苯和溴水混合制溴苯;
④用裂化汽油从碘水中提取碘.
①蒸馏普通酒精制无水乙醇;
②苯与浓硫酸混合加热至60℃制硝基苯;
③用苯和溴水混合制溴苯;
④用裂化汽油从碘水中提取碘.
| A、只有①和④ | B、只有②和③ |
| C、只有①和③ | D、①②③④ |
短周期元素X、Y、Z、W、Q在元素周期表的位置如表所示,其中X元素原子的内层电子数是最外层电子数的一半,则下列说法正确的是( )
| X | Y | ||
| Z | W | Q |
| A、W的一种核素质量数是A,则其中子数是A-16 |
| B、由Z与Y组成的物质在熔融时能导电 |
| C、W得电子能力比Q强 |
| D、X有多种同素异形体,而Y不存在同素异形体 |
设NA为阿伏加德罗常数的数值,下列说法中正确的是( )
| A、含1mol Fe(OH)3的胶体中的胶体粒子数目为NA |
| B、1mol氯气与足量的氢氧化钠反应电子转移总数为2NA |
| C、常温下,23g NO2和N2O4的混合气体中含有NA个氧原子 |
| D、11.2L CO2与8.5g NH3所含的分子数相等 |
用NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A、标准状况下,1mol CO2和CO的混合气中含有的氧原子数为1.5NA |
| B、常温常压下,11.2L氯化氢气体中含有的分子数为0.5NA |
| C、12g Mg与足量二氧化碳反应转移的电子数为NA |
| D、1mol?L-1 CuCl2溶液中含有的氯离子数为2NA |


 它可通过不同化学反应分别制得B、C、D和E四种物质.
它可通过不同化学反应分别制得B、C、D和E四种物质.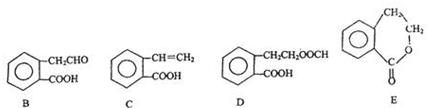
 、HCOOH、CH3COOC2H5
、HCOOH、CH3COOC2H5