题目内容
11.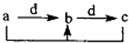 如表各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )
如表各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )物质 选项 | a | b | c | d |
| A | Al | Al(OH)3 | NaAlO2 | NaOH |
| B | N2 | NO | NO2 | O2 |
| C | Na2CO3 | NaHCO3 | NaOH | CO2 |
| D | Cl2 | FeCl3 | FeCl2 | Fe |
| A. | A | B. | B | C. | C | D. | D |
分析 A.Al和NaOH生成NaAlO2而不是Al(OH)3;
B.N2和O2反应生成一氧化氮,一氧化氮与氧气反应生成二氧化氮,但氮气与二氧化氮不反应;
C.NaHCO3与CO2不反应;
C.Cl2和Fe反应生成FeCl3,FeCl3与Fe反应生成FeCl2,Cl2与FeCl2反应生成FeCl3.
解答 解:A.Al和NaOH生成NaAlO2而不是Al(OH)3,如a为AlCl3可符合,故A错误;
B.N2和O2反应生成一氧化氮,一氧化氮与氧气反应生成二氧化氮,但氮气与二氧化氮不反应,故B错误;
C.NaHCO3与CO2不反应,故C错误;
D.Cl2和Fe反应生成FeCl3,FeCl3与Fe反应生成FeCl2,Cl2与FeCl2反应生成FeCl3,符合转化关系,故D正确.
故选D.
点评 本题考查无机物的推断,题目侧重于元素化合物的考查,注意把握相关物质的性质,题目难度不大.

练习册系列答案
 智慧小复习系列答案
智慧小复习系列答案
相关题目
2.既能发生皂化反应,又能发生氢化反应的是( )
| A. | 硬脂酸甘油酯 | B. | 油酸甘油酯 | C. | 软脂酸甘油酯 | D. | 乙酸乙酯 |
6.下列各组微粒半径(r)之比大于1的是( )
| A. | rF:rCl | B. | rI-:rI | C. | rMg2+:rNa+ | D. | rNa+:rNa |
16.化石燃料是最重要的能源之一.下列关于化石燃料的说法错误的是( )
| A. | 石油的分馏产物主要成分是碳氢化合物 | |
| B. | 工业上可通过石油的裂解获得大量乙烯 | |
| C. | 重油经过裂化可以得到汽油 | |
| D. | 煤中含有苯、甲苯,可用分馏的方法将它们分离 |
3.关于乙醇结构方面的说法中正确的是( )
| A. | 乙醇结构中有-OH,所以乙醇溶解于水,可以电离出OH-而显碱性 | |
| B. | 乙醇与乙酸反应生成乙酸乙酯,所以乙醇显碱性 | |
| C. | 乙醇与钠反应可以产生氢气,所以乙醇显酸性 | |
| D. | 乙醇与钠反应非常平缓,所以乙醇羟基上的氢原子不如水中的氢原子活泼 |
1.用NA表示阿伏加德罗常数的值.下列判断正确的是( )
| A. | 标准状况下,22.4 L苯中含有的分子数目为NA | |
| B. | 25℃、101 kPa时,20 g SO3中含有的原子数目为NA | |
| C. | 1 L 1 mol•L-1 MgCl2溶液中含有的氯离子数目为NA | |
| D. | 16.8 g Fe与足量水蒸气反应,转移的电子数目为0.9NA |
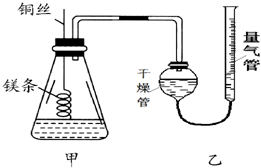 某研究性学习小组欲测定室温下(25℃、101kPa)的气体摩尔体积,请回答以下问题.该小组设计的简易实验装置如图所示:
某研究性学习小组欲测定室温下(25℃、101kPa)的气体摩尔体积,请回答以下问题.该小组设计的简易实验装置如图所示: