题目内容
1.用NA表示阿伏加德罗常数的值.下列判断正确的是( )| A. | 标准状况下,22.4 L苯中含有的分子数目为NA | |
| B. | 25℃、101 kPa时,20 g SO3中含有的原子数目为NA | |
| C. | 1 L 1 mol•L-1 MgCl2溶液中含有的氯离子数目为NA | |
| D. | 16.8 g Fe与足量水蒸气反应,转移的电子数目为0.9NA |
分析 A、标况下苯为液态;
B、求出三氧化硫的物质的量,然后根据1mol三氧化硫中含4mol原子来分析;
C、求出氯化镁的物质的量,然后根据1mol氯化镁中含2mol氯离子来分析;
D、求出铁的物质的量,然后根据铁和水蒸气反应后变为+$\frac{8}{3}$价来分析.
解答 解:A、标况下苯为液态,故不能根据气体摩尔体积来计算其物质的量和含有的分子个数,故A错误;
B、20g三氧化硫的物质的量n=$\frac{20g}{80g/mol}$=0.25mol,而1mol三氧化硫中含4mol原子,故0.25mol三氧化硫中含NA个原子,故B正确;
C、溶液中氯化镁的物质的量n=CV=1mol/L×1L=1mol,而1mol氯化镁中含2mol氯离子,故含2NA个,故C错误;
D、16.8g铁的物质的量n=$\frac{16.8g}{56g/mol}$=0.3mol,而铁和水蒸气反应后变为+$\frac{8}{3}$价,故0.3mol铁转移0.8NA个电子,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
11.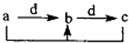 如表各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )
如表各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )
 如表各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )
如表各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )物质 选项 | a | b | c | d |
| A | Al | Al(OH)3 | NaAlO2 | NaOH |
| B | N2 | NO | NO2 | O2 |
| C | Na2CO3 | NaHCO3 | NaOH | CO2 |
| D | Cl2 | FeCl3 | FeCl2 | Fe |
| A. | A | B. | B | C. | C | D. | D |
6.短周期主族元素A、B、C、D,原子序数依次增大.A.C的原子序数的差为8,A、B、C三种元素原子的最外层电子数之和为15,B原子最外层电子数等于A原子最外层电子数的一半.下列叙述正确的是( )
| A. | 原子半径:A<B<C<D | |
| B. | 非金属性:A>C | |
| C. | B和D最高价氧化物对应水化物相互不反应 | |
| D. | 单质B常温下能溶于浓硝酸 |
13.下列各组元素性质递变情况错误的是( )
| A. | Li、Be、B原子最外层电子数依次增多 | |
| B. | N、O、F元素最高正化合价依次升高 | |
| C. | P、S、Cl原子半径依次增大 | |
| D. | Na、K、Rb的第一电离能依次减小 |
11.检验牙膏中是否含有甘油选用的试剂是( )
| A. | 氢氧化钠溶液 | B. | 新制氢氧化铜浊液 | ||
| C. | 醋酸溶液 | D. | 碳酸钠溶液 |
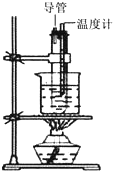 用苯和浓硝酸、浓硫酸按照如图装置制取硝基苯,回答下列问题:
用苯和浓硝酸、浓硫酸按照如图装置制取硝基苯,回答下列问题: ;反应类型:取代反应.
;反应类型:取代反应. ,Na2O2的电子式
,Na2O2的电子式
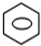 +HNO3(浓)$→_{△}^{浓硫酸}$
+HNO3(浓)$→_{△}^{浓硫酸}$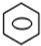 -NO2+H2O
-NO2+H2O ;
;