题目内容
10.CaCO3与稀盐酸反应(放热反应)生成CO2的量与反应时间的关系如图所示,下列结论不正确的是( )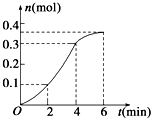
| A. | 反应开始2 min内平均反应速率最大 | |
| B. | 反应速率先增大后减小 | |
| C. | 反应2 min到第4 min内温度对反应速率的影响比浓度大 | |
| D. | 反应在第2 min到第4 min内生成CO2的平均反应速率为前2 min的2倍 |
分析 根据$\frac{△n}{△t}$知,相同时间内二氧化碳物质的量变化量越大其反应速率越大;该反应的正反应是放热反应,反应过程中溶液温度升高、溶液浓度降低,反应物浓度越大、溶液温度越高,反应速率越大,据此分析解答.
解答 解:A.由$\frac{△n}{△t}$知,相同时间内二氧化碳物质的量变化量越大其反应速率越大,根据图知,相同时间内物质的量变化量最大的是2-4min内,所以2-4min内平均反应速率最大,故A错误;
B.由$\frac{△n}{△t}$知,相同时间内二氧化碳物质的量变化量越大其反应速率越大,根据图知,相同时间内物质的量变化大小顺序是2-4min>0-2min>4-6min,所以反应速率先增大后减小,故B正确;
C.该反应的正反应是放热反应,反应过程中溶液温度升高、溶液浓度降低,反应物浓度越大、溶液温度越高,反应速率越大,随着反应减小溶液浓度减小但溶液温度升高,2-4min内反应速率大于0-2min内,所以说明温度影响反应速率大于浓度变化,故C正确;
D.根据图知,反应在第2 min到第4 min内生成CO2的物质的量变化量大于前2min物质的量变化量,所以平均反应速率为前2 min的2倍,故D正确;
故选A.
点评 本题考查图象分析,侧重考查学生分析判断能力,明确图象中曲线变化趋势及其斜率含义是解本题关键,注意该曲线斜率体现反应速率快慢,题目难度不大.

练习册系列答案
 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案
相关题目
20.下列说法正确的是( )
| A. | 常温下pH为5的盐酸溶液稀释1000倍后,pH等于8 | |
| B. | 碳酸钠溶液中存在:c(Na+)+c(H+)=c(CO32-)+c(OH-)+c(HCO3-) | |
| C. | 浓度均为0.1mo1•L-l的氨水和氯化铵溶液,水电离出的c(H+)前者和后者相同 | |
| D. | 等浓度的CH3COOH与KOH以任意比混合:c(K+)+c(H+)=c(OH-)+c(CH3COO-) |
18.原子序数小于18的某元素X,其原子的电子层数为n,最外层电子数为2n+1,核内质子数为2n2-1.下列有关X的说法中不正确的是( )
| A. | X原子的最外层电子数和核电荷数肯定为奇数 | |
| B. | X可能形成化学式为KXO3的含氧酸钾盐 | |
| C. | X能形成化学式为X(OH)3的碱 | |
| D. | X能与某些金属元素形成离子化合物 |
5.一定条件下,体积为2L的密闭容器中,1mol X和3mol Y进行反应:X(g)+3Y(g)?2Z(g),经12s达到平衡,生成0.6mol Z.下列说法正确的是( )
| A. | 以X浓度变化表示的反应速率为0.3 mol/(L•min) | |
| B. | 12 s后将容器体积扩大为10 L,Z的平衡浓度变为原来的$\frac{1}{5}$ | |
| C. | 若增大X的浓度,则物质Y的转化率减小 | |
| D. | 经12 s达到平衡后,2v(X)=v(Z) |
15.下列物质中所含原子的物质的量最多的是( )
| A. | 4g 氦气 | B. | 1.25mol O2 | ||
| C. | 22.4升 Cl2(标准状况) | D. | 6.02×1023个SO2分子 |
2.下列说法正确的是( )
| A. | H2O的摩尔质量为18g | |
| B. | 1mol O2的质量为32g•mol-1 | |
| C. | 相同质量的O2和O3,所含分子数不同,所含原子数相同 | |
| D. | 相同物质的量的CO2 和CO,所含O原子的个数比为1:1 |

 A,B,C,D,E五种物质可按图所示发生转变(反应条件已略去).
A,B,C,D,E五种物质可按图所示发生转变(反应条件已略去).