题目内容
20.下列说法正确的是( )| A. | 常温下pH为5的盐酸溶液稀释1000倍后,pH等于8 | |
| B. | 碳酸钠溶液中存在:c(Na+)+c(H+)=c(CO32-)+c(OH-)+c(HCO3-) | |
| C. | 浓度均为0.1mo1•L-l的氨水和氯化铵溶液,水电离出的c(H+)前者和后者相同 | |
| D. | 等浓度的CH3COOH与KOH以任意比混合:c(K+)+c(H+)=c(OH-)+c(CH3COO-) |
分析 A.酸溶液稀释后不可能为变成碱溶液,溶液的pH只能接近7;
B.关键碳酸钠溶液中的电荷守恒分析;
C.氨水为碱性溶液,溶液中氢氧根离子抑制了水的电离;铵根离子促进了水的电离;
D.根据混合液中的电荷守恒分析.
解答 解:A.常温下pH为5的盐酸溶液稀释1000倍后,溶液仍然为酸性溶液,溶液的pH只能无限接近7,不可能大于7,故A错误;
B.碳酸钠溶液中存在电荷守恒:c(Na+)+c(H+)=2c(CO32-)+c(OH-)+c(HCO3-),故B错误;
C.浓度均为0.1mo1•L-l的氨水和氯化铵溶液,氨水中氢氧根离子抑制了水的电离,而氯化铵溶液中的铵根离子促进了水的电离,则水电离出的c(H+)前者远远小于后者,故C错误;
D.等浓度的CH3COOH与KOH以任意比混合,溶液中一定满足电荷守恒:c(K+)+c(H+)=c(OH-)+c(CH3COO-),故D正确;
故选D.
点评 本题考查了离子浓度大小比较,题目难度中等,明确电荷守恒、盐的水解原理的含义为解答关键,注意熟练掌握电荷守恒、物料守恒及盐的水解在判断离子浓度大小中的应用方法.

练习册系列答案
相关题目
10.把镁带投入盛有盐酸的敞口容器里,在下列因素中:①盐酸的浓度,②镁带的表面积,③溶液的温度,④氯离子的浓度 ⑤滴加硫酸铜溶液.对反应速率有影响的是( )
| A. | ①② | B. | ③④ | C. | ①②③④ | D. | ①②③⑤ |
11.在标准状况下,mg气体A与ng气体B的分子数相同,下列说法中正确的是( )
| A. | 同温同压下,两气体A与B的密度之比为n:m | |
| B. | 同质量的A、B两种气体的分子数之比为m:n | |
| C. | 相同状况下,同体积的气体A和B的质量比为n:m | |
| D. | A与B两种气体的相对分子质量之比为m:n |
8.下列说法正确的是( )
| A. | 常温下,pH=3的盐酸、醋酸分别用水稀释m倍、n倍后pH相同,则m<n | |
| B. | △S>0的反应在一定条件下一定可以自发进行 | |
| C. | 以Al作阳极,Fe作阴极,可以实现铁上镀铝 | |
| D. | 工业合成SO3不采用高压是因为增大压强对SO2的转化率影响不大 |
9.0.1mol Na2SO4 溶液中钠离子的数目是( )
| A. | 6.02×1023 | B. | 2 | C. | 1.204×1023 | D. | 6.02×1022 |
10.CaCO3与稀盐酸反应(放热反应)生成CO2的量与反应时间的关系如图所示,下列结论不正确的是( )
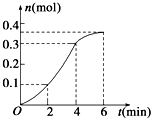

| A. | 反应开始2 min内平均反应速率最大 | |
| B. | 反应速率先增大后减小 | |
| C. | 反应2 min到第4 min内温度对反应速率的影响比浓度大 | |
| D. | 反应在第2 min到第4 min内生成CO2的平均反应速率为前2 min的2倍 |

