题目内容
氮族元素属于 族,氮族元素的最外层电子数为 ,随着核电荷数的递增,原子半径逐渐 ,得电子的能力逐渐 ,非金属性逐渐 ,其气态氢化物的稳定性从上到下逐渐 .
考点:同一主族内元素性质递变规律与原子结构的关系
专题:元素周期律与元素周期表专题
分析:根据氮族元素在周期表中的位置分析;同主族从上到下原子半径逐渐增大,得电子能力减弱,非金属性、氢化物的稳定性均减弱.
解答:
解:氮族元素在周期表中位于第VA主族,最外层电子数为5,同主族从上到下随着核电荷数的递增,原子半径逐渐,得电子能力减弱,非金属性和氢化物的稳定性均减弱;
故答案为:第VA;5;增大;减弱;减弱;减弱.
故答案为:第VA;5;增大;减弱;减弱;减弱.
点评:本题考查了元素周期表和元素周期律,明确同主族元素性质的递变规律即可解答,题目难度不大.

练习册系列答案
相关题目
人们在研究金星大气成分时发现其大气中有一种硫化羟(COS)的分子,其结构与CO2类似,硫化羟是一种与生命密切相关的物质.下列有关COS的推测肯定不正确的是( )
| A、COS的沸点比CO2低 |
| B、COS的结构式为O=C=S |
| C、COS分子中所有原子都满足8电子的稳定结构 |
| D、中心原子C是SP杂化 |
下列叙述合理的是( )
| A、酸雨的形成主要是化石燃料的大量燃烧引起的 |
| B、金属与盐溶液的反应都是置换反应 |
| C、实验室制取NO和NH3都采用排空气法收集 |
| D、标况下,22.4 L SO3的物质的量为1mol |
将等质量的镁铝混合分成四等分,分别加入到足量下列溶液中,充分反应后放出氢气体最多的是( )
| A、3mol?L-1的HCl |
| B、4mol?L-1的HNO3 |
| C、8mol?L-1的NaOH |
| D、18mol?L-1的H2SO4 |
常温下,下列关于电解质溶液的正确判断是( )
| A、pH=11的NaOH溶液中c(H+)是pH=9的Ba(OH)2溶液中c(H+)的100倍 |
| B、使甲基橙变红的溶液中,K+、NO3-、SO32-、HCO3-可以大量共存 |
| C、由0.1 mol?L-1一元酸HA溶液的pH=1,可推知HA溶液存在HA?H++A- |
| D、由0.1 mol?L-1一元碱MOH溶液的pH=10,可推知MCl溶液pH<7 |
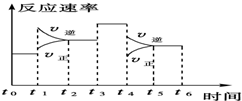 一密封体系中发生下列反应:N2+3H2?2NH3,△H<0,如图是某一时间段中反应速率与反应进程的曲线关系图.回答下列问题:
一密封体系中发生下列反应:N2+3H2?2NH3,△H<0,如图是某一时间段中反应速率与反应进程的曲线关系图.回答下列问题: