题目内容
 目前工业上利用CO2来生产燃料甲醇,可将CO2变废为宝.
目前工业上利用CO2来生产燃料甲醇,可将CO2变废为宝. Ⅰ.已知常温常压下:
①CH3OH(l)+O2(g)=CO(g)+2H2O(g)△H1=-354.8 kJ?mol-1
②2CO(g)+O2(g)=2CO2(g)△H2=-566 kJ?mol-1
则反应2CO2(g)+4H2O(g)=2CH3OH(l)+3O2(g)△H=
Ⅱ.如图是一个化学过程的示意图.已知甲池的总反应式为:2CH3OH+3O2+4KOH═2K2CO3+6H2O
(1)请回答图中甲、乙两池的名称.甲电池是
(2)请回答下列电极的名称:通入CH3OH的电极名称是
(3)通入O2的电极的电极反应式为:
(4)乙池中反应的化学方程式为
(5)电解一段时间后,乙池中A(Fe)极的质量增加5.4g时,且溶液的体积为500mL,求所得溶液在25℃时的pH=
考点:用盖斯定律进行有关反应热的计算,原电池和电解池的工作原理
专题:化学反应中的能量变化,电化学专题
分析:I.根据盖斯定律结合已知热化学方程式构建目标方程式再计算反应热;
II.(1)甲装置中能自发的发生氧化还原反应是一个燃料电池;乙有外加电源,所以是电解池.
(2)根据得失电子判断正负极,根据外加电源判断阴阳极.
(3)氧气在正极上得电子;Fe为阴极,阴极上银离子得电子;
(4)依据电子守恒和电解的实质写出化学方程式;
(5)根据电解方程式计算生成的氢离子的物质的量和浓度;根据得失电子数相等找出银与氧气的关系式,然后计算
II.(1)甲装置中能自发的发生氧化还原反应是一个燃料电池;乙有外加电源,所以是电解池.
(2)根据得失电子判断正负极,根据外加电源判断阴阳极.
(3)氧气在正极上得电子;Fe为阴极,阴极上银离子得电子;
(4)依据电子守恒和电解的实质写出化学方程式;
(5)根据电解方程式计算生成的氢离子的物质的量和浓度;根据得失电子数相等找出银与氧气的关系式,然后计算
解答:
解:I.已知常温常压下:
①CH3OH(l)+O2(g)═CO(g)+2H2O(g)△H=-354.8kJ/mol
②2CO(g)+O2(g)═2CO2(g)△H=-566kJ/mol
根据目标方程式,改写方程式①和②,把方程式①反写乘以2,再把方程②反写,然后二者相加,即得到目标方程,所以△H=-△H1×2-△H2=+1275.68kJ/mol,
故答案为:+1275.68;
II.(1)甲装置中能自发的发生氧化还原反应是一个燃料电池,所以甲是把化学能转变为电能的装置,是原电池;乙有外加电源,所以是电解池;
故答案为:原电池;电解池;
(2)根据2CH3OH+3O2+4KOH=2K2CO3+6H2O知,CH3OH发生氧化反应,所以该电极是负极,O2 发生还原反应,所以该电极是正极;石墨与原电池的正极相连,所以B石墨电极是阳极.
故答案为:负极;阳极;
(3)根据2CH3OH+3O2+4KOH=2K2CO3+6H2O知,CH3OH发生氧化反应,所以该电极是负极,O2 得电子和水反应生成氢氧根离子,发生还原反应,所以该电极是正极;石墨与原电池的正极相连,所以石墨电极是阳极该电极上发生氧化反应,电极反应为:O2+2H2O+4e-=4OH-;铁电极是阴极,该电极上银离子得电子发生还原反应,电极反应为:4Ag++4e-=4Ag;
故答案为:O2+2H2O+4e-=4OH-;4Ag++4e-=4Ag;
(4)乙池中离子放电顺序为:阳离子 Ag+>H+,阴离子OH->NO3 -,阴极电极反应为:O2+2H2O+4e-=4OH-;阳极电极反应为:4Ag++4e-=4Ag;依据电子守恒和电解的实质写出化学方程式:4AgNO4+2H2O
4Ag+O2↑+4HNO3
故答案为:4AgNO4+2H2O
4Ag+O2↑+4HNO3;
(5)乙池中A(Fe)极是阴极,阴极的质量增加5.40g是银,其物质的量为
=0.05mol,
由4AgNO4+2H2O
4Ag+O2↑+4HNO3
得生成的硝酸为0.05mol,则氢离子为0.05mol,其浓度为:
=
=0.1mol/L,所以pH=1;
根据得失电子数相等,氧气与银的关系式为:
O2--------4Ag
22.4L 4mol
VL 0.05mol
则V=0.28L=280ml
故答案为:1;280.
①CH3OH(l)+O2(g)═CO(g)+2H2O(g)△H=-354.8kJ/mol
②2CO(g)+O2(g)═2CO2(g)△H=-566kJ/mol
根据目标方程式,改写方程式①和②,把方程式①反写乘以2,再把方程②反写,然后二者相加,即得到目标方程,所以△H=-△H1×2-△H2=+1275.68kJ/mol,
故答案为:+1275.68;
II.(1)甲装置中能自发的发生氧化还原反应是一个燃料电池,所以甲是把化学能转变为电能的装置,是原电池;乙有外加电源,所以是电解池;
故答案为:原电池;电解池;
(2)根据2CH3OH+3O2+4KOH=2K2CO3+6H2O知,CH3OH发生氧化反应,所以该电极是负极,O2 发生还原反应,所以该电极是正极;石墨与原电池的正极相连,所以B石墨电极是阳极.
故答案为:负极;阳极;
(3)根据2CH3OH+3O2+4KOH=2K2CO3+6H2O知,CH3OH发生氧化反应,所以该电极是负极,O2 得电子和水反应生成氢氧根离子,发生还原反应,所以该电极是正极;石墨与原电池的正极相连,所以石墨电极是阳极该电极上发生氧化反应,电极反应为:O2+2H2O+4e-=4OH-;铁电极是阴极,该电极上银离子得电子发生还原反应,电极反应为:4Ag++4e-=4Ag;
故答案为:O2+2H2O+4e-=4OH-;4Ag++4e-=4Ag;
(4)乙池中离子放电顺序为:阳离子 Ag+>H+,阴离子OH->NO3 -,阴极电极反应为:O2+2H2O+4e-=4OH-;阳极电极反应为:4Ag++4e-=4Ag;依据电子守恒和电解的实质写出化学方程式:4AgNO4+2H2O
| ||
故答案为:4AgNO4+2H2O
| ||
(5)乙池中A(Fe)极是阴极,阴极的质量增加5.40g是银,其物质的量为
| 5.4g |
| 108g/mol |
由4AgNO4+2H2O
| ||
得生成的硝酸为0.05mol,则氢离子为0.05mol,其浓度为:
| n |
| V |
| 0.05mol |
| 0.5L |
根据得失电子数相等,氧气与银的关系式为:
O2--------4Ag
22.4L 4mol
VL 0.05mol
则V=0.28L=280ml
故答案为:1;280.
点评:本题考查了盖斯定律的应用、原电池和电解池的工作原理的应用,主要考查了是电池判断、电极判断,电解方程式的书写、电子守恒的应用等,题目难度中等.

练习册系列答案
相关题目
在允许加热的条件下,只用一种试剂就可以鉴别硫酸铵、氯化钾、氯化镁、硫酸铝和硫酸铁溶液,这种试剂是( )
| A、NaOH |
| B、NH3?H2O |
| C、AgNO3 |
| D、BaCl2 |
下列关于有机物的说法正确的是( )
| A、乙烯和聚乙烯都能发生加成反应 |
| B、淀粉和纤维素的分子式相同,互为同分异构体 |
| C、粮食酿酒的过程涉及到了水解反应、氧化还原反应等复杂变化 |
| D、向蛋白质溶液中分别滴加饱和NaCl 溶液和CuSO4 溶液,蛋白质均发生变性 |
对如图所示分子的描述不正确的是( )
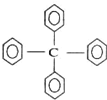

| A、该物质的分子式为C25H20 |
| B、该物质所有氢原子不可能在同一平面上 |
| C、该物质属于烷烃 |
| D、该物质的一氯代物有3种 |
某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )
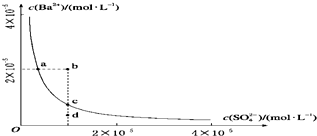

| A、加入Na2SO4可以使溶液由a点变到c点 |
| B、通过蒸发可以使溶液由d点变到c点 |
| C、b、d点都是不能长时间稳定存在的点 |
| D、a点对应的Ksp大于c点对应的Ksp |