题目内容
3.亚氯酸钠(NaClO2)常用于水的消毒和砂糖、油脂的漂白与杀菌.以下是用过氧化氢法生产亚氯酸钠的工艺流程图: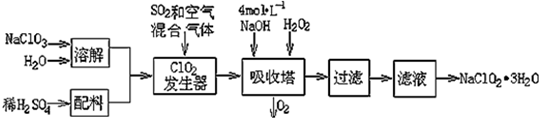
已知:①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2•3H2O;
②Ksp(FeS)=6.3×10-18; Ksp(CuS)=6.3×10-36;Ksp(PbS)=2.4×10-28
(1)吸收塔内发生反应的离子方程式为2NaOH+2ClO2+H2O2=2NaClO2+2H2O+O2.该工艺流程中的NaClO3、ClO2、NaClO2都是强氧化剂,它们都能和浓盐酸反应制取Cl2.若用二氧化氯和浓盐酸制取Cl2,当生成5mol Cl2时,通过还原反应制得氯气的质量为71g.
(2)从滤液中得到NaClO2•3H2O晶体的所需操作依次是dc (填写序号).
a.蒸馏 b.灼烧 c.过滤 d.冷却结晶 e.蒸发
(3)印染工业常用亚氯酸钠(NaClO2)漂白织物,漂白织物时真正起作用的是HClO2.
表是 25℃时HClO2及几种常见弱酸的电离平衡常数:
| 弱酸 | HClO2 | HF | HCN | H2S |
| Ka | 1×10-2 | 6.3×10-4 | 4.9×10-10 | K1=9.1×10-8 K2=1.1×10-12 |
②Na2S是常用的沉淀剂.某工业污水中含有等浓度的Cu2+、Fe2+、Pb2+离子,滴加Na2S溶液后首先析出的沉淀是CuS;当最后一种离子沉淀完全时(该离子浓度为10-5mol•L-1),此时体系中的S2-的浓度为6.3×10-13mol/L.
分析 (1)根据题目信息并运用氧化还原反应理论判断反应物、生成物.根据流程信息可知,吸收塔内生成NaClO2,一定有ClO2→NaClO2,Cl元素化合价降低,被还原;则H2O2必定被氧化,有氧气产生,据此配平书写方程式;
反应中ClO2是氧化剂,发生还原反应,HCl是还原剂,发生氧化反应,根据电子转移计算氧化剂与还原剂的物质的量之比,据此确定还原产物与氧化产物物质的量之比,计算还原反应生成的氯气,再根据m=nM计算;
(2)从溶液中得到含结晶水的晶体,只能采取蒸发、浓缩、冷却结晶方法,通过过滤得到粗晶体.得到的粗晶体经过重结晶可得到纯度更高的晶体;
(3)①、弱酸的电离平衡常数越大,酸性越强,反之酸性越弱,酸性越弱,对应钠盐中酸根离子水解程度越大,溶液的PH越大;
NaF、NaCN两溶液中钠离子浓度相同,由于阴离子都是-1价离子,1mol阴离子水解得到1mol氢氧根离子,阴离子的总浓度不变,两溶液中阴离子总浓度相同,故溶液碱性越强,氢离子浓度越小,含有阴阳离子总数的越小;
②物质组成类型相同,溶度积越小,溶解度越小,滴加硫化钠,相应阳离子最先沉淀;根据溶度积计算S2-的浓度.
解答 解:(1)根据流程信息可知,吸收塔内生成NaClO2,所以一定有ClO2→NaClO2,化合价降低,被还原;则H2O2必定被氧化,有氧气产生,反应方程式为:2NaOH+2ClO2+H2O2=2 NaClO2+2H2O+O2,反应中ClO2是氧化剂,发生还原反应,HCl是还原剂,发生氧化反应,根据电子转移守恒可知4n(ClO2)=n(HCl),故n(ClO2):n(HCl)=1:4,故还原产物与氧化产物物质的量之比为1:4,故还原反应生成的氯气为5mol×$\frac{1}{5}$=1mol,通过还原反应制得氯气的质量为1mol×71g/mol=71g,
故答案为:2NaOH+2ClO2+H2O2=2NaClO2+2H2O+O2;71;
(2)从溶液中得到含结晶水的晶体,只能采取蒸发、浓缩、冷却结晶方法,通过过滤得到粗晶体,所以操作顺序为dc,故答案为:dc;
(3)①根据电离平衡常数可知酸性强弱顺序为:HClO2>HF>HCN>HS-,酸性越弱,对应钠盐中酸根离子水解程度越大,溶液的PH越大,故物质的量浓度相等各溶液pH关系为:pH(Na2S)>pH(NaCN)>pH(NaF)>pH(NaClO2),
NaF、NaCN两溶液中钠离子浓度相同,由于阴离子都是-1价离子,1mol阴离子水解得到1mol氢氧根离子,阴离子的总浓度不变,两溶液中阴离子总浓度相同,溶液为碱性,pH(NaCN)>pH(NaF),故NaCN溶液碱氢离子浓度较小,含有阴阳离子总数较小,即NaF溶液中阴阳离子总数较大,
故答案为:pH(Na2S)>pH(NaCN)>pH(NaF)>pH(NaClO2);前者大;
②物质组成类型相同,溶度积越小,溶解度越小,滴加硫化钠,相应阳离子最先沉淀,故首先析出沉淀是CuS,Fe2+最后沉淀,沉淀完全时该浓度为10-5mol•L-1,此时的S2-的浓度为$\frac{6.3×10{\;}^{-18}}{10{\;}^{-5}}$mol/L=6.3×10-13mol/L,
故答案为:CuS;6.3×10-13mol/L.
点评 本题以学生比较陌生的亚氯酸钠制备为载体,考查学生阅读题目获取信息的能力、氧化还原反应计算、物质分离提纯、盐类水解、溶度积的有关计算与应用等,是在新情境下综合运用知识解决问题的能力的考查,题目有一定的难度.

| A. | 0.308 | B. | 308 | C. | 154 | D. | 0.154 |
①CS2+3Cl2$\frac{\underline{\;95-100℃\;}}{\;}$CCl4+S2Cl2;
②2S+Cl2$\frac{\underline{\;111-140℃\;}}{\;}$S2Cl2.
已知:S2Cl2易与水反应;S2Cl2+Cl2$\stackrel{△}{?}$2SCl2.
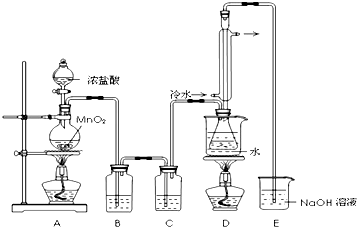
下表是几种物质的熔沸点,如图是反应装置图:
| 物质 | 沸点/℃ | 熔点/℃ |
| S | 445 | 113 |
| CS2 | 47 | -109 |
| CCl4 | 77 | -23 |
| S2Cl2 | 137 | -77 |
(2)若装置C更换成干燥管,则装置C中可选用的固体试剂是无水CaCl2(或固体P2O5).
(3)D装置中冷凝管的作用是冷凝、回流、导气;反应结束后,将D装置锥形瓶内的混合物中分离出产物的方法是蒸馏.
(4)S2Cl2与足量水反应有黄色沉淀生成,产生的无色气体能使品红溶液褪色,则该反应的化学方程式为2S2Cl2+2H2O═3S↓+SO2↑+4HCl↑.
(5)为了提高制得的产品S2Cl2的纯度,关键的操作是控制好温度和控制浓盐酸的滴速不能太快.
(6)上图尾部装置不够完善,改进措施是在D和E之间增加干燥装置,同时尾气吸收要防倒吸.
(7)若A中消耗了26.1g MnO2,得到10.8g产品,本实验的产率是80%.
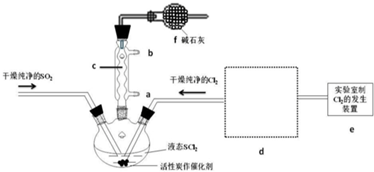
(1)仪器c的名称是球形冷凝管,装置f的作用是吸收逸出有毒的Cl2、SO2,防止空气中的水蒸气进入反应装置,防止SOCl2水解.
(2)SOCl2与水反应的化学方程式为SOCl2+H2O=SO2↑+2HCl↑.蒸干AlCl3溶液不能得到无水AlCl3,使SOCl2与AlCl3•6H2O混合加热,可得到无水AlCl3,试解释原因:AlCl3溶液易水解,AlCl3•6H2O与SOCl2混合加热,SOCl2与AlCl3•6H2O中的结晶水作用,生成无水AlCl3及SO2和HCl气体,SOCl2吸水,产物SO2和HCl抑制AlCl3水解.
(3)下列四种制备SO2的方案中最佳选择是丁.
| 方案 | 甲 | 乙 | 丙 | 丁 |
| 发生装置 | 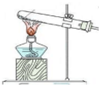 |  | 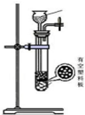 | 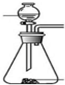 |
| 所选试剂 | NaHSO3固体 | 18.4mol/LH2SO4+Cu | 4mol/LHNO3+Na2SO3 | 70%H2SO4+K2SO3 |
(5)试验结束后,将三颈烧瓶中混合物分离开的实验操作是蒸馏;(已知SCl2的沸点为50℃)若反应中消耗的Cl2的体积为896ml(已转化为标准状况,SO2足量),最后得到纯净的SOCl24.76g,则SOCl2的产率为50% (保留三位有效数字).


 .
.