题目内容
16.某气态氧化物化学式为RO2,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为64g/mol.分析 标准状况下气体摩尔体积约为22.4L/mol,先根据n=$\frac{V}{{V}_{m}}$计算出标准状况下448mL该气体的物质的量,再根据m=$\frac{m}{n}$计算出该氧化物的摩尔质量.
解答 解:在标准状况下,1.28g该氧化物的体积为448mL,该气体的物质的量为:$\frac{0.448L}{22.4L/mol}$=0.02mol,
该气体的摩尔质量为:$\frac{1.28g}{0.02mol}$=64g/mol,
故答案为:64 g/mol.
点评 本题考查了物质的量的计算,题目难度不大,明确物质的量与气体摩尔体积、摩尔质量之间的关系为解答关键,试题侧重考查学生的分析能力及化学计算能力.

练习册系列答案
 快乐5加2金卷系列答案
快乐5加2金卷系列答案
相关题目
7.如图为空气成分示意图(按体积计算),其中“a”代表的是( )


| A. | 氧气 | B. | 氮气 | C. | 二氧化碳 | D. | 稀有气体 |
4.将浓度为0.1mol•L-1 HF溶液加水不断稀释,下列各量始终保持增大的是( )
| A. | c(H+) | B. | Ka(HF) | C. | $\frac{c({H}^{+})}{c(O{H}^{-})}$ | D. | $\frac{c({H}^{+})}{c(HF)}$ |
11.下列各组物质相互混合反应后,最终有白色沉淀生成的是( )
①少量Ca(OH)2投入过量NaHCO3溶液中
②过量NaOH溶液和明矾溶液混合
③金属钠投入到FeCl2中
④向NaAlO2溶液中通入过量CO2
⑤向饱和Na2CO3溶液中通入过量CO2.
①少量Ca(OH)2投入过量NaHCO3溶液中
②过量NaOH溶液和明矾溶液混合
③金属钠投入到FeCl2中
④向NaAlO2溶液中通入过量CO2
⑤向饱和Na2CO3溶液中通入过量CO2.
| A. | ①②③④⑤ | B. | 只有①④⑤ | C. | 只有②③ | D. | 只有③④ |
1.向ZnSO4和CuCl2的混合溶液中加入过量的铁粉,充分反应后,过滤、洗涤、干燥得到滤渣,该滤渣中含有的金属是( )
| A. | Zn、Fe | B. | Zn、Cu | C. | Fe、Cu | D. | Zn、Fe、Cu |
8.反应4A(s)+3B(g)═2C(g)+xD(g),经2min后B的浓度减少了1.2mol/L,下列反应速率的表示正确的是( )
| A. | 用A表示的反应速率是0.8mol/(L•min) | |
| B. | 2min末时的反应速率,用B表示为0.6mol/(L•min) | |
| C. | 用C表示的反应速率是0.4mol/(L•min) | |
| D. | 若用D表示反应速率是0.8mol/(L•min),则x=2 |
3.亚氯酸钠(NaClO2)常用于水的消毒和砂糖、油脂的漂白与杀菌.以下是用过氧化氢法生产亚氯酸钠的工艺流程图:
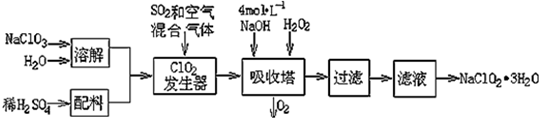
已知:①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2•3H2O;
②Ksp(FeS)=6.3×10-18; Ksp(CuS)=6.3×10-36;Ksp(PbS)=2.4×10-28
(1)吸收塔内发生反应的离子方程式为2NaOH+2ClO2+H2O2=2NaClO2+2H2O+O2.该工艺流程中的NaClO3、ClO2、NaClO2都是强氧化剂,它们都能和浓盐酸反应制取Cl2.若用二氧化氯和浓盐酸制取Cl2,当生成5mol Cl2时,通过还原反应制得氯气的质量为71g.
(2)从滤液中得到NaClO2•3H2O晶体的所需操作依次是dc (填写序号).
a.蒸馏 b.灼烧 c.过滤 d.冷却结晶 e.蒸发
(3)印染工业常用亚氯酸钠(NaClO2)漂白织物,漂白织物时真正起作用的是HClO2.
表是 25℃时HClO2及几种常见弱酸的电离平衡常数:
①常温下,物质的量浓度相等的NaClO2、NaF、NaCN、Na2S四种溶液的pH由大到小的顺序为pH(Na2S)>pH(NaCN)>pH(NaF)>pH(NaClO2)(用化学式表示);体积相等,物质的量浓度相同的NaF、NaCN两溶液中所含阴阳离子总数的大小关系为:前者大(填“前者大”“相等”或“后者大”).
②Na2S是常用的沉淀剂.某工业污水中含有等浓度的Cu2+、Fe2+、Pb2+离子,滴加Na2S溶液后首先析出的沉淀是CuS;当最后一种离子沉淀完全时(该离子浓度为10-5mol•L-1),此时体系中的S2-的浓度为6.3×10-13mol/L.

已知:①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2•3H2O;
②Ksp(FeS)=6.3×10-18; Ksp(CuS)=6.3×10-36;Ksp(PbS)=2.4×10-28
(1)吸收塔内发生反应的离子方程式为2NaOH+2ClO2+H2O2=2NaClO2+2H2O+O2.该工艺流程中的NaClO3、ClO2、NaClO2都是强氧化剂,它们都能和浓盐酸反应制取Cl2.若用二氧化氯和浓盐酸制取Cl2,当生成5mol Cl2时,通过还原反应制得氯气的质量为71g.
(2)从滤液中得到NaClO2•3H2O晶体的所需操作依次是dc (填写序号).
a.蒸馏 b.灼烧 c.过滤 d.冷却结晶 e.蒸发
(3)印染工业常用亚氯酸钠(NaClO2)漂白织物,漂白织物时真正起作用的是HClO2.
表是 25℃时HClO2及几种常见弱酸的电离平衡常数:
| 弱酸 | HClO2 | HF | HCN | H2S |
| Ka | 1×10-2 | 6.3×10-4 | 4.9×10-10 | K1=9.1×10-8 K2=1.1×10-12 |
②Na2S是常用的沉淀剂.某工业污水中含有等浓度的Cu2+、Fe2+、Pb2+离子,滴加Na2S溶液后首先析出的沉淀是CuS;当最后一种离子沉淀完全时(该离子浓度为10-5mol•L-1),此时体系中的S2-的浓度为6.3×10-13mol/L.
