题目内容
下列离子方程式错误的是( )
| A、向Mg(HCO3)2溶液中加入过量的 NaOH溶液:Mg2++2HCO3-+4OH-=Mg(OH)2↓+2CO32-+2H2O |
| B、向亚硫酸钡固体中加入稀硝酸:3BaSO3+2H++2NO3-=3BaSO4↓+2NO↑+H2O |
| C、在银氨溶液中滴加过量稀硝酸:[Ag(NH3)2]++2H+=Ag++2NH4+ |
| D、向NH4HSO4稀溶液中逐滴加入Ba(OH)2稀溶液至SO42-刚好沉淀完全:Ba2++2OH-+NH4++H++SO42-=BaSO4↓+NH3?H2O+H2O |
考点:离子方程式的书写
专题:
分析:A.向Mg(HCO3)2溶液中加入过量的 NaOH溶液,反应生成氢氧化镁沉淀和碳酸钠、水;
B.向亚硫酸钡固体中加入稀硝酸,发生氧化还原反应,生成硫酸钡、一氧化氮和水;
C.在银氨溶液中滴加过量稀硝酸,反应生成硝酸铵和硝酸银、水;
D.向NH4HSO4稀溶液中逐滴加入Ba(OH)2稀溶液至SO42-刚好沉淀完全,反应生成硫酸钡、一水合氨和水.
B.向亚硫酸钡固体中加入稀硝酸,发生氧化还原反应,生成硫酸钡、一氧化氮和水;
C.在银氨溶液中滴加过量稀硝酸,反应生成硝酸铵和硝酸银、水;
D.向NH4HSO4稀溶液中逐滴加入Ba(OH)2稀溶液至SO42-刚好沉淀完全,反应生成硫酸钡、一水合氨和水.
解答:
解:A.向Mg(HCO3)2溶液中加入过量的 NaOH溶液,离子方程式:Mg2++2HCO3-+4OH-=Mg(OH)2↓+2CO32-+2H2O,故A正确;
B.向亚硫酸钡固体中加入稀硝酸,离子方程式:3BaSO3+2H++2NO3-=3BaSO4↓+2NO↑+H2O,故B正确;
C.在银氨溶液中滴加过量稀硝酸,离子反应为OH-+[Ag(NH3)2]++2H+=Ag++2NH4++H2O,故C错误;
D.向NH4HSO4稀溶液中逐滴加入Ba(OH)2稀溶液至SO42-刚好沉淀完全,离子方程式:Ba2++2OH-+NH4++H++SO42-=BaSO4↓+NH3?H2O+H2O,故D正确;
故选:C.
B.向亚硫酸钡固体中加入稀硝酸,离子方程式:3BaSO3+2H++2NO3-=3BaSO4↓+2NO↑+H2O,故B正确;
C.在银氨溶液中滴加过量稀硝酸,离子反应为OH-+[Ag(NH3)2]++2H+=Ag++2NH4++H2O,故C错误;
D.向NH4HSO4稀溶液中逐滴加入Ba(OH)2稀溶液至SO42-刚好沉淀完全,离子方程式:Ba2++2OH-+NH4++H++SO42-=BaSO4↓+NH3?H2O+H2O,故D正确;
故选:C.
点评:本题考查了离子方程式的书写,为高考的热门考点,明确反应的实质是解题关键,注意反应物用量对反应的影响,注意化学式的正确拆分,选项CD为易错选项.

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目
下列各组的两种物质在溶液中的反应,可用同一离子方程式表示的是( )
| A、氢氧化钠与盐酸;氢氧化铜与盐酸 |
| B、BaCl2溶液与Na2SO4溶液;Ba(OH)2溶液与H2SO4溶液 |
| C、Na2CO3溶液与硝酸溶液;CaCO3与硝酸溶液 |
| D、石灰石与硝酸反应;大理石与盐酸 |
下列反应的离子方程式书写正确的是( )
| A、向AgCl悬浊液中滴加硫化钠溶液,白色沉淀变成黑色:2AgCl(s)+S2-(aq)═Ag2S(s)+2Cl-(aq) | ||||
| B、向NaClO溶液中通过少量SO2气体:2ClO-+SO2+H20═2HClO+SO32- | ||||
C、用两个铜电极电解硫酸铜溶液:Cu2++2H2O
| ||||
| D、硫化钠溶于水:S2-+2H2O?H2S+2OH- |
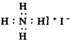
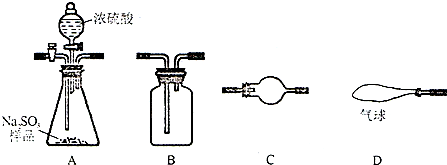
 X、Y、Z、W、T是短周期表中的5种主族元素.X基态原子核外L层p电子数等于s电子数.Y的一种核素的质量数为19,中子数比质子数多1.T-离子核外电子数与氩原子的核外电子数相同.X、Y、Z、W的第一电离能与它们的核电荷数的关系如图所示.
X、Y、Z、W、T是短周期表中的5种主族元素.X基态原子核外L层p电子数等于s电子数.Y的一种核素的质量数为19,中子数比质子数多1.T-离子核外电子数与氩原子的核外电子数相同.X、Y、Z、W的第一电离能与它们的核电荷数的关系如图所示.