��Ŀ����
������ͼ���ʼ�ת���Ŀ�ͼ���ش��й����⣺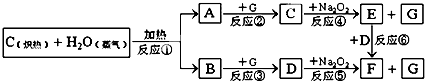
��1��д����ͼ������A��B��E��G�ֱ�ָ�����ʵĻ�ѧʽ��
A B E G
��2����ͼ2molNa2O2������ˮ������Ӧ���ɵñ�״������������ L��ͬʱ��Ӧ��ת�Ƶ��������� ����NA��ʾ����٤��������
��3����Ӧ�٢ڢۢܢݢ���������ԭ��Ӧ���� ��
��4�����A��B�������7.8g��ƽ��Ħ������10g?mol-1��������G��ַ�Ӧ��ͨ������Na2O2�㣬��ʹ
Na2O2���� g�����õ�O2 mol��

��1��д����ͼ������A��B��E��G�ֱ�ָ�����ʵĻ�ѧʽ��
A
��2����ͼ2molNa2O2������ˮ������Ӧ���ɵñ�״������������
��3����Ӧ�٢ڢۢܢݢ���������ԭ��Ӧ����
��4�����A��B�������7.8g��ƽ��Ħ������10g?mol-1��������G��ַ�Ӧ��ͨ������Na2O2�㣬��ʹ
Na2O2����
���㣺������ƶ�
ר�⣺�ƶ���
������C��H2O��Ӧ����CO��H2����ת����ϵ��֪GΪO2��EӦΪNaOH��FΪNa2CO3����AΪH2��BΪCO��CΪH2O��DΪCO2����϶�Ӧ���ʵ������Լ���ĿҪ��ɽ����⣮
���
�⣺C��H2O��Ӧ����CO��H2����ת����ϵ��֪GΪO2��EӦΪNaOH��FΪNa2CO3����AΪH2��BΪCO��CΪH2O��DΪCO2��
��1�������Ϸ�����֪AΪH2��BΪCO��EΪNaOH��GΪO2��
�ʴ�Ϊ��H2��CO��NaOH��O2��
��2������������������x��ת�Ƶ�������y��
2Na2O2+2H2O=4NaOH+O2 ��ת�Ƶ���
2mol 22.4L 2mol
2mol x y
x=22.4L
y=2NA
�ʴ�Ϊ��22.4L��2NA��
��3����Ӧ�٢ڢۢܢݢ��У�ֻ�з�Ӧ�������������������̼�ķ�Ӧ���Ƿ�������ԭ��Ӧ����������������ԭ��Ӧ����Ӧ�ж���Ԫ�صĻ��ϼ۷����仯��
�ʴ�Ϊ���٢ڢۢܢݣ�
��4��һ����̼��������������Ӧ���ɶ�����̼��ˮ����2Na2O2+2H2O=4NaOH+O2 ��2Na2O2+2CO2=2Na2CO3+O2 ��֪�������������ص���CO��H2���������ʹ�����������7.8g��
��������һ����̼�����ʵ�����n1�����������ʵ�����n2��
M=
=10��������n1��n2=4��9���ɶ���������28n1+2n2=7.8���������n1=0.24��n2=0.54��
����Ԫ���غ�CO��H2��O2��Ӧ������0.24molCO2��0.54molH2O����2Na2O2+2H2O=4NaOH+O2 ��2Na2O2+2CO2=2Na2CO3+O2 ��֪���������������Ϊ
��0.24mol+
��0.54mol=0.39mol��
�ʴ�Ϊ��7.8��0.39��
��1�������Ϸ�����֪AΪH2��BΪCO��EΪNaOH��GΪO2��
�ʴ�Ϊ��H2��CO��NaOH��O2��
��2������������������x��ת�Ƶ�������y��
2Na2O2+2H2O=4NaOH+O2 ��ת�Ƶ���
2mol 22.4L 2mol
2mol x y
x=22.4L
y=2NA
�ʴ�Ϊ��22.4L��2NA��
��3����Ӧ�٢ڢۢܢݢ��У�ֻ�з�Ӧ�������������������̼�ķ�Ӧ���Ƿ�������ԭ��Ӧ����������������ԭ��Ӧ����Ӧ�ж���Ԫ�صĻ��ϼ۷����仯��
�ʴ�Ϊ���٢ڢۢܢݣ�
��4��һ����̼��������������Ӧ���ɶ�����̼��ˮ����2Na2O2+2H2O=4NaOH+O2 ��2Na2O2+2CO2=2Na2CO3+O2 ��֪�������������ص���CO��H2���������ʹ�����������7.8g��
��������һ����̼�����ʵ�����n1�����������ʵ�����n2��
M=
| 28n1+2n2 |
| n 1+n 2 |
����Ԫ���غ�CO��H2��O2��Ӧ������0.24molCO2��0.54molH2O����2Na2O2+2H2O=4NaOH+O2 ��2Na2O2+2CO2=2Na2CO3+O2 ��֪���������������Ϊ
| 1 |
| 2 |
| 1 |
| 2 |
�ʴ�Ϊ��7.8��0.39��
����������������ͼ�����ʽ����C��Na��Ԫ�ص��ʼ��仯����֮����ת����ϵ����������������ѧ�������д��������ѧ����ȣ��Ѷ��еȣ�ע�⣨4�������������ʵ����������÷���ʽ�۲죬���Ԫ���غ㣬���������ʵ���Ϊһ����̼��������������һ�룮

��ϰ��ϵ�д�
�����Ŀ
��֪�������ʵ��۵�ͷе㣨�棩���£�����˵������ȷ���ǣ�������
ע��AlCl3�۵���202��10Pa�����²ⶨ��
| NaCl | KBr | AlCl3 | ������ | SiCl4 | |
| �۵� | 801 | 730 | 190��0.25MPa�� | 2300 | -70 |
| �е� | 1413 | 1380 | 180 | 2500 | 57 |
| A��SiCl4�Ƿ��Ӿ��� |
| B����������ԭ�Ӿ��� |
| C��AlCl3���������� |
| D��MgCl2�������Ӽ���ǿ�ȱ�NaCl�� |
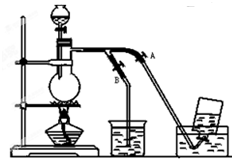 ��ͼ��ʾ��û��ͨ�紦�ռ�����������ʱ��Ƶ�װ��ͼ��ͼ��A��B�ǿɿ��Ƶĵ������У�
��ͼ��ʾ��û��ͨ�紦�ռ�����������ʱ��Ƶ�װ��ͼ��ͼ��A��B�ǿɿ��Ƶĵ������У�