题目内容
17.设NA为阿伏加德罗常数的值,下列说法正确的是( )| A. | 向密闭容器中通入0.1molN2和0.3molH2,在一定条件下充分反应,容器中N原子数为0.2NA | |
| B. | Cu-Zn-CuSO4原电池工作时,当转移电子数为0.2NA时,正极溶解Zn6.5g | |
| C. | 电解102g熔融的Al2O3,能产生54g金属铝和33.6LO2,转移电子数为6NA | |
| D. | 电解精炼铜当转移电子数为2NA时,阳极溶解的铜和阴极析出的铜均为64g |
分析 A、反应过程中满足原子个数守恒;
B、铜锌原电池中,正极上Cu2+放电;
C、氧气所处的状态不明确;
D、电解精炼铜时,阳极上溶解的不止是铜,还有比铜活泼的金属.
解答 解:A、反应过程中满足原子个数守恒,故无论氮气和氢气反应情况如何,容器中的N原子个数一直是0.2NA个,故A正确;
B、铜锌原电池中,正极上Cu2+放电,锌在负极放电,故B错误;
C、氧气所处的状态不明确,故生成的氧气的体积不一定是33.6L,故C错误;
D、电解精炼铜时,阳极上溶解的不止是铜,还有比铜活泼的金属,故当转移的电子为2NA时,阳极上溶解的铜小于64g,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
7.下列鉴别物质的方法不能达到目的是( )
| A. | 用碘水鉴别淀粉溶液和蔗糖溶液 | |
| B. | 用酸性高锰酸钾溶液鉴别乙烯和乙炔 | |
| C. | 用溴水鉴别四氯化碳和苯两种无色液体 | |
| D. | 用金属钠鉴别乙醇与二甲醚(CH3OCH3) |
8.下列说法正确的是( )
①用浓氨水清洗做过银镜反应的试管;
②用酒精清洗做过碘升华的烧杯;
③氢氟酸保存在玻璃瓶中,烧碱溶液存放在带有玻璃塞的试剂瓶中;
④液溴直接存放在棕色滴瓶中,浓硝酸保存在带橡胶塞的无色玻璃瓶中;
⑤少量金属钠保存在煤油中,少量白磷保存在水中.
①用浓氨水清洗做过银镜反应的试管;
②用酒精清洗做过碘升华的烧杯;
③氢氟酸保存在玻璃瓶中,烧碱溶液存放在带有玻璃塞的试剂瓶中;
④液溴直接存放在棕色滴瓶中,浓硝酸保存在带橡胶塞的无色玻璃瓶中;
⑤少量金属钠保存在煤油中,少量白磷保存在水中.
| A. | ②⑤ | B. | ①②③④ | C. | ①②③⑤ | D. | 全都正确 |
5.用质量相同的铁单质与下列条件下相同体积的硫酸反应时,速率最快的是( )
| A | 20℃ | 铁片 | 1mol/L硫酸 | B | 30℃ | 铁粉 | 1mol/L稀硫酸 |
| C | 30℃ | 铁粉 | 2mol/L稀硫酸 | D | 30℃ | 铁片 | 2mol/L稀硫酸 |
| A. | A | B. | B | C. | C | D. | D |
12.已知2SO2(g)+O2?2SO3(g)(正反应放热).若在500℃和催化剂的作用下,该反应在容积固定的密闭容器中进行,下列有关说法正确的是( )
| A. | 若降低温度,可以加快反应速率 | |
| B. | 在上述条件下,SO2能完全转化为SO3 | |
| C. | 反应达平衡时,SO2和SO3的浓度一定相等 | |
| D. | 反应达平衡时,正反应速率和逆反应速率一定相等 |
2.下列说法正确的是( )
| A. | 乙烯、乙醇、过氧化钠、CaCl2都含有非极性键 | |
| B. | 乙醇、乙酸、水分子中均含有氢键 | |
| C. | 甲苯分子中共平面的原子最多有13个 | |
| D. | BF3、PCl3、CCl4、苯中所有原子全部满足最外层为8个电子结构 |
6.300mL0.1mol•L-1Na2SO4溶液与100mL0.2mol•L-1Al2(SO4)3溶液中所含SO42-物质的量之比是( )
| A. | 1:2 | B. | 1:3 | C. | 2:1 | D. | 3:2 |
 NH3可用来制尿素(
NH3可用来制尿素(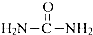 )等化学肥料.
)等化学肥料.