题目内容
NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A、由D和18O所组成的水11g,所含的中子数为4NA |
| B、常温常压下,8g O2含有4NA个电子 |
| C、25℃时,pH=13的1L Ba(OH)2溶液中含有OH-的数目为0.2 |
| D、1L 1mol/L的NaAlO2水溶液中含有的氧原子数为2NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.D和18O所组成的水的摩尔质量为22g/mol,该水分子中含有12个中子,11g该水的物质的量为0.5mol,含有5.5mol中子;
B.8g氧气的物质的量为0.25mol,氧气中含有16个电子,0.25mol氧气中含有4mol电子;
C.pH=13的1L Ba(OH)2溶液中氢氧根离子浓度为0.1mol/L,1L该溶液中含有0.1mol氢氧根离子;
D.偏铝酸钠溶液中的溶剂水中也含有氧原子.
B.8g氧气的物质的量为0.25mol,氧气中含有16个电子,0.25mol氧气中含有4mol电子;
C.pH=13的1L Ba(OH)2溶液中氢氧根离子浓度为0.1mol/L,1L该溶液中含有0.1mol氢氧根离子;
D.偏铝酸钠溶液中的溶剂水中也含有氧原子.
解答:
解:A.11g由D和18O所组成的水物质的量为:
=0.5mol,0.5mol该水中含有5.5mol中子,所含的中子数为5.5NA,故A错误;
B.8g氧气的物质的量为:
=0.25mol,0.25mol氧气中含有电子的物质的量为:0.25mol×16=4mol,含有4NA个电子,故B正确;
C.25℃时,pH=13的1L Ba(OH)2溶液中含有氢氧根离子的物质的量为:1mol/L×0.1mol/L=0.1mol,含有的氢氧根离子数为0.1NA,故C错误;
D.1L 1mol/L的NaAlO2水溶液中含有溶质偏铝酸钠1mol,1mol偏铝酸钠中含有2mol氧原子,由于水中含有氧原子,所以该溶液中含有的氧原子大于2mol,溶液中含有的氧原子数大于2NA,故D错误;
故选B.
| 11g |
| 22g/mol |
B.8g氧气的物质的量为:
| 8g |
| 32g/mol |
C.25℃时,pH=13的1L Ba(OH)2溶液中含有氢氧根离子的物质的量为:1mol/L×0.1mol/L=0.1mol,含有的氢氧根离子数为0.1NA,故C错误;
D.1L 1mol/L的NaAlO2水溶液中含有溶质偏铝酸钠1mol,1mol偏铝酸钠中含有2mol氧原子,由于水中含有氧原子,所以该溶液中含有的氧原子大于2mol,溶液中含有的氧原子数大于2NA,故D错误;
故选B.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系.有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
有关晶体结构的叙述中,错误的是( )


| A、金刚石的正四面体网状结构中最小的环上有6个碳原子 |
| B、如图在面心立方密堆积的金属晶体中,每个金属原子周围紧邻的有12个金属原子 |
| C、在氯化钠晶体中,每个氯离子周围都紧邻8个钠离子 |
| D、分子晶体干冰也是面心立方晶胞,每个晶胞平均含有4个CO2分子 |
 具有显著抗癌活性的10-羟基喜树碱的结构如图所示,下列关于10-羟基喜树碱的说法正确的是( )
具有显著抗癌活性的10-羟基喜树碱的结构如图所示,下列关于10-羟基喜树碱的说法正确的是( )| A、10-羟基喜树碱属于芳香烃 |
| B、分子式为:C20H16N2O5 |
| C、不能发生酯化反应 |
| D、一定条件下,1mol该物质可与9mol H2发生加成反应 |
在11g由D和18O组成的水中,含中子数为(NA表示阿伏加德罗常数)( )
| A、NA |
| B、2NA |
| C、6NA |
| D、10NA |
某烃的结构简式为 ,它可能具有的性质是( )
,它可能具有的性质是( )
 ,它可能具有的性质是( )
,它可能具有的性质是( )| A、能使溴水褪色,但不能使酸性KMnO4溶液褪色 |
| B、与足量氢气反应生成苯乙烷 |
C、能发生加聚反应,生成物可用表示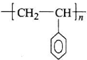 |
| D、易溶于水,也易溶于有机溶剂 |
下列叙述不正确的是( )
| A、金刚石、碳化硅、晶体硅的熔点依次降低 | |||||||
| B、CaO晶体结构与NaCl晶体结构相似,每个CaO晶胞中含有4个Ca2+和4个O2- | |||||||
C、设NaCl的摩尔质量为M g?mol-1,NaCl的密度为ρ g?cm-3,阿伏加德罗常数为NA mol-1,在NaCl晶体中,两个距离最近的Cl-中心间的距离为
| |||||||
| D、X、Y可形成立方晶体结构的化合物,其晶胞中X占据所有棱的中心,Y位于顶角位置,则该晶体的组成式为XY3 |
下列说法中,正确的是( )
| A、在常温常压下,22.4 L 氧气所含的分子数目为NA |
| B、18g水含有电子数为8NA |
| C、在1L水中溶解5.85g NaCl,即可配制得0.1mol/L的NaCl溶液 |
| D、1 mol 钠作为还原剂所提供的电子数为NA |
下列现象或事实可用同一原理解释的是( )
| A、氯水和二氧化硫使品红溶液褪色 |
| B、亚硫酸钠和水玻璃长期暴露在空气中变质 |
| C、稀硝酸和三氯化铁溶液使KI-淀粉试纸变蓝 |
| D、浓盐酸和浓硫酸长期暴露在空气中浓度变小 |