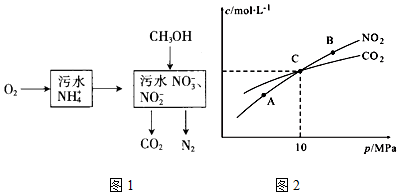
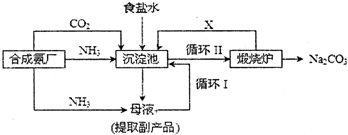
��Ŀ����
4��25��ʱ����֪��Ӧ��CO2��g��+H2��g��?CO ��g��+H2O ��g����H=+41kJ/mol���ش��������⣺��1���÷�Ӧ�������ȷ�Ӧ�������ȡ������ȡ������ж������ǡ�H��0
��2�����жϸ÷�Ӧ�Ƿ��Ѵ�ƽ��״̬��������ad������ţ���
a�����������n��CO������ b��v������CO2��=v������CO��
c��������������ʵ������� d����������ɫ���� e��c��CO��=c��H2O��
��3��һ�������µ��ܱ������У���Ӧ�ﵽƽ�⣬Ҫ���CO2��ת���ʣ����Բ�ȡ�Ĵ�ʩ��bd������ţ���
a������ϵ��ͨ��CO2 b�������¶�
c������ϵ��ͨ��������� d������ϵ��ͨ��H2 e���������
��4��25��ʱ����֪��2C��ʯī��+O2 ��g��=2CO��g����H1=-222kJ/mol
H2��g��+$\frac{1}{2}$O2��g��=H2O ��g����H2=-242kJ/mol
���������Ϣ��д��ʯī��������Ӧ����1mol CO2���Ȼ�ѧ����ʽC��ʯī��+O2��g��=CO2��g����H=-394 kJ/mol��
���� ��1������CO2��g��+H2��g��?CO ��g��+H2O ��g����H=+41kJ/mol����H��0Ϊ���ȷ�Ӧ��
��2����ѧƽ���־�����淴Ӧ������ͬ������ֺ������ֲ��䣬���ɴ�������һЩ������Ҳ���䣬�Դ˽��
��3��Ҫ���CO2��ת���ʣ�Ӧʹƽ��������Ӧ����ϻ�ѧƽ���ƶ�ԭ��������
��4����2C��ʯī��+O2��g��=2CO��g����H1=-222kJ/mol��
��H2��g��+$\frac{1}{2}$O2��g��=H2O ��g����H2=-242kJ/mol��
��CO2��g��+H2��g��?CO ��g��+H2O ��g����H=+41kJ/mol��
���ݸ�˹���ɣ��١�$\frac{1}{2}$+��-�ۼ���õ���
��� �⣺��1����ΪCO2��g��+H2��g��?CO ��g��+H2O ��g����H=+41kJ/mol����H��0����÷�Ӧ����Ϊ���ȷ�Ӧ���ʴ�Ϊ�����ȣ���H��0��
��2��a���淴Ӧ����CO��Ũ�������������n��CO�����䣬˵����Ӧ����ƽ�⣬��a��ȷ��
b��v������CO2��=v������CO��������ָ������Ӧ��������˵����Ӧ����ƽ�⣬��b����
c����Ϊ��Ӧǰ����������ʵ������䣬���Ի�����������ʵ���һֱ���䣬����˵����Ӧ����ƽ�⣬��c����
d����������ɫ���䣬˵��������Ũ�Ȳ��䣬˵����Ӧ����ƽ�⣬��d��ȷ��
e��c��CO��=c��H2O��ʱ���ܴ���ƽ��״̬�����ܲ�����ƽ��״̬���뷴Ӧ�������йأ��������̼��ת�����йأ���e����
��ѡ��ad��
��3��a������ϵ��ͨ��CO2����Ȼƽ��������Ӧ�����ƶ�������Ϊ���ӵ���CO2������CO2ת���ʼ�С���ʴ���
b�����ڷ�Ӧ���ȣ������¶�ƽ��������Ӧ�����ƶ���CO2ת����������ȷ��
c����Ϊһ�������µ��ܱ������У�����ϵ��ͨ��������壬ƽ�ⲻ�ƶ�������CO2ת���ʲ��䣬�ʴ���
d������ϵ��ͨ��H2��ƽ��������Ӧ�����ƶ���CO2ת����������ȷ��
e�����������ƽ�ⲻ�ƶ�������CO2ת���ʲ��䣬�ʴ���
�ʴ�Ϊ��bd��
��4����2C��ʯī��+O2��g��=2CO��g����H1=-222kJ/mol��
��H2��g��+$\frac{1}{2}$O2��g��=H2O ��g����H2=-242kJ/mol��
��CO2��g��+H2��g��?CO ��g��+H2O ��g����H=+41kJ/mol��
���ݸ�˹���ɣ��١�$\frac{1}{2}$+��-�۵�C��ʯī��+O2��g��=CO2��g����H=-222 kJ/mol��$\frac{1}{2}$-242 kJ/mol-41kJ/mol=-394 kJ/mol��
�ʴ�Ϊ��C��ʯī��+O2��g��=CO2��g����H=-394 kJ/mol��
���� ���⿼���˸�˹���ɵļ���Ӧ�ã���ѧƽ���Ӱ�����ط�������ƽ��״̬���жϵȣ���Ŀ�Ѷ��еȣ�

 ��У����ϵ�д�
��У����ϵ�д���1���жϷ�Ӧ�ﵽƽ��״̬�������ǣ�����ĸ��ţ���ͬ��CDE��
A������CH3OH������������CO���������
B�����������ܶȲ���
C����������ƽ����Է�����������
D��CH3OH��CO��H2��Ũ�ȶ����ٷ����仯
E�������������ѹǿ���ٸı�
��2�������������Ƿ�Ӧ�ڲ�ͬ�¶��µĻ�ѧƽ�ⳣ����K����
| �¶� | 250�� | 300�� | 350�� |
| K | 2.041 | 0.270 | 0.012 |
���ɱ��������жϸ÷�Ӧ�ġ�H��0�����������=����������
��ij�¶��£���2mol CO��6mol H2����2L���ܱ������У�5minʱ�ﵽƽ�⣬���c��CO��=0.2mol/L����CO��ת����Ϊ80%����ʱ���¶�Ϊ250�棬��0��5min�ڣ���H2��ʾ��ƽ����Ӧ����Ϊ0.32mol•L-1•min-1��ƽ��ʱCH3OH��Ũ��Ϊ0.8mol•L-1•
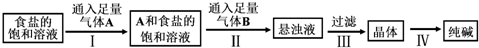
| A�� | ����A��NH3������B��CO2 | |
| B�� | �����Ƽ�Ĺ��չ�����Ӧ���������ܽ�ȵIJ��� | |
| C�� | ��III�������õ�����Ҫ�����������ձ���©���������� | |
| D�� | �ڢ�����������Ҫ�������ܽ⡢�������ᾧ |
| A�� | 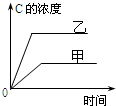 �о������¶ȶԷ�Ӧ��Ӱ�죬���ҵ��¶Ƚϸ� | |
| B�� | 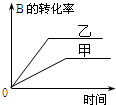 �о�����ѹǿ�Է�Ӧ��Ӱ�죬�Ҽ�ѹǿ�ϸ� | |
| C�� | 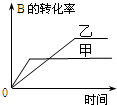 �о������¶ȶԷ�Ӧ��Ӱ�죬���ҵ��¶Ƚϸ� | |
| D�� | 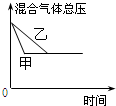 �о����Dz�ͬ�����Է�Ӧ��Ӱ�죬�Ҽ�ʹ�õĴ���Ч�ʽϸ� |
| t�� | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
��1���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK=$\frac{c��CO��c��{H}_{2}��}{c��{H}_{2}O��}$��
��2���÷�Ӧ���淴ӦΪ���ȷ�Ӧ��ѡ����ȡ����ȡ�����
��3�������жϸ÷�Ӧ�Ƿ�ﵽ��ѧƽ��״̬��������D��
A��������ѹǿ���� B�����������c��CO������
C��v����H2��=v����H2O�� D��c��H2��=c��CO��
��4��ij�¶��£�ƽ��Ũ�ȷ���c��CO��•c��H2��=c��H2O�������жϴ�ʱ���¶�Ϊ830�森
��5��Ϊ�����H2O��g����ת���ʣ����Բ�ȡ�Ĵ�ʩ�У��ټ�Сѹǿ�ڽ����¶ȣ�
| A�� | 0.1molKClO4 | B�� | 0.1molKClO3 | C�� | 0.1molKClO2 | D�� | 0.2molKClO |