题目内容
4.下列物质中氧元素的化合价正确的是( )| A. | H2O中氧元素的化合价为-l | B. | O2中氧元素的化合价为-2 | ||
| C. | NaOH中氧元素的化合价为-2 | D. | Na2O2中氧元素的化合价为-2 |
分析 根据在化合物中正负化合价代数和为零,单质中元素的化合价为零,据此解题.
解答 解:根据在化合物中元素正负化合价代数和为零,单质中元素的化合价为零,可知:
A.H2O中,氢元素为+1价,设H2O中氧元素的化合价是z,根据在化合物中正负化合价代数和为零,可得:(+1)×2+z=0,则z=-2价,故A错误;
B.氧气是由氧元素一种元素组成的,根据单质中元素的化合价为0,O2属于单质,故氧元素的化合价为0,故B错误;
C.NaOH中,钠元素显+1价,氢元素为+1价,设NaOH中氧元素的化合价是z,根据在化合物中正负化合价代数和为零,可得:(+1)×1+z+(+1)×1=0,则z=-2价,故C正确;
D.钠显+1价,设化合物Na2O2中O元素化合价为x,根据化合物中各元素化合价代数和为零,则
(+1)×2+2x=0
解得x=-1,故D错误.
故选C.
点评 本题考查了元素化合价的计算,抓住元素在化合物中正负化合价代数和为零、单质中元素化合价为零是解题本题的关键,难度不大.

练习册系列答案
相关题目
18.化学中常用图象直观地描述化学反应的进程或结果.下列图象描述正确的是( )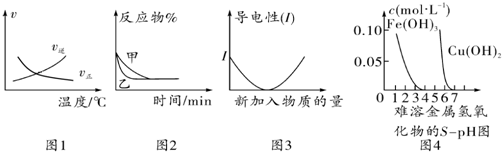

| A. | 根据图1可判断可逆反应“A2(g)+3B2(g)?2AB3(g)”的△H<0 | |
| B. | 图2可能表示压强对可逆反应 A(g)+2B(g)?3C(g)+D(s)的影响,乙的压强大 | |
| C. | 图3可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化 | |
| D. | 根据图4,若除去CuSO4溶液中的Fe3+可采用向溶液中加入适量Cu至pH在4左右 |
19.下列说法正确的是( )
| A. | 使用容量瓶、量筒、滴定管等仪器时,先用水洗后还需待装液润洗 | |
| B. | 洗涤沉淀的操作是将沉淀置于滤纸上(已放置在漏斗中),边用玻璃棒搅拌边加蒸馏水冲洗 | |
| C. | 为提升燃料电池的效率,通常可以用KNO3代替蒸馏水,同时作电极的碳棒先灼烧,然后投入到冷水中,反复3-5次 | |
| D. | 在制取乙酸乙酯的实验中,收集乙酸乙酯的试管中加的是饱和Na2CO3溶液,而且导管直接插入到饱和Na2CO3溶液 |
12.NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,将m1克锌加入到m2克20%的盐酸中放出nLH2,则转移电子数为$\frac{n{N}_{A}}{11.2}$ | |
| B. | 0.1mol/L的100mL H2SO3溶液中,含有的离子数约为0.03NA | |
| C. | 9gD2O中含有的电子数为5NA | |
| D. | 120g由NaHSO4和KHSO3组成的混合物中共含有3NA的阴阳离子 |
19.1923年以前,甲醇一般是用木材或其废料的分解蒸馏来生产的.现在工业上合成甲醇几乎全部采用一氧化碳或二氧化碳加压催化加氢的方法,工艺过程包括造气、合成净化、甲醇合成和粗甲醇精馏等工序.
已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:
(1)反应②是吸热(填“吸热”或“放热”)反应.
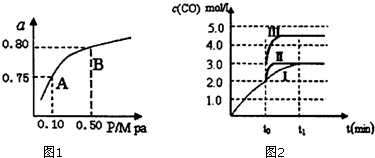
(2)某温度下反应①中H2的平衡转化率(a)与体系总压强(P)的关系如图1所示.则平衡状态由A变到B时,平衡常数K(A)=K(B)(填“>”、“<”或“=”).据反应①与②可推导出K1、K2与K3之间的关系,则K3=K1×K2(用K1、K2表示).
(3)在3L容积可变的密闭容器中发生反应②,已知c(CO)与反应时间t变化曲线Ⅰ如图2所示,若在t0时刻分别改变一个条件,则曲线Ⅰ可变为曲线Ⅱ和曲线Ⅲ.当曲线Ⅰ变为曲线Ⅱ时,改变的条件是加入催化剂.当曲线Ⅰ变为曲线Ⅲ时,改变的条件是将容器的体积(快速)压缩至2L.
(4)甲醇燃料电池有着广泛的用途,若采用铂为电极材料,两极上分别通入甲醇和氧气,以氢氧化钾溶液为电解质溶液,则该碱性燃料电池的负极反应式是CH3OH-6 e-+8 OH-=CO32-+6 H2O;
已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:
| 化学反应 | 平衡常数 | 温度℃ | |
| 500 | 800 | ||
| ①2H2(g)+CO(g)?CH3OH(g) | K1 | 2.5 | 0.15 |
| ②H2(g)+CO2(g)?H2O(g)+CO(g) | K2 | 1.0 | 2.50 |
| ③3H2(g)+CO2(g)?CH3OH(g)+H2O(g) | K3 | ||
(2)某温度下反应①中H2的平衡转化率(a)与体系总压强(P)的关系如图1所示.则平衡状态由A变到B时,平衡常数K(A)=K(B)(填“>”、“<”或“=”).据反应①与②可推导出K1、K2与K3之间的关系,则K3=K1×K2(用K1、K2表示).
(3)在3L容积可变的密闭容器中发生反应②,已知c(CO)与反应时间t变化曲线Ⅰ如图2所示,若在t0时刻分别改变一个条件,则曲线Ⅰ可变为曲线Ⅱ和曲线Ⅲ.当曲线Ⅰ变为曲线Ⅱ时,改变的条件是加入催化剂.当曲线Ⅰ变为曲线Ⅲ时,改变的条件是将容器的体积(快速)压缩至2L.
(4)甲醇燃料电池有着广泛的用途,若采用铂为电极材料,两极上分别通入甲醇和氧气,以氢氧化钾溶液为电解质溶液,则该碱性燃料电池的负极反应式是CH3OH-6 e-+8 OH-=CO32-+6 H2O;

13.足量的盐酸与下列物质反应,得到同温同压下气体体积相同的一组物质是( )
| A. | 等物质的量的Na2CO3和NaHCO3 | B. | 等物质的量的Al和CaCO3 | ||
| C. | 等质量的Na和Mg | D. | 等质量的Na2CO3和NaHCO3 |
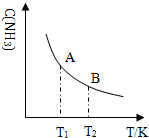
 开发利用清洁能源具有广阔的开发和应用前景,可减少污染解决雾霾问题.甲醇是一种可再生的清洁能源,一定条件下用CO和H2合成CH3OH:CO(g)+2H2 (g)?CH3OH(g)△H=-105kJ•mol-1.向体积为2L的密闭容器中充入2mol CO和4mol H2,测得不同温度下容器内的压强(P:kPa)随时间(min)的变化关系如下左图中Ⅰ、Ⅱ、Ⅲ曲线所示:
开发利用清洁能源具有广阔的开发和应用前景,可减少污染解决雾霾问题.甲醇是一种可再生的清洁能源,一定条件下用CO和H2合成CH3OH:CO(g)+2H2 (g)?CH3OH(g)△H=-105kJ•mol-1.向体积为2L的密闭容器中充入2mol CO和4mol H2,测得不同温度下容器内的压强(P:kPa)随时间(min)的变化关系如下左图中Ⅰ、Ⅱ、Ⅲ曲线所示: