题目内容
下列五种烃:①CH3CH2CH(CH3)2 ②CH3C(CH3)3 ③CH3CH2CH2CH2CH2CH3 ④CH3CH2CH2CH2CH3 ⑤CH3CH2CH2CH2CH2CH2CH3,其沸点按由高到低的顺序排列正确的是( )
| A、②①④③⑤ |
| B、②③④⑤① |
| C、⑤③④①② |
| D、④①②⑤③ |
考点:晶体熔沸点的比较,分子间作用力对物质的状态等方面的影响
专题:有机化学基础
分析:烃和烯烃的物理性质随着分子中碳原子数的递增呈规律性变化,沸点逐渐升高;碳原子数相同的烃,支链越多,熔、沸点越低.
解答:
解:烷烃和烯烃的物理性质随着分子中碳原子数的递增呈规律性变化,沸点逐渐升高;碳原子数相同的烃,支链越多,熔沸点越低.
⑤中碳原子都是7个,碳原子数最多,故沸点最高;
③中碳原子是6个,故沸点低于⑤;
①②④中碳原子都是5个,支链越少,沸点越高,故沸点:④>①>②;故沸点按由高到低的顺序排列是:⑤③④①②,
故选C.
⑤中碳原子都是7个,碳原子数最多,故沸点最高;
③中碳原子是6个,故沸点低于⑤;
①②④中碳原子都是5个,支链越少,沸点越高,故沸点:④>①>②;故沸点按由高到低的顺序排列是:⑤③④①②,
故选C.
点评:本题考查了烷烃沸点高低的判断,难度不大,明确碳原子数相同的烃,支链越多,熔沸点越低.

练习册系列答案
 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
下列叙述正确的是( )
| A、95℃纯水的pH<7,说明加热可导致水呈酸性 |
| B、pH=3的醋酸溶液,稀释10倍后pH=4 |
| C、0.2 mol?L-1的盐酸,与等体积水混合后pH=1 |
| D、25℃与60℃时,水的pH相等 |
设NA为阿伏加德罗常数,下列说法正确的是( )
| A、标况下,2.24L己烷所含分子数为0.1NA |
| B、1mol甲基中电子数为7NA |
| C、在反应KIO3+6HI═KI+3I2+3H2O中,每生成3mol I2转移的电子数为5NA |
| D、22.4L乙烯中C-H键数为4NA |
常温下,下列溶液的pH或微粒的物质的量浓度关系正确的是( )
| A、某溶液中由水电离出c(H+)=1×10-a mol?L-1,若a>7时,则该溶液pH一定为14-a |
| B、将标况下2.24L的CO2通入150mL 1mol?L-1NaOH溶液中充分反应后的溶液:2c(Na+)=3c(CO32-)+3c(HCO3-)+3c(H2CO3) |
| C、pH=3的二元弱酸H2R溶液与pH=11的NaOH溶液混合后,混合溶液的pH等于7,则反应后的混合液:2c(R2-)+c(HR-)>c(Na+) |
| D、0.2 mol?L-1的某一元酸HA溶液和0.1 mol?L-1NaOH溶液等体积混合后溶液pH大于7则反应后的混合液:c(OH-)+2c(A-)=c(H+)+2c(HA) |
近来据报道日本周边海洋发现丰富的稀土资源,下列有关稀土元素
Gd的说法正确的是( )
152 64 |
| A、质子数为152 |
| B、中子数为88 |
| C、质量数为216 |
| D、核外电子数为88 |
1mol甲烷和2mol氯气组成的混和气体,经较长时间的光照,最后得到的有机产物是( )
①CH3Cl;②CH2Cl2;③CHCl3;④CCl4.
①CH3Cl;②CH2Cl2;③CHCl3;④CCl4.
| A、只有① | B、只有② |
| C、只有①②③ | D、①②③④ |
能正确表示下列反应的离子方程式的是( )
| A、FeCl3溶液与Cu的反应:Cu+Fe3+═Cu2++Fe2+ | ||||
B、NH4HCO3溶于过量的NaOH溶液中:HCO
| ||||
C、稀H2SO4与Ba(OH)2溶液反应:Ba2++2OH-+2H++SO
| ||||
D、AgNO3溶液中加入过量的氨水:Ag++NH3?H2O═AgOH↓+NH
|
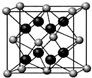 萤石(CaF2)晶体属于立方晶系如图所示,萤石中每个Ca2+被8个F-所包围,则每个F-周围最近距离的Ca2+数目为( )
萤石(CaF2)晶体属于立方晶系如图所示,萤石中每个Ca2+被8个F-所包围,则每个F-周围最近距离的Ca2+数目为( )