题目内容
某市进行学业水平考试实验操作考查,试题分别为:
Ⅰ.试验维生素C的化学性质(主要是还原性).
Ⅱ.葡萄糖与新制氢氧化铜的反应.
Ⅲ.配制一定物质的量浓度的氯化钠溶液.
(1)试题中设置了“评价与反思”,下列“评价与反思”不合理的是: .(填序号)
A.应该由监考老师去评价与反思
B.实验结论告诉我:维生素C原子应该密封保存
C.维生素C能使淀粉的碘溶液褪色
D.配制新制氢氧化铜时要将氢氧化钠与硫酸铜溶液等物质的量混合
E.实验Ⅲ中玻璃棒的作用是搅拌和引流
F.实验Ⅱ中的废水应该回收后再集中处理,不能直接倒入下水道
(2)实验Ⅲ中合理的实验操作顺序是:④ .(填序号)
①溶解,②计算和称量,③转移和洗涤,④查漏,⑤定容和摇匀.
(3)实验Ⅱ考查结束后,发现试管内壁附着一层红色固体.为了洗干净试管,某学习小组尝试往试管中加适量(3mL)稀硝酸,发现红色固体立即消失,溶液呈蓝色,则该反应的离子方程式为: .
Ⅰ.试验维生素C的化学性质(主要是还原性).
Ⅱ.葡萄糖与新制氢氧化铜的反应.
Ⅲ.配制一定物质的量浓度的氯化钠溶液.
(1)试题中设置了“评价与反思”,下列“评价与反思”不合理的是:
A.应该由监考老师去评价与反思
B.实验结论告诉我:维生素C原子应该密封保存
C.维生素C能使淀粉的碘溶液褪色
D.配制新制氢氧化铜时要将氢氧化钠与硫酸铜溶液等物质的量混合
E.实验Ⅲ中玻璃棒的作用是搅拌和引流
F.实验Ⅱ中的废水应该回收后再集中处理,不能直接倒入下水道
(2)实验Ⅲ中合理的实验操作顺序是:④
①溶解,②计算和称量,③转移和洗涤,④查漏,⑤定容和摇匀.
(3)实验Ⅱ考查结束后,发现试管内壁附着一层红色固体.为了洗干净试管,某学习小组尝试往试管中加适量(3mL)稀硝酸,发现红色固体立即消失,溶液呈蓝色,则该反应的离子方程式为:
考点:化学实验方案的评价,配制一定物质的量浓度的溶液
专题:实验评价题
分析:(1)A.评价反思要自我分析;
B.根据维生素C的性质分析;
C.根据维生素C和碘的反应判断;
D.配制新制氢氧化铜时氢氧化钠要过量;
E.玻璃棒有搅拌和引流作用;
F.废液要集中处理;
(2)根据实验步骤进行排序;
(3)氧化亚铜和稀硝酸反应生成硝酸铜、一氧化氮和水.
B.根据维生素C的性质分析;
C.根据维生素C和碘的反应判断;
D.配制新制氢氧化铜时氢氧化钠要过量;
E.玻璃棒有搅拌和引流作用;
F.废液要集中处理;
(2)根据实验步骤进行排序;
(3)氧化亚铜和稀硝酸反应生成硝酸铜、一氧化氮和水.
解答:
解:(1)A.应该先自我评价反思,故错误;
B.维生素C原子易被氧化,所以应该密封保存,故正确;
C.维生素C具有还原性,能被碘氧化,所以维生素C能使淀粉的碘溶液褪色,故正确;
D.配制的氢氧化铜悬浊液要呈碱性,所以配制新制氢氧化铜时氢氧化钠要过量,故错误;
E.配制溶液过程中,玻璃棒的作用是搅拌和引流,故正确;
F.实验Ⅱ中的废水含有重金属,不能直接倒入下水道,否则会污染环境,所以应该回收后再集中处理,故正确;
故选AD;
(2)一定物质的量浓度溶液的配制操作顺序是:查漏→计算、称量→溶解→转移和洗涤→定容和摇匀,
故答案为:②①③⑤;
(3)氧化亚铜和稀硝酸反应生成硝酸铜、一氧化氮和水,离子反应方程式为:3Cu2O+14H++2NO3-=6Cu2++2NO↑+7H2O,故答案为:3Cu2O+14H++2NO3-=6Cu2++2NO↑+7H2O.
B.维生素C原子易被氧化,所以应该密封保存,故正确;
C.维生素C具有还原性,能被碘氧化,所以维生素C能使淀粉的碘溶液褪色,故正确;
D.配制的氢氧化铜悬浊液要呈碱性,所以配制新制氢氧化铜时氢氧化钠要过量,故错误;
E.配制溶液过程中,玻璃棒的作用是搅拌和引流,故正确;
F.实验Ⅱ中的废水含有重金属,不能直接倒入下水道,否则会污染环境,所以应该回收后再集中处理,故正确;
故选AD;
(2)一定物质的量浓度溶液的配制操作顺序是:查漏→计算、称量→溶解→转移和洗涤→定容和摇匀,
故答案为:②①③⑤;
(3)氧化亚铜和稀硝酸反应生成硝酸铜、一氧化氮和水,离子反应方程式为:3Cu2O+14H++2NO3-=6Cu2++2NO↑+7H2O,故答案为:3Cu2O+14H++2NO3-=6Cu2++2NO↑+7H2O.
点评:本题考查了实验方案评价,明确实验原理是解本题关键,再结合一定物质的量浓度溶液的配制方法分析解答,注意氧化亚铜被稀硝酸氧化为硝酸铜,在一般的弱氧化性酸中能发生歧化反应.

练习册系列答案
相关题目
某无色溶液中放入铝片后有氢气产生,则下列离子可能大量存在的是( )
| A、Cu2+、Na+、SO42-、Cl- |
| B、K+、Na+、HCO3-、NO3- |
| C、Ba2+、Na+、OH-、Cl- |
| D、OH-、SO32-、Ca2+、Na+ |
原电池的电极名称不仅与电极材料的性质有关,也与电解质溶液有关.下列说法中不正确的是( )
| A、由Al、Cu、稀H2SO4组成原电池,其负极反应式为:Al→Al3++3e- |
| B、由Mg、Al、NaOH溶液组成原电池,其负极反应式为:Al+4OH→-Al(OH)4-+3e- |
| C、由Fe、Cu、FeCl3溶液组成原电池,其负极反应式为:Cu→Cu2++2e- |
| D、由Al、Cu、浓硝酸组成原电池,其负极反应式为:Cu→Cu2++2e- |
下列关于NH4Cl溶液的叙述中,正确的是( )
| A、c(NH4+)>c(Cl-) |
| B、c(NH4+)<c(Cl-) |
| C、c(NH4+)=c(Cl-) |
| D、不能确定c(NH4+)与c(Cl-)的大小 |
解释下列事实:
(1)饲养金鱼用的自来水须经日光曝晒或放置过夜后方能使用,其原因是 .
(2)常温下可用铁、铝制容器来盛装浓硫酸或浓硝酸,其原因是 .
(3)氨水呈弱碱性,其原因是(用离子方程式表示): .
(1)饲养金鱼用的自来水须经日光曝晒或放置过夜后方能使用,其原因是
(2)常温下可用铁、铝制容器来盛装浓硫酸或浓硝酸,其原因是
(3)氨水呈弱碱性,其原因是(用离子方程式表示):
下列各组中的两种物质无论以何种比例混合,其中氯元素的质量分数不变的是( )
| A、NaClO4和KClO3 |
| B、KClO和KCl |
| C、NaClO和NaCl |
| D、NaCl和KCl |
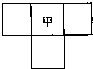 甲、乙、丙、丁四种短周期元素的位置如图(其中乙、丙、丁的位置未标出),已知四种元素的原子序数之和为36,乙的原子序数与甲、丁原子序数之和相等.
甲、乙、丙、丁四种短周期元素的位置如图(其中乙、丙、丁的位置未标出),已知四种元素的原子序数之和为36,乙的原子序数与甲、丁原子序数之和相等.