题目内容
现用18.4mol?L-1的浓硫酸来配制500mL 0.2mol?L-1的稀硫酸,可供选择的仪器有:①玻璃棒 ②烧杯 ③胶头滴管 ④量筒 ⑤容量瓶 ⑥托盘天平⑦药匙
(1)上述仪器在配制过程中不需要用到的是 .(填序号)
(2)计算所需浓硫酸的体积为 .现有①10mL ②50mL ③100mL三种规格的量筒,应当选用 .(填序号)
(3)实验中两次用到玻璃棒,其作用分别是: 、 .
(4)配制时,一般可分为以下几个步骤:
①量取 ②计算 ③稀释 ④摇匀 ⑤转移 ⑥洗涤 ⑦定容 ⑧冷却.其正确的操作顺序为 .(填序号)
(5)在配制过程中,下列操作可引起所配溶液浓度偏高的有 .(填序号)
①洗涤量取浓硫酸的量筒,并将洗涤液转移到容量瓶中.
②未等稀释后的硫酸溶液冷却至室温就转移到容量瓶中.
③转移前,容量瓶中含有少量蒸馏水.
④未洗涤稀释浓硫酸时用过的烧杯和玻璃棒.
⑤定容时,俯视刻度线.
(1)上述仪器在配制过程中不需要用到的是
(2)计算所需浓硫酸的体积为
(3)实验中两次用到玻璃棒,其作用分别是:
(4)配制时,一般可分为以下几个步骤:
①量取 ②计算 ③稀释 ④摇匀 ⑤转移 ⑥洗涤 ⑦定容 ⑧冷却.其正确的操作顺序为
(5)在配制过程中,下列操作可引起所配溶液浓度偏高的有
①洗涤量取浓硫酸的量筒,并将洗涤液转移到容量瓶中.
②未等稀释后的硫酸溶液冷却至室温就转移到容量瓶中.
③转移前,容量瓶中含有少量蒸馏水.
④未洗涤稀释浓硫酸时用过的烧杯和玻璃棒.
⑤定容时,俯视刻度线.
考点:配制一定物质的量浓度的溶液
专题:实验题
分析:(1)根据配制500mL 0.2mol?L-1的稀硫酸的仪器选择使用仪器,然后判断不需要的仪器;
(2)根据溶液稀释过程中溶质读到物质的量不变计算出需要浓硫酸的体积,根据计算结果判断量筒规格;
(3)根据配制过程中玻璃棒的作用进行解答;
(4)根据配制一定物质的量浓度的溶液的步骤进行排序;
(5)根据c=
可得,一定物质的量浓度溶液配制的误差都是由溶质的物质的量n和溶液的体积V引起的,误差分析时,关键要看配制过程中引起n和V怎样的变化:若n比理论值小,或V比理论值大时,都会使所配溶液浓度偏小;若n比理论值大,或V比理论值小时,都会使所配溶液浓度偏大.
(2)根据溶液稀释过程中溶质读到物质的量不变计算出需要浓硫酸的体积,根据计算结果判断量筒规格;
(3)根据配制过程中玻璃棒的作用进行解答;
(4)根据配制一定物质的量浓度的溶液的步骤进行排序;
(5)根据c=
| n |
| V |
解答:
解:(1)配制500mL 0.2mol?L-1的稀硫酸使用的仪器有:量筒、玻璃棒、烧杯、500mL容量瓶、胶头滴管,所以不需要的仪器为:⑥托盘天平⑦药匙,
故答案为:⑥⑦;
(2)500mL 0.2mol?L-1的稀硫酸中含有溶质硫酸的物质的量为:0.2mol?L-1×0.5L=0.1mol,需要18.4mol?L-1的浓硫酸的体积为:
≈0.054L=5.4mL,应该选用10mL量筒,
故答案为:5.4mL; ①;
(3)配制一定物质的量浓度的溶液过程中,稀释浓硫酸时使用玻璃棒搅拌,加速稀释过程;转移溶液时使用玻璃棒引流,避免液体流到容量瓶外面,
故答案为:搅拌;引流;
(4)配制一定物质的量浓度的溶液步骤为:计算、量取、稀释、冷却、转移、洗涤、定容、摇匀等,所以正确顺序为:②①③⑧⑤⑥⑦④,
故答案为:②①③⑧⑤⑥⑦④;
(5)①洗涤量取浓硫酸的量筒,并将洗涤液转移到容量瓶中,用于量取溶液的量筒不能洗涤,否则导致量取的液体体积偏大,根据c=
可得,配制的溶液浓度偏高,故①正确;
②未等稀释后的硫酸溶液冷却至室温就转移到容量瓶中,热的溶液体积偏大,冷却后溶液体积偏小,根据c=
可得,配制的溶液浓度偏高,故②正确;
③转移前,容量瓶中含有少量蒸馏水,对溶质的物质的量及溶液的体积没有影响,根据c=
可得,不影响配制结果,故③错误;
④未洗涤稀释浓硫酸时用过的烧杯和玻璃棒,导致配制的溶液中溶质的物质的量偏小,根据c=
可得,配制的溶液浓度偏低,故④错误;
⑤定容时,俯视刻度线,导致加入的蒸馏水体积偏小,根据c=
可得,配制的溶液浓度偏高,故⑤正确;
故答案为:①②⑤.
故答案为:⑥⑦;
(2)500mL 0.2mol?L-1的稀硫酸中含有溶质硫酸的物质的量为:0.2mol?L-1×0.5L=0.1mol,需要18.4mol?L-1的浓硫酸的体积为:
| 0.1mol |
| 18.4mol/L |
故答案为:5.4mL; ①;
(3)配制一定物质的量浓度的溶液过程中,稀释浓硫酸时使用玻璃棒搅拌,加速稀释过程;转移溶液时使用玻璃棒引流,避免液体流到容量瓶外面,
故答案为:搅拌;引流;
(4)配制一定物质的量浓度的溶液步骤为:计算、量取、稀释、冷却、转移、洗涤、定容、摇匀等,所以正确顺序为:②①③⑧⑤⑥⑦④,
故答案为:②①③⑧⑤⑥⑦④;
(5)①洗涤量取浓硫酸的量筒,并将洗涤液转移到容量瓶中,用于量取溶液的量筒不能洗涤,否则导致量取的液体体积偏大,根据c=
| n |
| V |
②未等稀释后的硫酸溶液冷却至室温就转移到容量瓶中,热的溶液体积偏大,冷却后溶液体积偏小,根据c=
| n |
| V |
③转移前,容量瓶中含有少量蒸馏水,对溶质的物质的量及溶液的体积没有影响,根据c=
| n |
| V |
④未洗涤稀释浓硫酸时用过的烧杯和玻璃棒,导致配制的溶液中溶质的物质的量偏小,根据c=
| n |
| V |
⑤定容时,俯视刻度线,导致加入的蒸馏水体积偏小,根据c=
| n |
| V |
故答案为:①②⑤.
点评:本题考查了配制一定物质的量浓度的溶液的方法,该题是中等难度的试题,试题基础性强,贴近高考,侧重对学生能力的培养和解题方法的指导和训练,有利于培养学生的逻辑思维能力和严谨的规范实验操作能力;该题的难点在于误差分析,注意明确误差分析的方法.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
在室温下,某溶液中由水电离出的H+浓度为1.0×10-13mol?L-1,则此溶液中一定不可能大量存在的离子组是( )
| A、Mg2+、NO3-、Cl-、Na+ |
| B、Al3+、SO42-、Cl-、K+ |
| C、Na+、Fe2+、SO42-、NO3- |
| D、S2-、SO32-、K+、Na+ |
常温下,下列溶液中各组离子一定大量共存的是( )
| A、使甲基橙呈红色的溶液中:Na+、AlO2-、NO3-、CO32- |
| B、c(ClO-)=1.0 mol?L-1溶液:Na+、SO32-、S2-、Cl- |
| C、含有0.1 mol?L-1 HCO3-的溶液:Na+、Fe3+、NO3-、C6H5O- |
| D、c(OH-)=0.1 mol?L-1的溶液:Na+、K+、CO32-、NO3- |
实验是化学研究的基础,关于下列各实验装置图的叙述中,正确的是( )
A、 可用于分离苯和硝基苯的混合物 |
B、 可用于吸收HCl气体.并防止倒吸 |
C、 可用于以NH4Cl为原料,实验室制取NH3 |
D、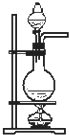 可用于实验室制取乙烯 |
为了同时对农作物施用含有N、P、K三种元素的化肥,对于给定的化肥:①KCl ②K2CO3 ③Ca(H2PO4)2 ④NH4Cl ⑤CO(NH2)2,不适合的组合是( )
| A、②③④ | B、①③④ |
| C、①③⑤ | D、①③④⑤ |
