题目内容
利用下列装置(部分仪器已省略),能顺利完成对应实验的是( )
A、 向容量瓶中转移溶液 |
B、 制氢氧化亚铁 |
C、 碳酸氢钠受 热分解 |
D、 蒸馏装置 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.转移液体时要防止液体外溅;
B.制备氢氧化亚铁时要防止氧化;
C.加热时要防止试管炸裂;
D.蒸馏时注意温度计位置以及冷凝水的进出方向.
B.制备氢氧化亚铁时要防止氧化;
C.加热时要防止试管炸裂;
D.蒸馏时注意温度计位置以及冷凝水的进出方向.
解答:
解:A.应用玻璃棒引流,防止液体流出,故A错误;
B.氢氧化亚铁易被氧化,胶头滴管应插入到液面以下,故B错误;
C.试管口应略向下倾斜,防止试管炸裂,故C错误;
D.温度计位置以及冷凝水的进出方向正确,可用于蒸馏操作,故D正确.
故选D.
B.氢氧化亚铁易被氧化,胶头滴管应插入到液面以下,故B错误;
C.试管口应略向下倾斜,防止试管炸裂,故C错误;
D.温度计位置以及冷凝水的进出方向正确,可用于蒸馏操作,故D正确.
故选D.
点评:本题考查较为综合,涉及溶液的配制、氢氧化亚铁的制备以及物质的分离、提纯等操作,侧重于学生的分析能力和实验能力的考查,为高考常见题型,注意把握物质的性质异同以及实验的严密性、可行性的评价,难度不大.

练习册系列答案
相关题目
能正确表示下列反应的离子方程式是( )
| A、氯气通入水中,溶液呈酸性:Cl2+H2O?2H++Cl-+ClO- |
| B、金属铝溶于氢氧化钠溶液:Al+2OH-═AlO2-+H2↑ |
| C、向明矾溶液中滴加Ba(OH)2溶液,达沉淀物质的量最大:2Al3++3SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4↓ |
| D、过量铁溶于稀硝酸:Fe+4H++NO3-═Fe3++NO↑+2H2O |
 某温度下,向一定体积0.10mol?L-1醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH[pOH=-lg(OH-)]与pH的变化关系如图所示,则( )
某温度下,向一定体积0.10mol?L-1醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH[pOH=-lg(OH-)]与pH的变化关系如图所示,则( )| A、在反应过程中P点水的电离程度最大 |
| B、M点和Q点溶液导电能力相同 |
| C、反应过程中一定存在:0.1mol?L-1+c(OH-)=c(Na+)+c(H+)+c(CH3COOH) |
| D、Q点对应的溶质可能有三种可能:①CH3COONa ②CH3COONa、CH3COOH ③CH3COONa、NaOH |
下列有关实验装置进行的相应实验,能达到实验目的是( )
A、 利用此图装置可从氯化铁溶液中直接蒸发结晶获得氯化铁晶体 |
B、 利用此图装置可分离石油,得到汽油、煤油和柴油等各种馏分 |
C、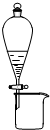 利用此图装置可分离CH3CH2OH和CH3COOC2H5混合液 |
D、 利用此图装置可进行酸碱中和滴定 |
近年来,我市部分出租车使用压缩天然气和液化石油气代替汽油作燃料,下列关于此项举措对环境的影响说法正确的是( )
| A、可以有效控制白色污染 |
| B、可能导致酸雨增多 |
| C、可能加剧温室效应 |
| D、可以有效减少大气污染 |
设NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A、标准状况下,11.2L乙醇所含的羟基数为0.5 NA |
| B、常温常压下,4.6g NO2和N2O4混合物中含有的原子总数为0.3 NA |
| C、1mol Cl2发生反应时,转移的电子数一定是2NA |
| D、常温下,1L pH=12的Ba(OH)2溶液中含有的OH-离子数为0.02NA |
常温下,下列溶液中,有关微粒的物质的量浓度关系正确的是( )
| A、0.1mol?L-1 (NH4)2Fe(SO4)2溶液:c(NH4+)>c(SO42- )>c(Fe2+)>c(H+) |
| B、0.1mol?L-1 Na2CO3溶液:c(Na+)+c(H+)=c(CO32-)+c(HCO3-)+c(OH-) |
| C、0.1mol?L-1 NaHCO3溶液:c(H+)+2c(H2CO3)=c(OH-)+c(CO32-) |
| D、0.01mol?L-1NaOH溶液与等体积pH=2的醋酸混合后的溶液中:c (CH3COO-)>c (Na+)>c (H+)>c (OH-) |
