题目内容
7.某有机物B的分子式为C4H4O4,其结构简式为HOOCCH=CHCOOH(1)B分子所含官能团的名称是羧基、碳碳双键.
(2)1mol C4H4O4完全燃烧需消耗O23 mol.
(3)与B的具有相同官能团的同分异构体的结构简式是(HOOC)2C=CH2.
分析 有机物结构简式为HOOCCH=CHCOOH,含-COOH、
解答 解:(1)含有的官能团有羧基、碳碳双键,故答案为:羧基;碳碳双键;
(2)由分子式C4H4O4可知,1mol C4H4O4完全燃烧需消耗O2的物质的量为(4+$\frac{4}{4}$-$\frac{4}{2}$)mol=3mol,故答案为:3;
(3)与B的具有相同官能团的同分异构体含有羧基、碳碳双键,为(HOOC)2C=CH2,故答案为:(HOOC)2C=CH2.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重烯烃、-COOH的性质及检验的考查,题目难度不大.

练习册系列答案
相关题目
17.下列说法不正确的是( )
| A. | 含有羟基的化合物不一定属于醇类 | |
| B. | 代表醇类的官能团是与链烃基相连的羟基 | |
| C. | 酚类和醇类具有相同的官能团 | |
| D. | 分子内有苯环和羟基的化合物一定是酚类 |
15.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 将1 mol Cl2通入H20中,生成NA个HC10分子 | |
| B. | 32 g硫在空气中燃烧,该反应转移6NA个电子 | |
| C. | 标准状况下,2.24 L CO气体中约含有1.4NA个质子 | |
| D. | 室温下,1 L pH=3的H2S04,溶液中,H2S04,电离出2×10 -3 NA个H+ |
12.下列物质之间的反应,一定不能生成盐的是( )
| A. | 酸性氧化物与碱反应 | B. | 碱性氧化物与酸反应 | ||
| C. | 单质与化合物的置换反应 | D. | 金属与氧气化合 |
16.有A、B、C、D、E五种前四周期元素,其元素特征信息如表:
回答下列问题:
(1)元素C在周期表中的位置为第3周期ⅠA族.
(2)B基态原子的核外电子排布图 ;E基态原子的电子排布式1s22s22p63s23p63d54s1.
;E基态原子的电子排布式1s22s22p63s23p63d54s1.
(3)写出化合物A2B2的电子式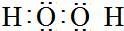 .
.
(4)D的氢氧化物与化合物CBA反应的离子方程式Al(OH)3+OH-=AlO2-+2H2O.
(5)B与C(碳)、N(氮)相比,第一电离能由大到小的顺序为N>O>C.
| 元素编号 | 元素特征信息 |
| A | 其单质是密度最小的物质 |
| B | 阴离子带两个单位负电荷,单质是空气的主要成分之一 |
| C | 其阳离子与B的阴离子有相同的电子层结构,电离能(I)数据依次为:I1=490kJ/mol-1,I2=4562kJ/mol-1,I3=6912kJ/mol-1… |
| D | 其氢氧化物和氧化物都有两性,与C同周期 |
| E | 在第四周期元素原子中,其所含不成对电子数最多 |
(1)元素C在周期表中的位置为第3周期ⅠA族.
(2)B基态原子的核外电子排布图
 ;E基态原子的电子排布式1s22s22p63s23p63d54s1.
;E基态原子的电子排布式1s22s22p63s23p63d54s1.(3)写出化合物A2B2的电子式
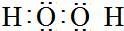 .
.(4)D的氢氧化物与化合物CBA反应的离子方程式Al(OH)3+OH-=AlO2-+2H2O.
(5)B与C(碳)、N(氮)相比,第一电离能由大到小的顺序为N>O>C.
17.下列微粒中:①12Mg2+ ②Na2-③ ④O2-,核外电子总数相同的是( )
④O2-,核外电子总数相同的是( )
 ④O2-,核外电子总数相同的是( )
④O2-,核外电子总数相同的是( )| A. | ②③④ | B. | ①②④ | C. | ①②③ | D. | ①③④ |
 已知A、B、C、D、E五种元素的原子序数依次递增,A、B、C、D位于短周期.A位于周期表的s区,其原子中电子层数和未成对电子数相同;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子最外层电子数是次外层电子数的3倍.E有“生物金属”之称,E4+和氩原子的核外电子排布相同.
已知A、B、C、D、E五种元素的原子序数依次递增,A、B、C、D位于短周期.A位于周期表的s区,其原子中电子层数和未成对电子数相同;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子最外层电子数是次外层电子数的3倍.E有“生物金属”之称,E4+和氩原子的核外电子排布相同.