��Ŀ����
18����һ���ݻ�������ܱ������У�������Ӧ��2NO��g��+O2��g���T2NO2��g����1����n��NO����n��O2��=4��1ʱ��O2��ת������ʱ��ı仯��ϵ��ͼ1��ʾ��
��A����淴Ӧ����v�� ��O2��С��B�������Ӧ����v����O2��������ڡ�����С�ڡ����ڡ�����
��NO��ƽ��ת����Ϊ30%�����ﵽB���������������4��1����ЩNO�� O2�����ﵽ��ƽ��ʱ����NO�İٷֺ���С��B��NO�İٷֺ���������ڡ�����С�ڡ����ڡ�����
�۵���B������й�ϵ��ȷ����ABCD
A��������������ɫ���ٱ仯 B��v����NO��=2v����O2��
C������ƽ��Ħ�������ڴ������´ﵽ��� D�������������ܶȲ��ٱ仯
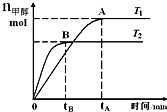
��2����ͼ2�г��ֵ��������ʶ�Ϊ���壬����ͼ2�����Ʋ⣺4NO��g��+3O2��g���T2N2O5��g����H=-787kJ/mol
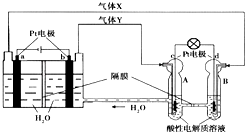
��3�������¶ȣ�NO2��g����ת��ΪN2O4��g������N2O4��O2������NaNO3��ɵ�ȼ�ϵ��װ����ͼ3��ʾ����ʹ�ù�����ʯīI�缫��Ӧ����һ��������Y��YΪN2O5���й�ʯīI�缫��Ӧʽ�ɱ�ʾΪ��N2O4+2NO3--2e-=2N2O5��
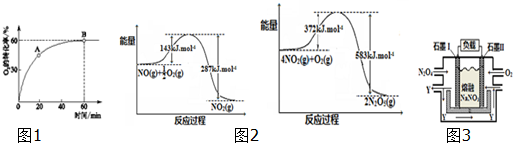
���� ��1����A��B��������ת��������˵����Ӧ������У�
��ƽ��ʱѹǿת����Ϊ60%����n��NO����n��O2��=4��1ʱ��NOΪ4��O2Ϊ1����ϻ�ѧƽ�����м���õ������ﵽB���������������4��1����ЩNO�� O2���൱���е�����������ѹǿ��ƽ��������У�
�۵���B�㼴�ﵽƽ��״̬�����淴Ӧ������ͬ������ֺ������ֲ��䣻
��2������ͼ��ֱ�д����Ӧ��Ӧ���Ȼ�ѧ����ʽ����ϸ�˹���ɼ���4NO��g��+3O2��g���T2N2O5��g����Ӧ���ʱ䣻
��3��ȼ��ԭ����У�������ȼ��ʧ���ӷ���������Ӧ���ȸ��ݻ��ϼ��ж�����������N2O5�ĵ缫���ٸ������ӵķŵ�˳��д���缫��Ӧʽ��
��� �⣺��1����A��B��������ת��������˵����Ӧ������У�A����淴Ӧ����v�� ��O2��С��B�������Ӧ����v����O2����
�ʴ�Ϊ��С�ڣ�
��ƽ��ʱѹǿת����Ϊ60%����n��NO����n��O2��=4��1ʱ��NOΪ4��O2Ϊ1����ת��������Ϊ0.6����ϻ�ѧƽ�����м��㣬
2NO��g��+O2��g���T2NO2��g��
��ʼ�� 4 1 0
�仯�� 1.2 0.6 1.2
ƽ���� 2.8 0.4 1.2
NO��ƽ��ת����$\frac{1.2}{4}$��100%=30%��
���ﵽB���������������4��1����ЩNO�� O2���൱���е�����������ѹǿ��ƽ��������У�һ�������ٷֺ�����С��NO�İٷֺ���С��B��NO�İٷֺ�����
�ʴ�Ϊ��30%��С�ڣ�
��2NO��g��+O2��g���T2NO2��g����Ӧ������������еķ��ȷ�Ӧ��
A��������������ɫ���ٱ仯��˵����������Ũ�Ȳ��䣬��Ӧ�ﵽƽ��״̬����A��ȷ��
B������֮�ȵ��ڻ�ѧ����ʽ������֮��Ϊ����Ӧ����֮�ȣ���Ӧ�ﵽƽ��״̬v����NO��=2v����O2������B��ȷ��
C���ﵽƽ��״̬�����������䣬���ʵ������䣬����ƽ��Ħ�������ڴ������´ﵽ���C��ȷ��
D���ﵽƽ��״̬�������������ܶȲ��ٱ仯����D��ȷ��
�ʴ�Ϊ��ABCD��
��2���Ȼ�ѧ����ʽΪ��NO��g��+$\frac{1}{2}$O2��g��=NO2��g����H=143KJ/mol-287KJ/mol=-144KJ/mol��
��4NO2��g��+O2��g��=2N2O5��g����H=��372-583��KJ/mol=-211KJ/mol��
���ݸ�˹���ɼ���١�4+�ڵõ�4NO��g��+3O2��g���T2N2O5��g����H=-787kJ/mol��
�ʴ�Ϊ��-787kJ/mol��
��3����N2O4��O2������NaNO3��ɵ�ȼ�ϵ��װ������ͼ��ʾ����ʹ�ù�����ʯīI�缫��Ӧ����һ��������Y��N2O4�ڸ���ʧ���ӷ���������Ӧ��Ԫ�ػ��ϼ�����Ϊ+5�ۣ�������ΪN2O5����Ӧ�ĵ缫��ӦΪ��N2O4+2NO3--2e-=2 N2O5��
�ʴ�Ϊ��N2O5��N2O4+2NO3--2e-=2 N2O5��
���� ���⿼����ͼ���������ѧƽ��Ӱ�����ء�ƽ���־���жϡ�ƽ����㡢�Ȼ�ѧ����ʽ��д��ԭ���ԭ����֪ʶ�㣬���ջ����ǽ���ؼ�����Ŀ�Ѷ��еȣ�

| A�� | SO2ʹ��ɫʯ����Һ���ɫ��SO2+H2O�T2H++SO32- | |
| B�� | ���κ������¶����ܷ���Cu+H2SO4�TCuSO4+H2����Ӧ | |
| C�� | FeCl3��Na2O2��Cu2S��������Ӧ����ֱ�ӻ������� | |
| D�� | Ũ�Ⱥ������ͬ��FeBr2��FeI2��Һ�У��ֱ�ͨ���������������ȷ����û���Ӧ |
| ������ | K+��Ba2+��Fe2+��Al3+��Fe3+��Mg2+ |
| ������ | OH-��HCO3-��CO32-��Cl-��NO3-��SO42- |
�����й�˵������ȷ���ǣ�������
| A�� | �ɢ١����жϣ���Һ��һ�������е���������K+��Fe3+ | |
| B�� | ʵ����е����岻����ΪCO2 | |
| C�� | �ۺϷ����жϣ�ԭ��Һ������������Ϊ��Fe2+��Mg2+��Cl-��NO3-��SO42- | |
| D�� | ����ԭ��Һ�м�������������������Һ����ַ�Ӧ�������ˡ����������أ��õ��Ĺ�������Ϊ8g |
 �ں����ܱյ������У���CO�ϳɼ״���CO��g��+2H2��g��?CH3OH��g�����������������������£��о��¶ȶԷ�Ӧ��Ӱ�죬ʵ������ͼ��ʾ������˵����ȷ���ǣ�������
�ں����ܱյ������У���CO�ϳɼ״���CO��g��+2H2��g��?CH3OH��g�����������������������£��о��¶ȶԷ�Ӧ��Ӱ�죬ʵ������ͼ��ʾ������˵����ȷ���ǣ�������| A�� | ����A��ķ�Ӧ��ϵ��T1�䵽T2���ﵽƽ��ʱ$\frac{n��{H}_{2}��}{n��C{H}_{3}OH��}$���� | |
| B�� | CO�ϳɼ״��ķ�ӦΪ���ȷ�Ӧ | |
| C�� | �÷�Ӧ��T1ʱ��ƽ�ⳣ����T2ʱ��С | |
| D�� | �÷�Ӧƽ�ⳣ���ɱ�ʾΪK=$\frac{c��C{H}_{3}OH��}{c��CO��c��{H}_{2}��}$ |
 ˮ�ĵ���ƽ��������ͼ��ʾ������A���ʾ25��ʱˮ�ĵ����ƽ��ʱ������Ũ�ȣ�B���ʾ100��ʱˮ�ĵ����ƽ��ʱ������Ũ�ȣ�������˵����ȷ���ǣ�������
ˮ�ĵ���ƽ��������ͼ��ʾ������A���ʾ25��ʱˮ�ĵ����ƽ��ʱ������Ũ�ȣ�B���ʾ100��ʱˮ�ĵ����ƽ��ʱ������Ũ�ȣ�������˵����ȷ���ǣ�������| A�� | �ı�����ʹ��ˮ��pHֵ��С����������ǿ | |
| B�� | 100��ʱij��Һ����ˮ���������c��H+��=1��10-11 mol•L-1�������Һ��pH������11��3 | |
| C�� | ��pH=9��Ba��OH��2��Һ��pH=4��ϡ�����ϣ�������100��ĺ��£������Һ��pH=7����Ba��OH��2��Һ������������Ϊ10��1 | |
| D�� | 100��ʱ��pHֵ��Ϊ8�Ĵ����ƺͰ�ˮ����Һ�У�ˮ�ĵ���̶�֮��Ϊ104��1 |
 �ռ�ʵ���ҡ��칬һ�š��Ĺ���ϵͳ������������ȼ�ϵ�أ�RFC����RFC��һ�ֽ�ˮ��⼼��������ȼ�ϵ�ؼ������ϵĿɳ���أ���ͼΪRFC����ԭ��ʾ��ͼ���й�˵����ȷ���ǣ�������
�ռ�ʵ���ҡ��칬һ�š��Ĺ���ϵͳ������������ȼ�ϵ�أ�RFC����RFC��һ�ֽ�ˮ��⼼��������ȼ�ϵ�ؼ������ϵĿɳ���أ���ͼΪRFC����ԭ��ʾ��ͼ���й�˵����ȷ���ǣ�������| A�� | ����0.1mol����ת��ʱ��a������1.12L O2������� | |
| B�� | b���Ϸ����ĵ缫��Ӧ�ǣ�2H++2e-�TH2�� | |
| C�� | d���Ϸ����ĵ缫��Ӧ�ǣ�O2+4H++4e-�T2H2O | |
| D�� | c���Ͻ��л�ԭ��Ӧ��B�е�H+����ͨ����Ĥ����A |
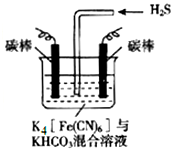 [Fe��CN��6]3-�ɽ���̬�������е�����ת��Ϊ�����õ���������ԭΪ[Fe��CN��6]4-����ҵ�ϳ�������ͼ��ʾ�ĵ��װ�ã�ͨ���⣬Ȼ��ͨ��H2S���Դ���������˵������ȷ���ǣ�������
[Fe��CN��6]3-�ɽ���̬�������е�����ת��Ϊ�����õ���������ԭΪ[Fe��CN��6]4-����ҵ�ϳ�������ͼ��ʾ�ĵ��װ�ã�ͨ���⣬Ȼ��ͨ��H2S���Դ���������˵������ȷ���ǣ�������| A�� | ������������Ҫ���ϲ���K4[Fe��CN��6]��KHCO3 | |
| B�� | ���ʱ������ӦʽΪ��2HCO3-+2 e-�TH2��+2CO32- | |
| C�� | ������������22.4L��״���µ�H2����ʱ����Һ����32gS�������ܽ���Բ��ƣ� | |
| D�� | ���ʱ������ӦʽΪ[Fe��CN��6]4--e-�T[Fe��CN��6]3- |
| A�� | �ռ��NaOH | B�� | ��ʯ�� CaO | C�� | ��� Na2CO3 | D�� | С�մ� NaHCO3 |