题目内容
1.某有机物的结构简式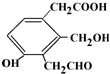 ,等物质的量的该物质,消耗Na、NaOH、NaHCO3的物质的量之比为3:2:1;消耗H2、Br2(水)的物质的量之比为2:1.
,等物质的量的该物质,消耗Na、NaOH、NaHCO3的物质的量之比为3:2:1;消耗H2、Br2(水)的物质的量之比为2:1.
分析 能与Na反应的有1个酚羟基、1个羧基和1个醇羟基;能与NaOH反应的有1个酚羟基和1个羧基;能与NaHCO3反应的只有1个羧基;能与氢气发生加成反应为苯环和碳碳双键,能与溴水反应的为酚羟基邻位的取代反应以及醛基的氧化反应,以此解答该题.
解答 解:能与Na反应的有1个酚羟基、1个羧基和1个醇羟基;
能与NaOH反应的有1个酚羟基和1个羧基;
能与NaHCO3反应的只有1个羧基,
则消耗Na、NaOH、NaHCO3的物质的量之比为3:2:1,
能与氢气发生加成反应为苯环和碳碳双键,则1mol有机物可与4mol氢气发生加成反应,能与溴水反应的为酚羟基邻位的取代反应以及醛基的氧化反应,则1mol有机物可与2mol溴发生反应,物质的量之比为2:1,
故答案为:3:2:1;2:1.
点评 本题考查有机物的结构与性质,为高频考点,注意把握官能团、性质的关系为解答的关键,熟悉苯酚、醇、酸的性质即可解答,题目难度中等.

练习册系列答案
相关题目
11.高氯酸是一种酸性极强的无机含氧酸,可用于制备高氯酸盐、人造金刚石提纯等方面.
查阅资料得到以下有关高氯酸的信息:
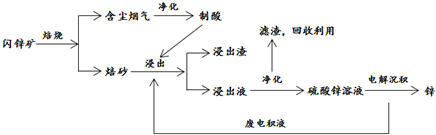
工业上生产高氯酸的同时还生产了亚氯酸钠,工业流程如图:

(1)操作①的名称是过滤.
(2)反应器Ⅰ中投料时需加入过量浓硫酸,请简述目的为了产物能得到HClO4而不是NaClO4.
(3)反应器Ⅱ中发生反应的离子方程式为4OH-+SO2+2ClO2=2ClO2-+SO42-+2H2O.
(4)某学习小组模拟工业流程图中的蒸馏过程,有液体流出时立即收集产品以获得HClO4纯品.请评价这一操作是否合理并说明理由不合理,因为水的沸点是100℃,HClO4的沸点是130℃,所以最先蒸馏流出的是水而不是HClO4.
(5)若想得到201kg的 HClO4纯品,至少需要NaClO3639kg.
(6)工业上也可用铂作阳极、铜作阴极电解盐酸制得高氯酸,在阳极区可得到20%的高氯酸.写出阳极的电极反应式(其中盐酸与高氯酸以化学式出现)4H2O+HCl-8e-=HClO4+8H+.
查阅资料得到以下有关高氯酸的信息:
| 名称 | 分子式 | 外观 | 沸点 |
| 高氯酸 | HClO4 | 无色液体 | 130℃ |

(1)操作①的名称是过滤.
(2)反应器Ⅰ中投料时需加入过量浓硫酸,请简述目的为了产物能得到HClO4而不是NaClO4.
(3)反应器Ⅱ中发生反应的离子方程式为4OH-+SO2+2ClO2=2ClO2-+SO42-+2H2O.
(4)某学习小组模拟工业流程图中的蒸馏过程,有液体流出时立即收集产品以获得HClO4纯品.请评价这一操作是否合理并说明理由不合理,因为水的沸点是100℃,HClO4的沸点是130℃,所以最先蒸馏流出的是水而不是HClO4.
(5)若想得到201kg的 HClO4纯品,至少需要NaClO3639kg.
(6)工业上也可用铂作阳极、铜作阴极电解盐酸制得高氯酸,在阳极区可得到20%的高氯酸.写出阳极的电极反应式(其中盐酸与高氯酸以化学式出现)4H2O+HCl-8e-=HClO4+8H+.
12.下列物质中存在顺反异构体的是( )
| A. | 1-氯丙烯 | B. | 丙烯 | C. | 2-甲基-2-丁烯 | D. | 1-丁烯 |
16.下列说法正确的是( )
| A. | 泡沫灭火器中将Al2(SO4)3与NaHCO3两溶液混合后,喷出大量泡沫,起到灭火作用 | |
| B. | KNO3、KClO3与单质S、C2H5OH混搭存放在同一库房间 | |
| C. | 包装用材料聚乙烯、聚氯乙烯等都属于烃 | |
| D. | 绿色化学的核心就是治理工业生产对环境产生的污染 |
13.下列各组物质,互称为同系物的一组是( )
| A. | O2和O3 | B. | CH3CH3和CH3CH2CH2CH3 | ||
| C. | H和D | D. | 正丁烷和异丁烷 |
10.下列各项在化学反应中一定发生变化的是( )
| A. | 元素种类 | B. | 原子数目 | C. | 化学键 | D. | 原子核 |
9.下列物质中既能发生水解反应又能发生消去反应,且消去反应的产物只有一种的是( )
| A. |  | B. |  | C. | CH3Cl | D. |  |