题目内容
5.有以下各组微粒或物质:A、正丁烷和异丁烷; B、金刚石、石墨和C60; C、冰和干冰; D、35Cl和37Cl; E、NO和NO2;F.甲烷和乙烷;其中,互为同分异构体的有A(填编号,以下同);互为同素异形体的有B.互为同位素的有D 互为同系物的有F.
分析 同分异构体:分子式相同、结构不同的化合物;
同素异形体:由相同元素组成的形态不同的单质;
同位素:质子数相同、中子数不同的同一元素的不同核素;
同系物:结构相似,分子组成上相差一个或若干个CH2的有机化合物.
解答 解:A、正丁烷和异丁烷的分子式相同,结构不同,互为同分异构体;
B、金刚石、石墨和C60;都是由碳元素组成的不同单质,互为同素异形体;
C、冰和干冰的成分分别是水、二氧化碳,是两种不同的物质;
D、35Cl和37Cl都是氯元素的不同核素,互为同位素;
E、NO和NO2是两种不同的物质;
F.甲烷和乙烷的结构相似,分子组成相差一个CH2,互为同系物;
互为同分异构体的有A,互为同素异形体的有B,互为同位素的有D,互为同系物的有F,
故答案为:A;B;D;F.
点评 本题考查“四同”比较,难度不大,侧重考查学生的辨别能力,选项多,要细心排查.

练习册系列答案
相关题目
15.下列关于热化学反应的描述中正确的是( )
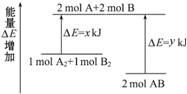

| A. | 已知H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ•mol-1,则H2SO4和Ba(OH)2反应的反应热△H=2×(-57.3)kJ•mol-1 | |
| B. | 燃料电池中将甲醇蒸气转化为氢气的热化学方程式是:CH3OH(g)+$\frac{1}{2}$O2(g)═CO2(g)+2H2(g)△H=-192.9 kJ•mol-1 则CH3OH(g)的燃烧热为192.9 kJ•mol-1 | |
| C. | 葡萄糖的燃烧热是2800 kJ•mol-1,则$\frac{1}{2}$C6H12O6(s)+3O2(g)═3CO2(g)+3H2O(l)△H=-1400 kJ•mol-1 | |
| D. | H2(g)的燃烧热是285.8 kJ•mol-1,则2H2O(g)═2H2(g)+O2(g)△H=+571.6 kJ•mol-1 |
16.下列有机物的系统命名正确的是( )
| A. | CH≡C-CH2CH3 丁炔 | B. | CH2═CH-CH=CH-CH3 1,3-二戊烯 | ||
| C. |  2-甲基丁烯 2-甲基丁烯 | D. |  1,2,3-三甲苯 1,2,3-三甲苯 |
13.化学反应速率是有单位的,下列表示的不是化学反应速率的单位的是( )
| A. | mol/L•s | B. | mol•(L•min)-1 | C. | mol/(L•min) | D. | mol•L-1•s-1 |
20.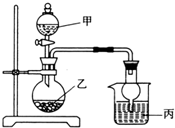 用如图所示装置进行实验(必要时可以进行加热),如表实验现象描述错误的是( )
用如图所示装置进行实验(必要时可以进行加热),如表实验现象描述错误的是( )
 用如图所示装置进行实验(必要时可以进行加热),如表实验现象描述错误的是( )
用如图所示装置进行实验(必要时可以进行加热),如表实验现象描述错误的是( ) | 实验 | 试剂甲 | 试剂乙 | 试剂丙 | 丙中的现象 |
| A | H2O2 | MnO2 | FeCl2溶液 | 溶液由浅绿色变为棕黄色 |
| B | 浓氨水 | CaO | AgNO3溶液 | 有白色沉淀生成 |
| C | H2SO4 | Na2SO3 | BaCl2溶液 | 有白色沉淀生成 |
| D | 浓HNO3 | Cu | NaHCO3溶液 | 有无色气体生成 |
| A. | A | B. | B | C. | C | D. | D |
10.下列化合物中,阳离子半径与阴离子半径比值最小的是( )
| A. | NaI | B. | NaBr | C. | MgI2 | D. | KBr |
17.以下能说明氯的非金属性比硫强的事实是( )
| A. | 氯的最高价为+7价而硫的最高价为+6价 | |
| B. | HCl的酸性比H2S的酸性强 | |
| C. | H2S能被Cl2氧化成硫单质 | |
| D. | HClO的氧化性比H2SO4的氧化性强 |
15.近年来高铁酸钾(K2FeO4)已经被广泛应用在水处理方面,高铁酸钾的氧化性超过高锰酸钾,是 一种集氧化、吸附、凝聚、杀菌的新型高效的多功能水处理剂.高铁酸钾在水处理过程中没有涉及到的过程是( )
| A. | 蛋白质的变性 | B. | 蛋白质的盐析 | C. | 胶体聚沉 | D. | 盐类水解 |