题目内容
17.某元素原子核外第二层是其他层电子数之和的2倍,则该元素的核电荷数为( )| A. | 4 | B. | 8 | C. | 12 | D. | 16 |
分析 由于K层容纳2个电子、L层容纳8个电子,结合某元素原子核外第二层是其他层电子数之和的2倍计算第三层容纳电子数,原子核电荷数等于核外电子数.
解答 解:由于K层容纳2个电子、L层容纳8个电子,某元素原子核外第二层是其他层电子数之和的2倍,则第三层容纳电子数为$\frac{8}{2}$-2=2,故该元素原子核外电子数为2+8+2=12,即该元素核电荷数为12,故选C.
点评 本题考查核外电子排布,关键是理解核外电子排布规律,有利于基础知识的巩固.

练习册系列答案
相关题目
7.下列事实中能说明亚硝酸(HNO2)是弱电解质的是( )
| A. | 0.1 mol•L-1的HNO2溶液中[H+]约为0.01 mol•L-1 | |
| B. | 用HNO2溶液做导电实验,灯泡很暗 | |
| C. | HNO2溶液不与Na2SO4溶液反应 | |
| D. | HNO2能与NaOH溶液发生中和反应 |
8.下列实验操作中,正确的是( )
| A. | 为了使过滤速度加快,可用玻璃棒在过滤器中轻轻搅拌,加速液体流动 | |
| B. | 燃着的酒精灯打翻失火,应立即用水浇灭 | |
| C. | 为加速固体物质的溶解,可采用粉碎、振荡、搅拌、加热等方法 | |
| D. | 为增大气体物质的溶解度,常采用搅拌、加热等措施 |
5.下列离子方程式书写不正确的是( )
| A. | 往NaOH溶液中通入过量CO2:CO2+OH-═HCO3- | |
| B. | 往水玻璃中加入盐酸:SiO32-+2H+═H2SiO3↓ | |
| C. | 石英砂与烧碱反应制水玻璃:SiO2+2OH-═SiO32-+H2O | |
| D. | 往水玻璃中通入CO2:Na2SiO3+H2O+CO2═H2SiO3+2Na++CO32- |
12.下列叙述正确的是 ( )
| A. | 二氧化硫既有氧化性又有还原性,在空气中易被氧化为三氧化硫 | |
| B. | 标准状况下,每摩三氧化硫的体积约为2.24L | |
| C. | 二氧化硫、三氧化硫都是酸性氧化物 | |
| D. | 二氧化硫具有漂白性、三氧化硫具有氧化性 |
2.实验室制取氯气可以有以下途径,用化学方程式表示如下.若制取等质量的氯气,消耗盐酸最少的是( )
| A. | 8HCl+K2Cr2O7$\frac{\underline{\;\;△\;\;}}{\;}$2KCl+Cr2O3+3Cl2↑+4H2O | |
| B. | 16HCl+2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$2MnCl2+2KCl+5Cl2↑+8H2O | |
| C. | 4HCl+MnO2═MnCl2+Cl2↑+2H2O | |
| D. | 6HCl+KClO3═KCl+3Cl2↑+3H2O |
6.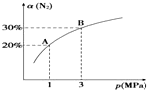 某温度下,对于反应N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol-1.N2的平衡转化率(α)与体系总压强(p)的关系如图所示.下列说法正确的是( )
某温度下,对于反应N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol-1.N2的平衡转化率(α)与体系总压强(p)的关系如图所示.下列说法正确的是( )
 某温度下,对于反应N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol-1.N2的平衡转化率(α)与体系总压强(p)的关系如图所示.下列说法正确的是( )
某温度下,对于反应N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol-1.N2的平衡转化率(α)与体系总压强(p)的关系如图所示.下列说法正确的是( )| A. | 将1 mol氮气、3 mol氢气,置于1 L密闭容器中发生反应,放出的热量为92.4 kJ | |
| B. | 平衡状态由A变到B时,平衡常数K(A)<K(B) | |
| C. | 上述反应在达到平衡后,增大压强,H2的转化率增大 | |
| D. | 升高温度,平衡向逆反应方向移动,说明逆反应速率增大,正反应速率减小 |