题目内容
18.在标准状况下,下列物质占体积最大的是( )| A. | 18g H2O | B. | 6.02×1023个氮分子 | ||
| C. | 44.8L HCl | D. | 6g氢气 |
分析 通常情况下,物质的量相差不大时,物质所占体积:气体>液态>固体;所以气体体积较大的为B、C、D;然后根据V=nVm计算出6g氢气和6.02×1023个氮分子的体积,根据计算结果进行比较即可.
解答 解:标准状况下,H2O为液态,所占体积都远远小于6.02×1023个氮分子、44.8LHCl、6gH2的体积;6.02×1023个氮分子的物质的量为:1mol,所以体积为22.4L,
标准状况下气体摩尔体积约为22.4L/mol,则6g H2在标准状况下的体积为:22.4L/mol×$\frac{6g}{2g/mol}$=67.2L,
则所占体积最大的为6g H2,
故选D.
点评 本题考查了物质的量的计算,题目难度不大,明确常见物质体积与所处状态的关系为解答关键,注意掌握物质的量与气体摩尔体积、摩尔质量等之间的关系,试题培养了学生的灵活应用能力.

练习册系列答案
相关题目
8.某合作学习小组讨论辨析以下说法:
①粗盐和酸雨 都是混合物;
②冰和干冰既是纯净物又是化合物;
③不锈钢和装修门窗使用的铝材料都是合金;
④盐酸和醋酸都属于电解质;
⑤纯碱和熟石灰都是碱;
⑥豆浆和雾都是胶体
上述说法正确的是( )
①粗盐和酸雨 都是混合物;
②冰和干冰既是纯净物又是化合物;
③不锈钢和装修门窗使用的铝材料都是合金;
④盐酸和醋酸都属于电解质;
⑤纯碱和熟石灰都是碱;
⑥豆浆和雾都是胶体
上述说法正确的是( )
| A. | ①②③⑥ | B. | ①②⑤⑥ | C. | ③⑤⑥④ | D. | ①③④⑥ |
9.Al、Mg混合物与适量的稀硫酸恰好完全反应,将溶液蒸干得固体质量比原固体增加了4.8g,则该混合物的物质的量可能为( )
| A. | 0.03 mol | B. | 0.04 mol | C. | 0.05 mol | D. | 0.06 mol |
6.已知重铬酸钾(K2Cr2O7)溶液中存在如下平衡:Cr2O72-(橙色)+H2O?2H++2CrO42- (黄色)
①向2mL 0.1mol•L-1 K2Cr2O7溶液中滴入3滴6mol•L-1NaOH溶液,溶液由橙色变为黄色;向所得溶液中再滴入5滴浓H2SO4,溶液由黄色变为橙色.
②向2mL 0.1mol•L-1 酸化的K2Cr2O7溶液中滴入适量(NH4)2Fe(SO4)2溶液,溶液由橙色变为绿色,发生反应:Cr2O72-+14H++6Fe2+?2Cr3+(绿色)+6Fe3++7H2O.下列分析正确的是( )
①向2mL 0.1mol•L-1 K2Cr2O7溶液中滴入3滴6mol•L-1NaOH溶液,溶液由橙色变为黄色;向所得溶液中再滴入5滴浓H2SO4,溶液由黄色变为橙色.
②向2mL 0.1mol•L-1 酸化的K2Cr2O7溶液中滴入适量(NH4)2Fe(SO4)2溶液,溶液由橙色变为绿色,发生反应:Cr2O72-+14H++6Fe2+?2Cr3+(绿色)+6Fe3++7H2O.下列分析正确的是( )
| A. | 实验①和②均能证明K2Cr2O7溶液中存在上述平衡 | |
| B. | 实验②能说明氧化性:Cr2O72->Fe3+ | |
| C. | CrO42- 和Fe2+在酸性溶液中可以大量共存 | |
| D. | 稀释K2Cr2O7溶液时,溶液中各离子浓度均减小 |
13.根据所学的知识和经验,判断下列变化在常温下的焓变,熵变及方向性,填表.
| 变化 | △H | △S | 方向性 |
| H2O(l)→H2O(g) | |||
| CaO(s)+SO2(g)═CaSO3(s) | |||
| 2Fe3+(aq)+Cu(s)═2Fe2+(aq)+Cu2+(aq) | |||
| NH4Cl(s)═HCl(g)+NH3(g) |
3.NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,22.4L四氯化碳的分子数约为NA | |
| B. | 2.4g金属镁变为镁离子时失去的电子数为0.2NA | |
| C. | 16gO2和O3的混合气体中所含的原子数为NA | |
| D. | 1mo1•L-1的A1C13溶液中,C1-离子的数目为3NA |
7.科学家正在研究利用催化技术将汽车尾气中的NO和CO转变成CO2和N2化学方程式如下:2NO(g)+2CO(g) $\frac{\underline{\;催化剂\;}}{\;}$2CO2(g)+N2(g)△H.
为了测定在某种催化剂作用下的反应速度,某温度下,在容积固体的容器内进行此反应,并用气体传感器测得不同时间的NO和CO浓度如表:
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
(1)在该反应的平衡常数的表达式K=$\frac{{{c^2}(C{O_2})•c({N_2})}}{{{c^2}(NO)•{c^2}(CO)}}$.
(2)该反应在此温度下能够自发进行,说明△H<0(填写“>”、“<”、“=”).
若只将反应条件改为绝热,平衡时NO的浓度将增大(填“增大”、“减小”、“不变”)
(3)前2s内的平均反应速率v(N21.88×10-4mol•L-1•s-1.
研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率.为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中.
(5)请在上表空格中填入剩余的实验条件数据.
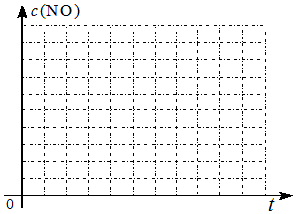
(6)请在给出的坐标图中,参考实验 I实验条件下混合气体中NO浓度随时间变化的趋势曲线图,画出 II、III条曲线图,并标明各条曲线的实验编号.
为了测定在某种催化剂作用下的反应速度,某温度下,在容积固体的容器内进行此反应,并用气体传感器测得不同时间的NO和CO浓度如表:
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/mol•L | 1.00×10-3 | 4.50×10-4 | 2.50×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO)/mol•L | 3.60×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
(1)在该反应的平衡常数的表达式K=$\frac{{{c^2}(C{O_2})•c({N_2})}}{{{c^2}(NO)•{c^2}(CO)}}$.
(2)该反应在此温度下能够自发进行,说明△H<0(填写“>”、“<”、“=”).
若只将反应条件改为绝热,平衡时NO的浓度将增大(填“增大”、“减小”、“不变”)
(3)前2s内的平均反应速率v(N21.88×10-4mol•L-1•s-1.
研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率.为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中.
| 实验编号 | T(℃) | NO初始浓度 (mol/L) | C O初始浓度 (mol/L) | 催化剂的比表面积 (m2/g) |
| 1 | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
| 2 | 124 | |||
| 3 | 350 | 124 |
(6)请在给出的坐标图中,参考实验 I实验条件下混合气体中NO浓度随时间变化的趋势曲线图,画出 II、III条曲线图,并标明各条曲线的实验编号.

8.已知R2+离子核外有a个电子,b个中子.表示R原子符号正确的是( )
| A. | ${\;}_{b}^{a}R$ | B. | ${\;}_{a-2}^{a+b-2}R$ | C. | ${\;}_{a+2}^{a+b+2}R$ | D. | ${\;}_{a-2}^{a+b}R$ |