��Ŀ����
4����֪X��Y��Z��W���Ƕ�����Ԫ�أ����ǵ�ԭ���������ε�����Xԭ�ӵĵ��Ӳ��������ĺ������������ȣ���Zԭ�ӵ������������Ǵ�����3����Y��Z�����γ�����������̬�����W����������X����������1��������˵��������ǣ�������| A�� | Y��Z�������һ��Y��Z��������Ϊ7��20�Ĺ��ۻ����� | |
| B�� | X��Y��Z�������һ���Σ�����X��Y��ZԪ��ԭ�Ӹ�����Ϊ4��2��3 | |
| C�� | Y��W��ɵĻ�������X��Z��ɵĻ����ﷴӦ������2�ּ������� | |
| D�� | ��X��Y��Z����Ԫ���е�����������ɵľ���10���ӵ�����2�� |
���� X��Y��Z���Ƕ�����Ԫ�أ����ǵ�ԭ���������ε�����Zԭ�ӵ������������Ǵ�����3������Z��OԪ�أ�Xԭ�ӵĵ��Ӳ��������ĺ������������ȣ���ԭ������С��Z������X��HԪ�أ�W����������X����������1����Wλ�ڢ�A�壬W��ԭ����������Y����WΪMgԪ�أ�Y��Z�����γ�����������̬�������Y��ԭ������С��OԪ�أ���Yֻ��Ϊֻ��ΪNԪ�أ��ݴ˽��н��
��� �⣺X��Y��Z���Ƕ�����Ԫ�أ����ǵ�ԭ���������ε�����Zԭ�ӵ������������Ǵ�����3������Z��OԪ�أ�Xԭ�ӵĵ��Ӳ��������ĺ������������ȣ���ԭ������С��Z������X��HԪ�أ�W����������X����������1����Wλ�ڢ�A�壬W��ԭ����������Y����WΪMgԪ�أ�Y��Z�����γ�����������̬�������Y��ԭ������С��OԪ�أ���Yֻ��Ϊֻ��ΪNԪ�أ�
A��Y��NԪ�أ�Z��OԪ�أ�Y��Z��������Ϊ7��20ʱ��ԭ�Ӹ�����=$\frac{7}{14}$��$\frac{20}{16}$=2��5���û�������N2O5����A��ȷ��
B��X��Y��Z�������һ���Σ���X��Y��ZԪ��ԭ�Ӹ���֮��Ϊ4��2��3ʱ��������NH4NO3����B��ȷ��
C��Y��W��ɵĻ�����Ϊ����þ��X��Z��ɵĻ�����Ϊˮ��˫��ˮ������þ��ˮ��Ӧ����������þ�Ͱ��������߶��Ǽ������ʣ���C��ȷ��
D����X��Y��Z����Ԫ���е�����������ɵľ���10���ӵ�����H2O��H3O+��NH3��NH4+����D����
��ѡD��
���� ���⿼��ԭ�ӽṹ��Ԫ�������ɵĹ�ϵ����Ŀ�Ѷ��еȣ���ȷ�ƶ�Ԫ���ǽⱾ��ؼ���ע����������ԭ�ӽṹ��Ԫ�������ɡ�Ԫ�����ڱ��Ĺ�ϵ������������ѧ���ķ������������Ӧ��������


| A�� | ���ܷ���������Ӧ | |
| B�� | 1mol ������������2molBr2��Ӧ | |
| C�� | 1mol ������������4mol NaOH��Ӧ | |
| D�� | ��NaHCO3��Na2CO3���ܷ�����Ӧ |
| A�� | 2.8 g��ϩ�ͱ�ϩ�Ļ������������̼ԭ����Ϊ0.2NA | |
| B�� | 0.5mol C3H8����������C-H���ۼ���Ϊ2NA | |
| C�� | ��״���£�1L������ȫȼ�������ɵ���̬����ķ�����Ϊ$\frac{7}{22.4}$NA | |
| D�� | 1mol̼������CH5+�����ĵ�����Ϊ11NA |
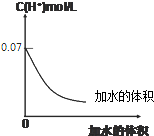
| A�� | ��ʹ��Һ��pH����1���������Һ���¶ȼ�ˮ����� | |
| B�� | ��ʹ��Һ��pH����1������Һϡ�͵�ԭ�����10�� | |
| C�� | 0.1 mol•L-1HIO3��Һϡ��10������Һ��c��H+����c��IO3-����c��HIO3�� | |
| D�� | ��ˮϡ������n��HIO3��+n����IO3-����С |
| A�� | Ϊ��ȥFeCl2��Һ��������FeCl3���ɼ���������ۣ��ٹ��� | |
| B�� | ������Al3+ˮ��������������ԵĽ��壬��������������ˮ�ľ��� | |
| C�� | Ϊ��ȥCO2��������HCl����ʹ��ͨ�����͵�Na2CO3��Һ | |
| D�� | Ϊ��ȥKCl��Һ��������MgCl2���ɼ�������KOH��Һ���ٹ��� |
| A�� | ˮ�����c��H+������=��=��=�� | |
| B�� | ���ڡ�����Һ��Ϻ�pH=7����������Һ��������ڣ��� | |
| C�� | ������Ģ١��ڡ�����Һ�ֱ����������۷�Ӧ������H2����������С | |
| D�� | ����Һ�м�ˮϡ�͵�ԭ����10������Һ��pH���ܣ��ۣ��ڣ��� |
| A�� | �ŵ�ʱ�������������� | |
| B�� | �ŵ�ʱ����Һ�е�BF4-ֻ�������ƶ� | |
| C�� | ���ʱ������������Һ��������ǿ | |
| D�� | ���ʱ�������ĵ缫��ӦʽΪPb2+-2e-=Pb |
CO2��g��+3H2��g��?CH3OH��g��+H2O��g����H=-46kJ•mol-1
��1���״������Ʒ�Ӧ��д����Ӧ�Ļ�ѧ����ʽ��2CH3OH+2Na��2CH3ONa+H2����
��2����֪H-H��C-O��C�T0��H-O���ļ�������Ϊ436kJ•mol-1��326kJ•mol-1��803kJ•mol-1��464kJ•mol-1����C-H���ļ���Ϊ414kJ•mol-1��
��3��һ�������£���n��CO2����n��H2��=1��1�Ļ����������Ⱥ����ܱ������з�����Ӧ��������ʵ����˵���÷�ӦCO2��g��+3H2��g��?CH3OH��g��+H2O��g���Ѵﵽƽ�����BCD������ĸ��
A�������������ܶȱ��ֲ��� B��CO2������������ֲ���
C���÷�Ӧ��ƽ�ⳣ�����ֲ��� D����������ƽ����Է�����������
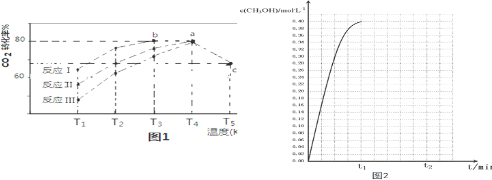
��4��һ�������£���2L�����ܱ������г���1.2molCO2��3.6molH2��������ӦCO2��g��+3H2��g��?CH3OH��g��+H2O��g�����ڲ�ͬ�������������£�����ͬʱ����CO2ת�������¶ȱ仯�����������ʾ�����ݱ������ݻ�����ͼ��T5ʱ��ͼ��c��ת����Ϊ66.67%����ת����$\frac{2}{3}$����
| ��ͬʱ����CO2ת���� | T1 | T2 | T3 | T4 | T5 |
| ��Ӧ�� | 65% | 77% | 80% | 80% | 66.67% |
| ��Ӧ�� | 56% | 67% | 76% | 80% | 66.67% |
| ��Ӧ�� | 48% | 62% | 72% | 80% | 66.67% |
��T3��b��v������=v���棩�����������������=����
��T4��a��ת���ʱ�T5��c���ԭ����T4��Ӧ�Ѿ��ﵽƽ�⣬�����¶ȵ�T5ƽ�����淴Ӧ�ƶ����Ӷ�ʹCO2��ת���ʽ��ͣ���
�����¶�ΪT5ʱ���÷�Ӧ��ƽ�ⳣ��K=3.70��