题目内容
19.①向Na2CO3溶液中通入氯气,可制得某种生产和生活中常用的漂白、消毒的物质,同时有NaHCO3生成,该反应的化学方程式是2Na2CO3+Cl2+H2O=NaClO+NaCl+2NaHCO3.②Na2CO3浓溶液中通入氯气时,可产生气体CO2和化合物NaClO3.反应的化学方程式为3Na2CO3+3Cl2=NaClO3+5NaCl+3CO2.
分析 ①氯气和水反应生成HCl和HClO,HCl和HClO与碳酸钠反应生成氯化钠、碳酸氢钠和次氯酸钠;
②Na2CO3浓溶液中通入氯气时,可产生气体CO2和化合物NaClO3 ,结合原子守恒和电子守恒写出反应的化学方程式.
解答 解:①氯气和水反应生成HCl和HClO,HCl和HClO与碳酸钠反应生成氯化钠、碳酸氢钠和次氯酸钠,反应方程式为2Na2CO3+Cl2+H2O=2 NaHCO3+NaCl+NaClO,
故答案为:2Na2CO3+Cl2+H2O=2 NaHCO3+NaCl+NaClO;
②Na2CO3浓溶液中通入氯气时,可产生气体CO2和化合物NaClO3.氯气是氧化剂生成NaClO3,电子转移5,生成NaCl电子转移1,反应的化学方程式为:3Na2CO3+3Cl2=NaClO3+5NaCl+3CO2,
故答案为:3Na2CO3+3Cl2=NaClO3+5NaCl+3CO2.
点评 本题考查了化学方程式书写,主要是氧化还原反应电子守恒的应用,掌握基础解题关键,题目难度中等.

练习册系列答案
相关题目
9.下列各组中每种物质都既有离子键又有共价键的一组是( )
| A. | NaOH、H2SO4、(NH4)2SO4 | B. | HCl、Al2O3、MgCl2 | ||
| C. | Na2CO3、HNO3、MgO | D. | Ba(OH)2、Na2SO4、Na3PO4 |
10.用下列实验装置完成对应的实验(部分仪器略去),能达到实验目的是( )
| A. |  如图验证溴乙烷发生消去反应生成烯烃 | |
| B. | 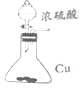 如图进行浓硫酸与铜的反应 | |
| C. |  如图实验验证酸性:CH3COOH>H2CO3>C6H5OH | |
| D. |  如图吸收氨气 |
7.化学与生活、社会发展息息相关,下列有关说法不正确的是( )
| A. | “时气错逆,霾雾蔽日”,雾所形成的气溶胶能产生丁达尔效应 | |
| B. | “青蒿一揭,以水二升溃,绞取汁”,屠呦呦提取青蒿素的过程中发生了化学变化 | |
| C. | “熬胆矾铁釜,久之亦化为铜”,北宋沈括用胆矾炼铜的过程属于置换反应 | |
| D. | “外观如雪,强烧之,紫青烟起”,南北朝陶弘景对硝酸钾的鉴定过程中利用了焰色反应 |
14.将1mol CH4和适量的O2在密闭容器中点燃,充分反应后CH4和O2均无剩余,产物的总质量为72g,且均为气体(101kPa,120℃),下列有关叙述不正确的是( )
| A. | 反应中消耗O2 56 g | |
| B. | 所得产物中各物质的物质的量相等 | |
| C. | 若将产物通过碱石灰,不能被完全吸收 | |
| D. | 若将产物通过浓硫酸,充分吸收后,浓硫酸增重36g |
4.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 10mL18mol/L浓硫酸与足量铜加热充分反应,转移电子数为0.18NA | |
| B. | 11gT2O超重水中含有的中子数为5NA | |
| C. | 标准状况下,22.4LCO2中含有的共用电子对数为2NA | |
| D. | 7.8 gNa2S固体和7.8gNa2O2固体中含有的阴离子数目均为0.1NA |
11.下列关于乙酸的说法正确的是( )
| A. | 常温下是一种无色无味的液体 | B. | 能与乙醇发生酯化反应 | ||
| C. | 不能与NaHCO3反应放出CO2 | D. | 能与溴水发生加成反应 |
9.六种短周期元素A、B、C、D、E、F的原子序数依次增大,其中A与E,B与F同主族,E与F同周期;D的核电荷数是F的最外层电子数的2倍;B的最高正价与最低负价的代数和为0;常温下单质A与E的状态不同.下列判断正确的是( )
| A. | A、D两种元素形成的化合物中只含有极性键 | |
| B. | A、C、D三种元素形成的化合物一定是共价化合物,其溶液一定呈酸性 | |
| C. | 六种元素中,最高价氧化物对应水化物酸性最强的元素是C | |
| D. | 原子半径由大到小的顺序是F>E>C>D |
 所示的是战国初期的曾侯乙编钟,它是一套庞大的青铜乐器.铸造该器物的主要材料是b(填字母,下同).
所示的是战国初期的曾侯乙编钟,它是一套庞大的青铜乐器.铸造该器物的主要材料是b(填字母,下同).