��Ŀ����
�Ҵ�����Ũ�����Ϲ��ȵķ�Ӧ�����У��ܷ�Ӧ������Ӱ�죬�ɷ������ͬ�ķ�Ӧ���ͣ�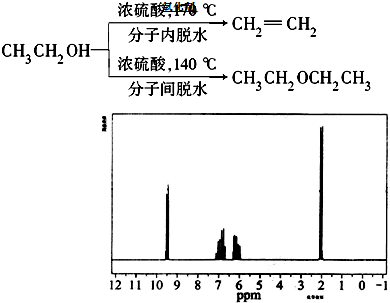
1��4-����������һ�ֳ������ܼ���������ͨ�����кϳ�·���Ƶã�
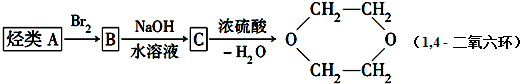
��ش�
��1��д���������ʵĽṹ��ʽ��
A�� ��B�� ��C�� ��
��2��д�����з�Ӧ����ʽ����ע����Ӧ���ͣ�
A��B ����Ӧ���ͣ� ��
B��C ����Ӧ���ͣ� ��
C��1��4�������� ����Ӧ���ͣ� ��

1��4-����������һ�ֳ������ܼ���������ͨ�����кϳ�·���Ƶã�

��ش�
��1��д���������ʵĽṹ��ʽ��
A��
��2��д�����з�Ӧ����ʽ����ע����Ӧ���ͣ�
A��B
B��C
C��1��4��������
���㣺�л�����ƶ�
ר�⣺�л���Ļ�ѧ���ʼ��ƶ�
�������������Ʒ����������ݺϳ�·����1��4-���������Ľṹ����֪��CӦ����HOCH2CH2OH��B��BrCH2CH2Br����A��CH2=CH2��A���巢���ӳɷ�Ӧ����B��B����ˮ�ⷴӦ����C��C�������Ӽ���ˮ��ȡ������Ӧ����1��4-�����������ݴ˴��⣮
���
�⣺���ݺϳ�·����1��4-���������Ľṹ����֪��CӦ����HOCH2CH2OH��B��BrCH2CH2Br����A��CH2=CH2��A���巢���ӳɷ�Ӧ����B��B����ˮ�ⷴӦ����C��C�������Ӽ���ˮ��ȡ������Ӧ����1��4-����������
��1��������ķ�����֪��A��CH2=CH2��B��BrCH2CH2Br��C��HOCH2CH2OH��
�ʴ�Ϊ��CH2=CH2��BrCH2CH2Br��HOCH2CH2OH��
��2��A��B�ķ�Ӧ����ʽΪCH2=CH2+Br2=BrCH2CH2Br����Ӧ�����Ǽӳɷ�Ӧ��
B��C �ķ�Ӧ����ʽΪBrCH2CH2Br+2NaOH
HOCH2CH2OH+2NaBr����Ӧ������ˮ�⣨ȡ������Ӧ��
C��1��4���������ķ�Ӧ����ʽΪ2HOCH2CH2OH
 +2H2O����Ӧ������ȡ����Ӧ��
+2H2O����Ӧ������ȡ����Ӧ��
�ʴ�Ϊ��CH2=CH2+Br2=BrCH2CH2Br���Ǽӳɷ�Ӧ��BrCH2CH2Br+2NaOH
HOCH2CH2OH+2NaBr��ˮ�⣨ȡ������Ӧ��2HOCH2CH2OH
 +2H2O��ȡ����Ӧ��
+2H2O��ȡ����Ӧ��
��1��������ķ�����֪��A��CH2=CH2��B��BrCH2CH2Br��C��HOCH2CH2OH��
�ʴ�Ϊ��CH2=CH2��BrCH2CH2Br��HOCH2CH2OH��
��2��A��B�ķ�Ӧ����ʽΪCH2=CH2+Br2=BrCH2CH2Br����Ӧ�����Ǽӳɷ�Ӧ��
B��C �ķ�Ӧ����ʽΪBrCH2CH2Br+2NaOH
| ˮ |
| �� |
C��1��4���������ķ�Ӧ����ʽΪ2HOCH2CH2OH
| ŨH2SO4 |
| �� |
 +2H2O����Ӧ������ȡ����Ӧ��
+2H2O����Ӧ������ȡ����Ӧ���ʴ�Ϊ��CH2=CH2+Br2=BrCH2CH2Br���Ǽӳɷ�Ӧ��BrCH2CH2Br+2NaOH
| ˮ |
| �� |
| ŨH2SO4 |
| �� |
 +2H2O��ȡ����Ӧ��
+2H2O��ȡ����Ӧ��
������������Ҫ�������л�����ƶ���ϳɣ�����ʱע��ͨ����ѧ��Ӧʹ�л����̼�����������̣���̼����̼�����ת�䣬����̼����̼���������ת�����ֹ����ţ�����ȡ��ͬ���͡���ͬ���ʵ��л����Ŀ�ѶȲ����ܽ�ȫ��ؿ���ѧ�����л���ѧ����֪ʶ����˼ά����������˼ά�����ȣ�

��ϰ��ϵ�д�
 ����С����ͬ������ϵ�д�
����С����ͬ������ϵ�д�
�����Ŀ
��25�桢101kPa�£�1g�״�ȼ������CO2��Һ̬ˮʱ����22.68kJ�������Ȼ�ѧ����ʽ��ȷ���ǣ�������
A��CH3OH��l��+3
| ||
| B��2CH3OH��l��+3O2��g���T2CO2��g��+4H2O��l����H=-1452 kJ?mol-1 | ||
| C��2CH3OH��l��+3O2��g���T2CO2��g��+4H2O��l����H=-725.8 kJ?mol-1 | ||
| D��2CH3OH��l��+3O2��g���T2CO2��g��+4H2O��l����H=+1452 kJ?mol-1 |
��һ������������������������ͭ�Ļ�����ĩ����70mL 4.0mol/L�����У���ַ�Ӧ�����448mL H2����״��������������0.64g�����ˣ���Һ����Cu2+������Һ��ˮϡ�͵�200mL���������c��H+��Ϊ0.20mol/L����ԭ������е������������ǣ�������
| A��4.48g |
| B��3.36g |
| C��3.25g |
| D��2.80g |
0.5molij����1molHCl��һ��������ǡ����ȫ�ӳɣ����������ڹ�������Cl2����ȡ����Ӧ����ԭ��ǡ��ȫ����ȡ������Cl23mol��������ķ���ʽΪ��������
| A��C3H6 |
| B��C4H6 |
| C��C3H4 |
| D��C2H4 |
 �����£���100mL 0.01mol?L-1 HA��Һ����μ���0.02mol?L-1MOH��Һ��ͼ����ʾ���߱�ʾ�����Һ��pH�仯���������仯���Բ��ƣ���������˵��������ǣ�������
�����£���100mL 0.01mol?L-1 HA��Һ����μ���0.02mol?L-1MOH��Һ��ͼ����ʾ���߱�ʾ�����Һ��pH�仯���������仯���Բ��ƣ���������˵��������ǣ�������| A�������£�MA��ˮ��Һ��pH=a����ˮ���������c��H+��=1��10-a mol?L-1 |
| B����K�㣬ˮ��Һ�д��ڣ�c��M+��=2c��A-�� |
| C����N�㣬ˮ��Һ�д��ڣ�c��M+��+c��H+��=c��A-��+c��OH-�� |
| D����K�㣬����ʱ��Һ��pH=10����c��MOH��+c��M+��=0.01mol?L-1 |

