题目内容
氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点.
已知:CH4(g)+H2O(g)═CO (g)+3H2(g)△H=+206.2kJ?mol-1
CH4(g)+CO2(g)═2CO(g)+2H2(g)△H=+247.4kJ?mol-1
以甲烷为原料制取氢气是工业上常用的制氢方法.CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为 .
已知:CH4(g)+H2O(g)═CO (g)+3H2(g)△H=+206.2kJ?mol-1
CH4(g)+CO2(g)═2CO(g)+2H2(g)△H=+247.4kJ?mol-1
以甲烷为原料制取氢气是工业上常用的制氢方法.CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为
考点:用盖斯定律进行有关反应热的计算
专题:
分析:利用盖斯定律解答,从待求反应出发分析反应物、生成物在所给反应中的位置,通过相互加减可得.
解答:
解:①CH4(g)+H2O(g)═CO(g)+3H2(g)△H=+206.2kmol-1
②CH4(g)+CO2(g)═2CO(g)+2H2(g)△H=+247.4kJmol-1
据盖斯定律,①×2-②得:CH4(g)+2H2O(g)═CO2(g)+4H2(g)△H=165.0kmol-1,
故答案为:CH4(g)+2H2O(g)═CO2(g)+4H2(g)△H=+165.0kmol-1.
②CH4(g)+CO2(g)═2CO(g)+2H2(g)△H=+247.4kJmol-1
据盖斯定律,①×2-②得:CH4(g)+2H2O(g)═CO2(g)+4H2(g)△H=165.0kmol-1,
故答案为:CH4(g)+2H2O(g)═CO2(g)+4H2(g)△H=+165.0kmol-1.
点评:有关盖斯定律的习题,首先要根据所求的反应分析,分析以下几点:
1、所求反应中的反应物在哪个反应了?是反应物还是生成物?
2、所给反应中哪些物质是所求反应中没有的?
3、如何才能去掉无用的?然后,通过相互加减,去掉无关物质.
将所对应的△H代入上述化学方程式的加减中就可以了.
1、所求反应中的反应物在哪个反应了?是反应物还是生成物?
2、所给反应中哪些物质是所求反应中没有的?
3、如何才能去掉无用的?然后,通过相互加减,去掉无关物质.
将所对应的△H代入上述化学方程式的加减中就可以了.

练习册系列答案
相关题目
下列关于铝的叙述中,不正确的是( )
| A、铝是地壳里含量最多的金属元素 |
| B、铝容易失去电子,表现还原性 |
| C、在空气中用酒精灯点不着 |
| D、在常温下,铝不能与氧气反应 |
将NaClO3和Na2SO3按物质的量比2:1加入烧瓶中,再滴入少量稀硫酸并加热,产生棕黄色气体X,反应后测得恰好完全反应,则X为( )
| A、ClO2 |
| B、Cl2O3 |
| C、Cl2O |
| D、Cl2 |
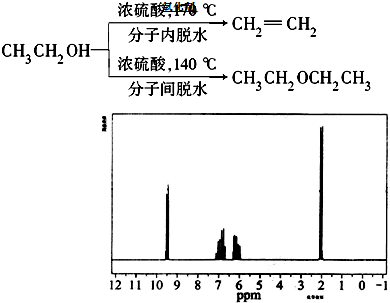
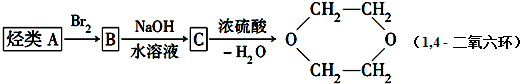
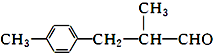
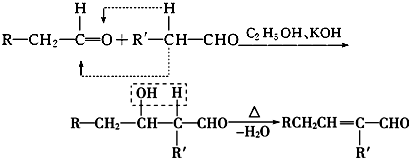 (R-代表烃基)
(R-代表烃基)