题目内容
某元素M所形成的气态单质为双原子分子,共有三种形式,其式量分别为70、72、74,它们的物质的量之比为9:6:1,则:M有 种同位素,其质量数分别为 (取整数),各种同位素所占的原子百分比分别为 (取整数);M2的平均式量为 .
考点:同位素及其应用,质量数与质子数、中子数之间的相互关系
专题:原子组成与结构专题
分析:M所形成的气态单质为双原子分子,共有三种形式,故M有两种同位素;
假设分别为A和B,则它们的组合为:AA、AB、BB,AA的式量为70、BB的式量为74,由此得出A和B的质量数;
根据AA、AB、BB的分子个数比为9:6:1得出A和B所占的原子百分比;M2的平均式量=
.
假设分别为A和B,则它们的组合为:AA、AB、BB,AA的式量为70、BB的式量为74,由此得出A和B的质量数;
根据AA、AB、BB的分子个数比为9:6:1得出A和B所占的原子百分比;M2的平均式量=
| 总质量 |
| 总物质的量 |
解答:
解:M所形成的气态单质为双原子分子,共有三种形式,故M有两种同位素;假设分别为A和B,则它们的组合为:AA、AB、BB,AA的式量为70、BB的式量为74,故A和B的质量数分别为35和37;AA、AB、BB的分子个数比为9:6:1,故共有A:9×2+6=24,B:6+1×2=8;故A所占的原子百分比分别为
×100%=75%,B所占的原子百分比分别为1-75%=25%;M2的平均式量=
=
=71,
故答案为:两;35和37;75%和25%;71.
| 24 |
| 24+8 |
| 总质量 |
| 总物质的量 |
| 70×9+72×6+74×1 |
| 9+6+1 |
故答案为:两;35和37;75%和25%;71.
点评:本题考查同位素的组合、原子百分比和平均式量的计算,难度中等.要注意两种同位素能形成三种双原子分子.

练习册系列答案
相关题目
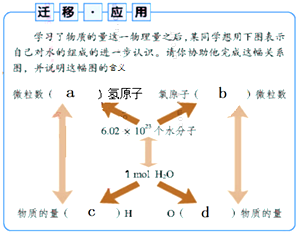 如图所示为鲁科版化学教科书(我们正在使用的教科书)必修1中“迁移应用”栏目的一个学习活动.下列关于a、b、c、d处所填内容及这幅图含义的描述中,不正确的是( )
如图所示为鲁科版化学教科书(我们正在使用的教科书)必修1中“迁移应用”栏目的一个学习活动.下列关于a、b、c、d处所填内容及这幅图含义的描述中,不正确的是( )| A、a=1.204×1024、b=6.02×1023、c=2、d=1 |
| B、6.02×1023个H2O水分子中含有1.204×1024个氢原子和6.02×1023个氧原子 |
| C、1mol H2O中含有2mol H和1mol O |
| D、对于同一微粒,其物质的量与微粒数间可通过阿伏加德罗常数实现相互换算 |
下列溶液中的Cl-的物质的量与50mL 1mol?L-1 MgCl2溶液中相等的是( )
| A、150mL 1mol?L-1的NaCl溶液 |
| B、75mL 0.5mol?L-1的CaCl2溶液 |
| C、50mL 2mol?L-1的KCl溶液 |
| D、75mL 1mol?L-1的FeCl3溶液 |
下列电子排布中,原子处于激发状态的是( )
| A、1s22s2 |
| B、1s22s22p5 |
| C、1s22s22p63s23p63d54s1 |
| D、1s22s22p63s23p63d104s14p3 |
某化学反应中,反应混合物A、B、C的物质的量浓度(c)与时间(t)关系如下表所示:下列说法正确的是( )
| 初始 | 2min | 4min | 6min | |
| c (A)(mol/L) | 1.45 | 1.28 | 1.00 | 1.00 |
| c (B)(mol/L) | 0.38 | 0.72 | 1.28 | 1.28 |
| c (C)(mol/L) | 0.095 | 0.18 | 0.32 | 0.32 |
| A、该反应的化学方程式为A=2B+C |
| B、4min末A的转化率约为31% |
| C、4~6min时,反应停止了 |
| D、正反应是吸热反应 |