题目内容
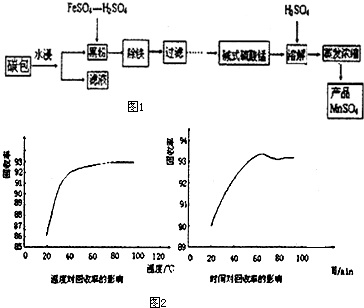
工业上,常用FeSO4-H2SO4溶液浸出法从废旧干电池中回收锰制备硫酸锰,既有效解决废旧电池对环境的污染,又得到了有实际应用意义的锰资源.其工艺流程图如下:(电池的组成为:Zn皮、碳包、Fe壳、碳棒及其它)
(1)为了加快碱式硫酸锰的溶解速率,可采取的措施有 ;在此过程中需保持硫酸过量,其目的是 .
(2)该工艺流程中,温度和时间对产品回收率的影响如图所示:考虑到能耗和生产效率这两个因素,选定的适宜温度是 ,反应时间为 .
(3)测定碳包中MnO2的含量的实验主要步骤为:
a、准确称取样品0.500g,加入50mL蒸馏水于烧杯中溶解.
b、加入4.000gKI,并滴加少量稀硫酸进行酸化,充分搅拌后,放置暗处.
c、15分钟后滴加1mL0.5%淀粉溶液,用cmol/L的Na2S2O3溶液进行滴定(发生的反应为:4I2+S2O32-+5H2O=8I-+2SO42-+10H+),记录消耗Na2S2O3溶液的体积.
d、重复实验2-3次,取有效数据,求平均值得出消耗Na2S2O3溶液的体积胃VmL.
①步骤b中发生反应的离子方程式为:
②步骤c中,到达滴定终点时的现象为:
③碳包中MnO2的质量分数为: .

(1)为了加快碱式硫酸锰的溶解速率,可采取的措施有
(2)该工艺流程中,温度和时间对产品回收率的影响如图所示:考虑到能耗和生产效率这两个因素,选定的适宜温度是
(3)测定碳包中MnO2的含量的实验主要步骤为:
a、准确称取样品0.500g,加入50mL蒸馏水于烧杯中溶解.
b、加入4.000gKI,并滴加少量稀硫酸进行酸化,充分搅拌后,放置暗处.
c、15分钟后滴加1mL0.5%淀粉溶液,用cmol/L的Na2S2O3溶液进行滴定(发生的反应为:4I2+S2O32-+5H2O=8I-+2SO42-+10H+),记录消耗Na2S2O3溶液的体积.
d、重复实验2-3次,取有效数据,求平均值得出消耗Na2S2O3溶液的体积胃VmL.
①步骤b中发生反应的离子方程式为:
②步骤c中,到达滴定终点时的现象为:
③碳包中MnO2的质量分数为:
考点:金属的回收与环境、资源保护,制备实验方案的设计
专题:实验题
分析:(1)除了Ca(OH)2和NaCl外,其他的固体物质,均是升高温度,溶解度增大,或是搅拌也能加快溶解;MnSO4是强酸弱碱盐,Mn2+是弱碱阳离子,在水溶液中会水解;(2)从图象可以看出,从80℃开始,回收率达到最高值并几乎不再升高,此时应从耗能的角度来考虑;在60℃时,回收率达到最高值;
(3)①MnO2中滴入KI后,在酸性环境下,MnO2把I-氧化为I2,MnO2被还原为Mn2+,据此写出离子方程式;
②想步骤b所得的含I2的溶液中滴加1mL0.5%淀粉溶,溶液变蓝;步骤C中,用用cmol/L的Na2S2O3溶液来滴定生成的I2,当蓝色变无色时,达滴定终点;
③由反应可知:4MnO2 ~4I2 ~Na2S2O3 ,根据消耗的Na2S2O3的物质的量,求出MnO2的物质的量,从而求出碳包中MnO2的质量分数.
(3)①MnO2中滴入KI后,在酸性环境下,MnO2把I-氧化为I2,MnO2被还原为Mn2+,据此写出离子方程式;
②想步骤b所得的含I2的溶液中滴加1mL0.5%淀粉溶,溶液变蓝;步骤C中,用用cmol/L的Na2S2O3溶液来滴定生成的I2,当蓝色变无色时,达滴定终点;
③由反应可知:4MnO2 ~4I2 ~Na2S2O3 ,根据消耗的Na2S2O3的物质的量,求出MnO2的物质的量,从而求出碳包中MnO2的质量分数.
解答:
解:(1)除了Ca(OH)2和NaCl外,其他的固体物质,均是升高温度,溶解度增大,为了加快碱式硫酸锰的溶解速率,可采取的措施有加热,或是搅拌也能加快溶解;MnSO4是强酸弱碱盐,Mn2+是弱碱阳离子,在水溶液中会水解,故此过程中需保持硫酸过量,其目的是抑制硫酸锰的水解,故答案为:加热或搅拌;抑制硫酸锰的水解;
(2)从图象可以看出,从80℃开始,回收率达到最高值并几乎不再升高,而温度越高,耗能越多,从耗能的角度来考虑,应选定的适宜温度是80℃;在60℃时,回收率达到最高值,时间延后后,回收率反而下降,故适宜的反应时间为60min,故答案为:80℃,60min;
(3)①MnO2中滴入KI后,在酸性环境下,MnO2把I-氧化为I2,MnO2被还原为Mn2+,故离子方程式为:MnO2+I-+H+=Mn2++I2+2H2O,故答案为:MnO2+I-+H+=Mn2++I2+2H2O;
②想步骤b所得的含I2的溶液中滴加1mL0.5%淀粉溶,溶液变蓝;步骤C中,用cmol/L的Na2S2O3溶液来滴定生成的I2,故达滴定终点时,蓝色变无色且半分钟不恢复原色即达滴定终点,故答案为:溶液由蓝色变为无色且半分钟不恢复原色;
③滴定过程中消耗的Na2S2O3的物质的量n=CV=cmol/L×V×10-3L=10-3CVmol,设MnO2的物质的量为Xmol,
据反应可知:4MnO2 ~4I2 ~Na2S2O3
4 1
Xmol 10-3CVmol
可得:
=
解得X=4×10-3CVmol
故MnO2的质量m=nM=4×10-3CVmol×87g/mol=0.348CVg
故碳包中MnO2的质量分数=
×100%=69.6Cv%
故答案为:69.6Cv%
(2)从图象可以看出,从80℃开始,回收率达到最高值并几乎不再升高,而温度越高,耗能越多,从耗能的角度来考虑,应选定的适宜温度是80℃;在60℃时,回收率达到最高值,时间延后后,回收率反而下降,故适宜的反应时间为60min,故答案为:80℃,60min;
(3)①MnO2中滴入KI后,在酸性环境下,MnO2把I-氧化为I2,MnO2被还原为Mn2+,故离子方程式为:MnO2+I-+H+=Mn2++I2+2H2O,故答案为:MnO2+I-+H+=Mn2++I2+2H2O;
②想步骤b所得的含I2的溶液中滴加1mL0.5%淀粉溶,溶液变蓝;步骤C中,用cmol/L的Na2S2O3溶液来滴定生成的I2,故达滴定终点时,蓝色变无色且半分钟不恢复原色即达滴定终点,故答案为:溶液由蓝色变为无色且半分钟不恢复原色;
③滴定过程中消耗的Na2S2O3的物质的量n=CV=cmol/L×V×10-3L=10-3CVmol,设MnO2的物质的量为Xmol,
据反应可知:4MnO2 ~4I2 ~Na2S2O3
4 1
Xmol 10-3CVmol
可得:
| 4 |
| X |
| 1 |
| 10-3CV |
解得X=4×10-3CVmol
故MnO2的质量m=nM=4×10-3CVmol×87g/mol=0.348CVg
故碳包中MnO2的质量分数=
| 0.348CVg |
| 0.500g |
故答案为:69.6Cv%
点评:本题考查了滴定过程中的有关计算和实验操作以及氧化还原反应的书写,根据滴定物质之间的计量关系来进行计算,综合性较强,但难度不大.

练习册系列答案
相关题目
化合物丙由如下反应:C4H10O(甲)
C4H8(乙)
C4H8Br2(丙)得到,丙不可能的是( )
| 浓H2SO4 |
| △ |
| Br2 |
| CCl4 |
| A、CH3CH2CHBrCH2Br |
| B、CH3CH(CH2Br)2 |
| C、CH3CHBrCHBrCH3 |
| D、(CH3)2CBrCH2Br |
在一定温度下,向饱和氢氧化钠溶液中加入一定量的过氧化钠固体,充分反应后恢复到原来温度下,下列说法正确的是( )
| A、溶液的pH不变,有氢气放出 |
| B、溶液的pH增大,有氧气放出 |
| C、溶液中Na+数目减小,有氧气放出 |
| D、溶液中c(Na+)增大,有氧气放出 |
研究二氧化碳性质的微型实验装置如图,现用70%硫酸溶液和亚硫酸钠晶体反应制取SO2气体,实验现象很明显,且不易污染空气.下列说法中错误的是( )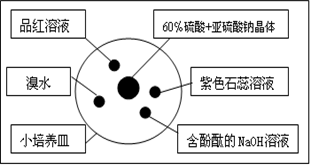

| A、溴水橙色褪去,原因是SO2气体具有漂白性 |
| B、含酚酞的NaOH溶液红色变浅,原因是SO2气体具有漂白性 |
| C、品红溶液褪色,原因是SO2气体具有漂白性 |
| D、紫色石蕊溶液变蓝色,原因是SO2气体具有酸性和漂白性 |

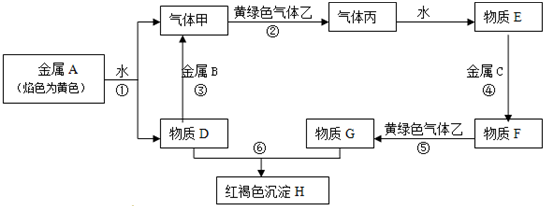

 雾.试完成下列问题:
雾.试完成下列问题: