题目内容
二氧化铈(CeO2)是一种重要的稀土氧化物.平板电视显示屏生产过程中产生大量的废玻璃粉末(含SiO2、Fe2O3、CeO2以及其他少量可溶于稀酸的物质).某课题组以此粉末为原料回收铈,设计实验流程如图:

(1)洗涤滤渣A的目的是为了去除 (填离子符号),检验该离子是否洗涤的方法是 .
(2)第②步反应的离子方程式是 ,滤渣B的主要成分是 .
(3)萃取是分离稀土元素的常用方法,已知化合物TBP作为萃取剂能将铈离子从水溶液中萃取出来,TBP (填“能”或“不能”)与水互溶.实验室进行萃取操作是用到的主要玻璃仪器有 、烧杯、玻璃棒、量筒等.

(1)洗涤滤渣A的目的是为了去除
(2)第②步反应的离子方程式是
(3)萃取是分离稀土元素的常用方法,已知化合物TBP作为萃取剂能将铈离子从水溶液中萃取出来,TBP
考点:金属的回收与环境、资源保护
专题:实验题
分析:根据该反应过程为:①CeO2、SiO2、Fe2O3等中加入稀盐酸,Fe2O3转化FeCl3存在于滤液中,滤渣为CeO2和SiO2;②加入稀硫酸和H2O2,CeO2转化为Ce3+,滤渣为SiO2;③加入碱后Ce3+转化为沉淀,④通入氧气讲Ce从+3氧化为+4,得到产品;
(1)根据滤渣A上含有FeCl3;取最后一次洗涤液,加入KSCN溶液,若不出现红色,则已洗净,反之,未洗净;
(2)根据氧化还原反应中电子得失守恒来分析;滤渣B为SiO2;
(3)萃取剂与水不互溶,结合萃取需要的仪器分析.
(1)根据滤渣A上含有FeCl3;取最后一次洗涤液,加入KSCN溶液,若不出现红色,则已洗净,反之,未洗净;
(2)根据氧化还原反应中电子得失守恒来分析;滤渣B为SiO2;
(3)萃取剂与水不互溶,结合萃取需要的仪器分析.
解答:
解:(1)滤渣A上含有FeCl3,洗涤滤渣A的目的是为了除去Fe3+、Cl-;取最后一次洗涤液,加入KSCN溶液,若不出现红色,则已洗净,反之,未洗净;
故答案为:Fe3+、Cl-;取最后一次洗涤液,加入KSCN溶液,若不出现红色,则已洗净,反之,未洗净或取最后洗涤液少量,滴加AgNO3,如无白色沉淀,则洗干净;
(2)稀硫酸、H2O2,CeO2三者反应生成转化为Ce2(SO4)3、O2和H2O,反应的离子方程式为:6H++H2O2+2CeO2=2Ce3++O2 ↑+4H2O;加入稀硫酸和H2O2,CeO2转化为Ce3+,SiO2不反应,滤渣B的成分为SiO2,
故答案为:6H++H2O2+2CeO2=2Ce3++O2 ↑+4H2O;SiO2;
(3)化合物TBP作为萃取剂能将铈离子从水溶液中萃取出来,所以TBP不能与水互溶,故答案为:不能;分液漏斗.
故答案为:Fe3+、Cl-;取最后一次洗涤液,加入KSCN溶液,若不出现红色,则已洗净,反之,未洗净或取最后洗涤液少量,滴加AgNO3,如无白色沉淀,则洗干净;
(2)稀硫酸、H2O2,CeO2三者反应生成转化为Ce2(SO4)3、O2和H2O,反应的离子方程式为:6H++H2O2+2CeO2=2Ce3++O2 ↑+4H2O;加入稀硫酸和H2O2,CeO2转化为Ce3+,SiO2不反应,滤渣B的成分为SiO2,
故答案为:6H++H2O2+2CeO2=2Ce3++O2 ↑+4H2O;SiO2;
(3)化合物TBP作为萃取剂能将铈离子从水溶液中萃取出来,所以TBP不能与水互溶,故答案为:不能;分液漏斗.
点评:本题以工艺流程为基础,考察化学实验基本操作、元素及化合物知识、化学计算、氧化还原反应等相关知识,题目难度中等.

练习册系列答案
相关题目
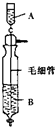 《Inorganic Syntheses》(无机合成)一书中,有一如图所示的装置,用以制备某种干燥的纯净气体.该装置中所装的药品正确的是( )
《Inorganic Syntheses》(无机合成)一书中,有一如图所示的装置,用以制备某种干燥的纯净气体.该装置中所装的药品正确的是( )| A、A中装浓盐酸,B中装浓硫酸 |
| B、A中装浓硫酸,B中装浓盐酸 |
| C、A中装氢氧化钠浓溶液,B中装浓氨水 |
| D、A中装浓氨水,B中装氢氧化钠浓溶液 |
一定物质的量浓度溶液的配制和酸碱中和滴定是中学化学中两个典型的定量实验.某研究性学习小组在实验中配制1mol?L-1的稀硫酸标准,然后用其滴定某未知浓度的氢氧化钠溶液.下列有关说法中正确的是( )
| A、实验中所用到的锥形瓶和容量瓶,在洗涤后均需要润洗 |
| B、酸式滴定管用蒸馏水洗涤后,即装入标准浓度的稀硫酸,最终氢氧化钠溶液浓度将偏大 |
| C、滴定时,左手提酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视滴定管内液面变化 |
| D、中和滴定时,若在最后一次读数时俯视读数,则导致实验结果偏大 |
分离下列各组固体混合物时,可按溶解、过滤、蒸发的操作顺序进行的是( )
| A、氯化钠和硝酸钾 |
| B、铁粉和锌粉 |
| C、氯化钾和碳酸钙 |
| D、碳酸铵和氯化铵 |
下列说法中,不正确的是( )
| A、焓变为正值的反应都是吸热反应 |
| B、放热的,熵增加的反应一定能自发进行 |
| C、同一条件下,氨水在不同物质的量浓度的溶液中,其电离程度是不同的 |
| D、强电解质都是离子化合物,弱电解质都是共价化合物 |
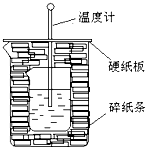 50ml0.50mol?L-1盐酸与50mL0.55mol?L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中放出的热量可计算中和热.回答下列问题:
50ml0.50mol?L-1盐酸与50mL0.55mol?L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中放出的热量可计算中和热.回答下列问题: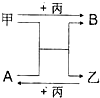 甲、乙、丙是三种单质,A、B是两种化合物,它们相互间有如图转化关系.请回箸下列问题:
甲、乙、丙是三种单质,A、B是两种化合物,它们相互间有如图转化关系.请回箸下列问题: