题目内容
7.下列体系中,离子能大量共存的是( )| A. | 无色透明的酸性溶液:MnO4-、K+、Cl-、SO42- | |
| B. | 0.1 mol/LNaHCO3溶液:Na+、Ba2+、NO3-、OH- | |
| C. | 使酚酞变红的溶液:K+、Na+、NO3-、Cl- | |
| D. | 滴加KSCN显红色的溶液:NH4+、K+、Cl-、CO32- |
分析 A.MnO4-为紫色;
B.离子之间结合生成沉淀;
C.使酚酞变红的溶液,显碱性;
D.滴加KSCN显红色的溶液,含铁离子.
解答 解:A.MnO4-为紫色,与无色不符,且MnO4-、Cl-发生氧化还原反应,故A错误;
B.Ba2+、HCO3-、OH-结合生成沉淀,不能共存,故B错误;
C.使酚酞变红的溶液,显碱性,该组离子之间不反应,可大量共存,故C正确;
D.滴加KSCN显红色的溶液,含铁离子,与CO32-相互促进水解,不能共存,故D错误;
故选C.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应、氧化还原反应的离子共存考查,题目难度不大.

练习册系列答案
 孟建平名校考卷系列答案
孟建平名校考卷系列答案
相关题目
17.X、Y、Z、W和N均是由短周期元素组成的五种化合物.已知五种化合物水溶液的焰色反应均呈黄色,Y、Z和N均由三种元素组成.请根据题目要求回答下列问题.
(1)固体化合物X为浅黄色粉末,该化合物中含有的化学键有AC(填序号).
A.离子键 B.极性共价键 C.非极性共价键 D.氢键
(2)写出X与二氧化碳反应的化学方程式2CO2+2Na2O2═2Na2CO3+O2.
(3)下表为Y与Z实验的部分内容:
写出Y与稀硫酸反应的离子方程式S2O32-+2H+═S↓+SO2↑+H2O.
(4)写出含0.1mol Z的溶液与20mL 5mol•L-1的盐酸反应的离子反应式AlO2-+H++H2O═Al(OH)3↓.实验③加热蒸发、灼烧得到的最终产物主要是Al2O3.
(1)固体化合物X为浅黄色粉末,该化合物中含有的化学键有AC(填序号).
A.离子键 B.极性共价键 C.非极性共价键 D.氢键
(2)写出X与二氧化碳反应的化学方程式2CO2+2Na2O2═2Na2CO3+O2.
(3)下表为Y与Z实验的部分内容:
| 序号 | 主要实验步骤及实验现象 |
| ① | 在含Y的溶液中,加入稀硫酸放置,产生浅黄色沉淀和无色有刺激性气味的气体,该气体可使品红溶液褪色 |
| ② | 在含Z的溶液中,滴加盐酸,开始有白色沉淀,继续滴加盐酸,白色沉淀先增加后消失,然后加入过量的氨水又出现白色沉淀 |
| ③ | 将实验②最终得到的混合物加热蒸发、灼烧,最终得到白色固体 |
(4)写出含0.1mol Z的溶液与20mL 5mol•L-1的盐酸反应的离子反应式AlO2-+H++H2O═Al(OH)3↓.实验③加热蒸发、灼烧得到的最终产物主要是Al2O3.
18.下列物质中,没有固定沸点的是( )
| A. | 正已烷 | B. | 苯 | C. | 汽油 | D. | 乙烯 |
15.若NA表示阿伏伽德罗常数,下列说法正确的是( )
| A. | 1molCl2的体积为22.4L | |
| B. | 在0℃101KPa时,22.4L氢气中含有NA个氢原子 | |
| C. | 14g氮气中含有7NA个电子 | |
| D. | NA个CO和0.5molCH4的质量比为7:4 |
12.几种短周期元素的主要化合价及原子的原子半径数据见表:
据表中信息判断,下列有关叙述中,正确的是( )
| 元素代号 | L | M | Q | R | T |
| 主要化合价 | +2 | +3 | +6、-2 | +7、-1 | -2 |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.099 | 0.074 |
| A. | M与T形成的化合物和强酸、强碱均能反应 | |
| B. | L、M的单质分别与同浓度的稀盐酸反应时,M的单质反应更剧烈 | |
| C. | Q元素在自然界中只能以化合态形式存在 | |
| D. | L与R两元素形成的化合物中,含有共价键 |
19.分子式为C4H10O的醇与苯甲酸(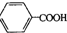 )在一定条件下反应生成酯的种类有( )
)在一定条件下反应生成酯的种类有( )
 )在一定条件下反应生成酯的种类有( )
)在一定条件下反应生成酯的种类有( )| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
17.下列各组互为同位素的是( )
| A. | 氧气、臭氧 | B. | 重氢、超重氢 | C. | 纯碱、苏打 | D. | 乙酸、甲酸 |
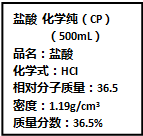 按要求完成下列小题.
按要求完成下列小题. .
.