题目内容
 密闭容器中mA(g)+nB(g)?pC(g),反应达到平衡,经测定增大压强P时,A的转化率随P而变化的曲线如图.则:
密闭容器中mA(g)+nB(g)?pC(g),反应达到平衡,经测定增大压强P时,A的转化率随P而变化的曲线如图.则:(1)增大压强,A的转化率
(2)上述化学方程式中的系数m、n、p的正确关系是
向上述平衡体系中加入B,则平衡
(3)当降低温度时,C的质量分数增大,则A的转化率
考点:转化率随温度、压强的变化曲线
专题:化学平衡专题
分析:根据影响化学平衡移动的因素进行判断得出正确结论.升高温度,平衡向着吸热的方向移动;增大压强,平衡向着气体体积减小的方向移动.
解答:
解:(1)由图象可知,增大压强,A的转化率降低,平衡逆向移动,C的质量分数降低,
故答案为:减小,逆方向,减小;
(2)增大压强,平衡逆向移动,所以逆方向为体积减小的方向,则m+n<p;增大反应B的浓度,平衡正向移动;
故答案为:m+n<p;正移;
(3)当降低温度时,C的质量分数增大,平衡正向移动,A的转化率增大,则正反应是放热反应,
故答案为:增大,放.
故答案为:减小,逆方向,减小;
(2)增大压强,平衡逆向移动,所以逆方向为体积减小的方向,则m+n<p;增大反应B的浓度,平衡正向移动;
故答案为:m+n<p;正移;
(3)当降低温度时,C的质量分数增大,平衡正向移动,A的转化率增大,则正反应是放热反应,
故答案为:增大,放.
点评:本题考查外界条件对化学平衡移动的影响,题目难度不大.要注意勒夏特列原理的运用.

练习册系列答案
相关题目
下列生成SO2的反应中,反应物中的含硫物质被氧化的是( )
| A、Cu与浓H2SO4共热 |
| B、红热的木炭与浓H2SO4反应 |
| C、Na2SO3与浓H2SO4反应 |
| D、S在空气中燃烧 |
已知等体积的20%硫酸溶液其质量大于10%硫酸溶液,则将溶质的质量分数为a%、物质的量浓度为C1mol?L-1的稀硫酸加热蒸发掉溶液总质量的一半的水,此时溶质的质量分数变为b%,物质的量浓度为C2mol?L-1,下列关系正确的是( )
| A、b<2 a |
| B、C2<2 C1 |
| C、C2>2 C1 |
| D、C1=2 C2 |

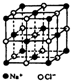 【化学--进修3:物质结构与性质】
【化学--进修3:物质结构与性质】
