题目内容
下列物质①氯化钠 ②Cl2 ③乙醇 ④碳酸,其中
(1)属于强电解质的是 ;
(2)属于非电解质的是 ;
(3)既不是电解质也不是非电解质的是 ;
(4)熔融状态下能导电的是 ;
(5)属于弱电解质的是 (填序号),并写出弱电解质在水溶液中电离的离子方程式 , .
(1)属于强电解质的是
(2)属于非电解质的是
(3)既不是电解质也不是非电解质的是
(4)熔融状态下能导电的是
(5)属于弱电解质的是
考点:电解质与非电解质,强电解质和弱电解质的概念
专题:离子反应专题
分析:电解质是指:在水溶液中或熔融状态下能够导电的化合物;
非电解质是指:在水溶液里和熔融状态下都不导电的化合物;
单质、混合物既不是电解质也不是非电解质;
在水溶液里或熔融状态下完全电离的电解质是强电解质,部分电离的电解质是弱电解质,强酸、强碱和大部分的盐属于强电解质,弱酸、弱碱、水是弱电解质,弱电解质分步电离;以此解答.
熔融状态可以导电的化合物一定为电解质,必须满足在熔融状态下存在自由移动的导电粒子,这类电解质属于离子化合物,
非电解质是指:在水溶液里和熔融状态下都不导电的化合物;
单质、混合物既不是电解质也不是非电解质;
在水溶液里或熔融状态下完全电离的电解质是强电解质,部分电离的电解质是弱电解质,强酸、强碱和大部分的盐属于强电解质,弱酸、弱碱、水是弱电解质,弱电解质分步电离;以此解答.
熔融状态可以导电的化合物一定为电解质,必须满足在熔融状态下存在自由移动的导电粒子,这类电解质属于离子化合物,
解答:
解:(1)①氯化钠是在水溶液里或熔融状态下完全电离的电解质,属于强电解质;
故答案为:①;
(2)③乙醇是在水溶液里和熔融状态下都不导电的化合物,属于非电解质;
故答案为:③;
(3)②Cl2 是单质,既不是电解质也不是非电解质;
故答案为:②;
(4)①氯化钠为离子化合物,在熔融状态下电离产生自由移动氯离子和钠离子而导电;
故答案为:①;
(5)碳酸是弱酸,分两步电离,H2CO3?H++HCO3-,HCO3-?H++CO32-,
故答案为:④;H2CO3?H++HCO3-,HCO3-?H++CO32-;
故答案为:④;H2CO3?H++HCO3-,HCO3-?H++CO32-;
故答案为:①;
(2)③乙醇是在水溶液里和熔融状态下都不导电的化合物,属于非电解质;
故答案为:③;
(3)②Cl2 是单质,既不是电解质也不是非电解质;
故答案为:②;
(4)①氯化钠为离子化合物,在熔融状态下电离产生自由移动氯离子和钠离子而导电;
故答案为:①;
(5)碳酸是弱酸,分两步电离,H2CO3?H++HCO3-,HCO3-?H++CO32-,
故答案为:④;H2CO3?H++HCO3-,HCO3-?H++CO32-;
故答案为:④;H2CO3?H++HCO3-,HCO3-?H++CO32-;
点评:本题考查了电解质与非电解质、强电解质与弱电解质的概念及判断,题目难度不大,注意明确强弱电解质的本质区别,明确电解质与非电解质的概念及判断方法.

练习册系列答案
相关题目
下列说法中正确的是(NA表示阿伏伽德罗常数)( )
| A、0.1mol H2O中所含的原子总数是0.3NA |
| B、在常温常压下,11.2L氯气所含的原子数为NA |
| C、标准状况下,22.4L氢气所含的质子数为2 2.4NA |
| D、2mol K2SO4中离子的总数为4NA |
在实验中,下列的操作错误的是( )
| A、稀释浓硫酸时,将浓硫酸慢慢注入盛有水的烧杯,并不断用玻璃棒搅拌 |
| B、制取蒸馏水时,为防止烧瓶内产生暴沸现象,应先向烧瓶中加入几片碎瓷片 |
| C、分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| D、用蒸发的方法将自来水制成蒸馏水 |
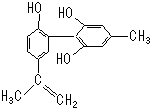 “人文奥运”的一个重要体现是:坚决反对运动员服用兴奋剂.某种兴奋剂的结构简式如图所示,有关该物质的说法正确的是( )
“人文奥运”的一个重要体现是:坚决反对运动员服用兴奋剂.某种兴奋剂的结构简式如图所示,有关该物质的说法正确的是( )| A、1 mol该物质与浓溴水和H2反应最多消耗Br2和H2分别为4 mol、7 mol |
| B、滴入KMnO4(H+)溶液,观察紫色褪去,能证明结构中存在碳碳双键 |
| C、遇FeCl3溶液显紫色,因为该物质与苯酚属于同系物 |
| D、该分子中的所有原子可能共平面 |