题目内容
下列说法中正确的是(NA表示阿伏伽德罗常数)( )
| A、0.1mol H2O中所含的原子总数是0.3NA |
| B、在常温常压下,11.2L氯气所含的原子数为NA |
| C、标准状况下,22.4L氢气所含的质子数为2 2.4NA |
| D、2mol K2SO4中离子的总数为4NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.1mol H2O中所含的3mol原子;
B.常温常压不是标准状况,气体摩尔体积大于22.4L/mol;
C.1mol氢气含质子为2mol;
D.1molK2SO4中含2molK+和1molSO42-.
B.常温常压不是标准状况,气体摩尔体积大于22.4L/mol;
C.1mol氢气含质子为2mol;
D.1molK2SO4中含2molK+和1molSO42-.
解答:
解:A.1mol H2O中所含的3mol原子,故0.1mol H2O中所含的原子总数是0.3NA,故A正确;
B.常温常压下,气体摩尔体积大于22.4L/mol,11.2L氯气的物质的量小于0.5mol,含有的分子数小于0.5NA,故B错误;
C.标准状况下,22.4L氢气物质的量为1mol,1mol氢气所含的质子数为2NA,故C错误;
D.1molK2SO4中含2molK+和1molSO42-,故2molK2SO4离子的总数为6NA,故D错误;
故选A.
B.常温常压下,气体摩尔体积大于22.4L/mol,11.2L氯气的物质的量小于0.5mol,含有的分子数小于0.5NA,故B错误;
C.标准状况下,22.4L氢气物质的量为1mol,1mol氢气所含的质子数为2NA,故C错误;
D.1molK2SO4中含2molK+和1molSO42-,故2molK2SO4离子的总数为6NA,故D错误;
故选A.
点评:本题考查阿伏加德罗常数的有关计算和判断,气体摩尔体积的使用条件,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列说法中,不正确的是( )
| A、32g O2所含的分子数目为6.02×1023 |
| B、0.5mol H2SO4 含有的原子数目为3.5×6.02×1023 |
| C、100mL 2mol?L-1的盐酸中含有1.204×1023个HCl分子 |
| D、3.01×1023个Cl2在标准状况下的体积为11.2L |
当密闭容器中合成氨反应N2+3H2?2NH3达到平衡后,保持温度不变,将容器的容积压缩为原来的
.达到新平衡后,与原平衡相比较,下列说法中正确的是( )
| 1 |
| 2 |
| A、容器内的总压强为原来的2倍 |
| B、NH3的浓度为原来的2倍 |
| C、H2的转化率为原来的2倍 |
| D、气体的密度为原来的2倍 |
常温下,下列各组离子在指定溶液中能大量共存的是( )
| A、l.0 mol?L-1 NaClO溶液:Fe2+、K+、I一、Cl- |
| B、澄清透明的溶液:Cu2+、SO42-、Mg2+、Cl- |
| C、由水电离出的C(H+)=1×10-13 mol?L-1的溶液:K+、HCO3-、Na+、Cl- |
| D、滴加甲基橙试液后呈红色的溶液中:Na+、CO32-、K+、CH3COO- |
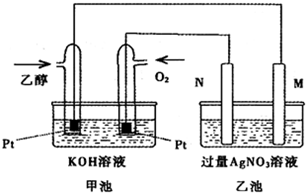
 化学反应中一定伴随着能量的变化,化学能在实际生产生活中的应用将越来越广泛.
化学反应中一定伴随着能量的变化,化学能在实际生产生活中的应用将越来越广泛.