题目内容
【题目】下表为元素周期表的一部分,列出10种元素在周期表中的位置。用化学符号回答下列问题:
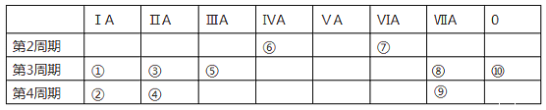
(1)10种元素中,第一电离能最大的是_______,电负性最小的金属元素是_____。
(2)①、③、⑤三种元素最高价氧化物对应的水化物中,碱性最强的是__________。
(3)②、③、④三种元素形成的离子,离子半径由大到小的顺序是_____________。
(4)①和⑨的最高价氧化物对应水化物的化学式分别为_________、____________
(5)①和⑤的最高价氧化物对应水化物相互反应的离子方程式为______________________
(6)用电子式表示第三周期元素中由电负性最小的元素和电负性最大的元素形成化合物的过程:______________________________________
(7)⑨元素的价电子的轨道表示式为________________________________。
【答案】Ar K NaOH r(K+)>r(Ca2+)>r(Mg2+) NaOH HBrO4 Al(OH)3+OH- == AlO2-+2H2O ![]()
![]()
【解析】
根据元素在周期表中的位置,①、②、③、④、⑤、⑥、⑦、⑧、⑨、⑩元素分别是Na、K、Mg、Ca、Al、C、O、Cl、Br、Ar。
(1)Ar最外层有8个电子,结构稳定,10种元素中,第一电离能最大的是Ar;同周期元素从左到右电负性增大,同主族元素从上到下电负性减小,所以电负性最小的金属元素是K。
(2)同周期的元素从左到右,金属性减弱,金属性越强,最高价氧化物对应的水化物碱性越强,Na、Mg、Al三种元素最高价氧化物对应的水化物中,碱性最强的是NaOH。
(3)微粒电子层数越多半径越大,电子层数相同时,质子数越多半径越小,所以K+、Mg2+、Ca2+三种离子,半径由大到小的顺序是r(K+)>r(Ca2+)>r(Mg2+)。
(4) Na的最高价为+1,最高价氧化物对应水化物的化学式为NaOH;Br的最高价是+7,最高价氧化物对应水化物的化学式为HBrO4;
(5) Na的最高价氧化物对应水化物是NaOH,Al的最高价氧化物对应水化物是Al(OH)3,NaOH、Al(OH)3相互反应生成偏铝酸钠,反应的离子方程式为Al(OH)3+OH- == AlO2-+2H2O;
(6) 第三周期元素中由电负性最小的元素是Na,电负性最大的元素是Cl,NaCl为离子化合物,用电子式表示NaCl的形成化合物的过程为![]()
(7)Br是35号元素,核外有35个电子,价电子排布式是4s24p5,价电子的轨道表示式为![]() 。
。

【题目】在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应
X(g)+Y(g) ![]() 2Z(g) △H < 0,一段时间后达到平衡,反应过程中测定的数据如下表:
2Z(g) △H < 0,一段时间后达到平衡,反应过程中测定的数据如下表:
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
下列说法正确的是
A.反应前2min的平均速率ν(Z)=2.0×10-3mol·L-1·min-1
B.其他条件不变,降低温度,反应达到新平衡前ν(逆)> ν(正)
C.该温度下此反应的平衡常数K=1.44
D. 其他条件不变,再充入0.2molZ,平衡时X的体积分数增大