题目内容
16.离子方程式CO32-+2H+=CO2↑+H2O可表示的反应是( )| A. | 石灰石和盐酸 | B. | 碳酸氢铵和盐酸 | C. | 碳酸钾和醋酸 | D. | 碳酸钠和硫酸 |
分析 离子方程式CO32-+2H+→CO2↑+H2O表示可溶性碳酸盐与强酸的反应,注意碳酸盐不能为碳酸钙、碳酸氢铵,酸不能为醋酸,据此进行解答.
解答 解:A.石灰石为碳酸钙,碳酸钙与盐酸反应的离子方程式为:CaCO3+2H+=Ca2++H2O+CO2↑,故A错误;
B.碳酸氢根离子不能拆开,碳酸氢钠与盐酸反应的离子方程式为:CO32-+H+=HCO3-,故B错误;
C.醋酸为弱酸,离子方程式中不能拆开,醋酸与碳酸钾反应的离子方程式为:CO32-+2CH3COOH=H2O+CO2↑+2CH3COO-,故C错误;
D.碳酸钠为可溶性碳酸盐,硫酸为强酸,二者反应的离子方程式为:CO32-+2H+=CO2↑+H2O,故D正确;
故选D.
点评 本题考查了离子方程式的书写,题目难度不大,明确离子方程式表示意义为解答关键,注意掌握离子方程式的书写原则,试题培养了学生的灵活应用能力.

练习册系列答案
相关题目
6.NA表示阿伏加德罗常数的值,则下列说法正确的是( )
| A. | 1 摩尔任何物质都含NA个原子 | |
| B. | 0.1 mol/L K2SO4溶液中含有 K+为0.2 NA | |
| C. | 7.1gCl2与足量的氢氧化钠溶液反应转移的电子数一定为0.2NA | |
| D. | 标准状况下,22.4L 以任意比混合的CO、CO2混合气体所含碳原子数约为NA |
11.下列各组实验中,将等体积的Na2S2O3和HCl混合,反应速率最快的一组是( )
| 组号 | 反应温度(℃) | Na2S2O3浓度(mol/L) | HCl浓度(mol/L) |
| A. | 10 | 0.1 | 0.1 |
| B. | 10 | 0.2 | 0.2 |
| C. | 20 | 0.1 | 0.1 |
| D. | 20 | 0.2 | 0.2 |
| A. | A | B. | B | C. | C | D. | D |
8.下列说法中不正确的是( )
| A. | 化学反应中的能量变化,通常表现为热量的变化 | |
| B. | 反应物的总能量高于生成物的总能量时发生放热反应 | |
| C. | Ba(OH)2•8H2O与NH4Cl的反应是吸热反应 | |
| D. | 在化学反应中需要加热的反应就是吸热反应 |
6.下列关于生铁和钢的叙述正确的是( )
| A. | 由铁矿石炼成铁是化学变化,由生铁炼成钢是物理变化 | |
| B. | 生铁、钢的硬度都比纯铁的大 | |
| C. | 生铁和钢都含有铁元素,它们的性能和用途相差不大 | |
| D. | 生铁可以完全溶解在足量稀盐酸中 |
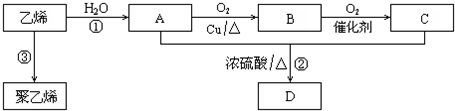
 ;反应类型:加聚反应
;反应类型:加聚反应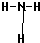 .氨常作致冷剂,是因为氨气具有氨气易液化,挥发后吸收能量使周围温度降低的性质.氨气溶于水得到氨水,氨水显碱性的原因是(用电离方程式表示)NH3•H2O?NH4++OH-.玻璃棒蘸浓盐酸接触氨气时,观察到的现象为冒白烟.
.氨常作致冷剂,是因为氨气具有氨气易液化,挥发后吸收能量使周围温度降低的性质.氨气溶于水得到氨水,氨水显碱性的原因是(用电离方程式表示)NH3•H2O?NH4++OH-.玻璃棒蘸浓盐酸接触氨气时,观察到的现象为冒白烟. 工业上制取氯酸钾的主要步骤为:
工业上制取氯酸钾的主要步骤为: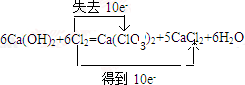 .
.