题目内容
用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
(1)从实验装置上看,图中尚缺少的一种玻璃用品是 .
(2)如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所求中和热 (填“相等、不相等”).
(3)实验时所用盐酸及NaOH溶液的体积均为50mL,各溶液密度均为1g/mL,生成溶液的比热容c=4.18J?g-1?℃-1,实验起始温度为t1℃,终止温度为t2℃.试推断中和热的计算式△H= .

(1)从实验装置上看,图中尚缺少的一种玻璃用品是
(2)如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所求中和热
(3)实验时所用盐酸及NaOH溶液的体积均为50mL,各溶液密度均为1g/mL,生成溶液的比热容c=4.18J?g-1?℃-1,实验起始温度为t1℃,终止温度为t2℃.试推断中和热的计算式△H=
考点:中和热的测定
专题:实验题
分析:(1)根据量热计的构造来判断该装置的缺少仪器;
(2)反应放出的热量和所用酸以及碱的量的多少有关,并根据中和热的概念和实质来回答;
(3)先根据Q=m?c?△T计算反应放出的热量,然后根据△H=-
kJ/mol计算出反应热.
(2)反应放出的热量和所用酸以及碱的量的多少有关,并根据中和热的概念和实质来回答;
(3)先根据Q=m?c?△T计算反应放出的热量,然后根据△H=-
| Q |
| n |
解答:
解:(1)由量热计的构造可知该装置的缺少仪器是环形玻璃搅拌棒,故答案为:环形玻璃搅拌棒;
(2)反应放出的热量和所用酸以及碱的量的多少有关,若用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,生成水的物质的量增多,所放出的热量偏高,但中和热是强酸和强碱反应生成1mol水时放出的热量,与酸碱的用量无关,中和热数值相等;
故答案为:相等;
(3)用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行中和反应生成水的物质的量为0.05L×0.50mol/L=0.025mol,溶液的质量为100ml×1g/ml=100g,温度变化的值为t2-t1,则生成0.025mol水放出的热量为Q=m?c?△T=4.18J/(g?℃)×100mL×1g/cm3(t2-t1)=0.418kJ,所以实验测得的中和热△H=-
=-16.72(t2-t1)kJ/mol;
故答案为:-16.72(t2-t1)kJ/mol.
(2)反应放出的热量和所用酸以及碱的量的多少有关,若用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,生成水的物质的量增多,所放出的热量偏高,但中和热是强酸和强碱反应生成1mol水时放出的热量,与酸碱的用量无关,中和热数值相等;
故答案为:相等;
(3)用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行中和反应生成水的物质的量为0.05L×0.50mol/L=0.025mol,溶液的质量为100ml×1g/ml=100g,温度变化的值为t2-t1,则生成0.025mol水放出的热量为Q=m?c?△T=4.18J/(g?℃)×100mL×1g/cm3(t2-t1)=0.418kJ,所以实验测得的中和热△H=-
| 0.418kJ |
| 0.025mol |
故答案为:-16.72(t2-t1)kJ/mol.
点评:本题考查中和热的测定与计算,题目难度中等,注意理解中和热的概念是解题的关键.

练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目
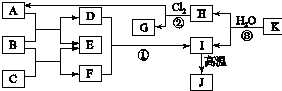 如图中,A、C是工业上用途很广的两种重要化工原料,B为日常生活中常见的金属,H、G是正四面体结构的非极性分子,H是一种重要的能源、燃料,J是一种耐高温材料且是两性氧化物,K是由两种常见元素组成的化合物(图中部分反应物或生成物没有列出).
如图中,A、C是工业上用途很广的两种重要化工原料,B为日常生活中常见的金属,H、G是正四面体结构的非极性分子,H是一种重要的能源、燃料,J是一种耐高温材料且是两性氧化物,K是由两种常见元素组成的化合物(图中部分反应物或生成物没有列出).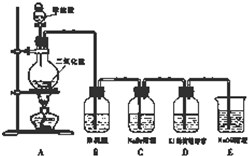 某校研究性学习小组设计实验,制取氯气以探究Cl2、Br2、I2的氧化性强弱(制取氯气的化学方程式为:MnO2+4HCl(浓)
某校研究性学习小组设计实验,制取氯气以探究Cl2、Br2、I2的氧化性强弱(制取氯气的化学方程式为:MnO2+4HCl(浓)